
【题目】下列说法中正确的是
A. 25 ℃时0.1molL﹣1NH4Cl溶液的Kw大于100℃时0.01molL﹣1NaCl溶液的Kw
B. 常温下,pH均为3的醋酸和硫酸铝两种溶液中,由水电离出的氢离子浓度之比为1∶108
C. 根据溶液的pH与酸碱性的关系,推出pH=6.5的溶液一定显酸性
D. 室温下,将pH=2的盐酸与pH=12的氨水等体积混合,溶液显中性
【答案】B
【解析】
A.水的电离吸热,升高温度促进水电离,则离子积常数增大,所以25℃时0.1molL-1NH4Cl溶液的Kw小于100℃时0.1molL-1NaCl溶液的Kw,故A错误;
B.酸抑制水的电离、含有弱离子的盐促进水的电离,则常温下pH=3的醋酸和硫酸铝溶液中由水电离出的c(H+)分别为:![]() mol/L=10-11 mol/L、10-3 mol/L,二者之比为1:108,故B正确;
mol/L=10-11 mol/L、10-3 mol/L,二者之比为1:108,故B正确;
C.温度未知,不能根据溶液的pH判断溶液酸碱性,pH=6.5的溶液可能呈酸性,可能呈碱性,也可能是中性,故C错误;
D.室温下,pH=2的盐酸浓度小于pH=12的氨水浓度,二者等体积混合时氨水过量较多,溶液呈碱性,故D错误;
答案选B。


科目:高中化学 来源: 题型:
【题目】Fe、Co、Ni均为第Ⅷ族元素,它们的化合物在生产、生活中有着广泛的应用。
(1)基态Co原子的价电子排布式为_______,Co2+核外3d能级上有_____对成对电子。
(2)Co3+的一种配离子[Co(N3)(NH3)5]2+中,Co3+的配位数是________。1 mol配离子中所含σ键的数目为________,配位体N3-中心原子的杂化类型为________。
(3)Co2+在水溶液中以[Co(H2O)6]2+存在。向含Co2+的溶液中加入过量氨水可生成更稳定的[Co(NH3)6]2+,其原因是_________________________________________________。
(4)某蓝色晶体晶体结构如图,Fe2+、Fe3+分别占据立方体互不相邻的顶点,而立方体的每条棱上均有一个CN-,K+位于立方体的体心上。据此可知该晶体的化学式为________,立方体中Fe2+间连接起来形成的空间构型是________。K+空缺率(体心中没有K+的占总体心的百分比)为_____________。
(5)NiO的晶胞结构如图甲所示,其中原子坐标参数A为(0,0,0),B为(1,1,0),则C原子坐标参数为________。
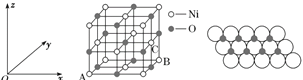
图甲 图乙
(6)一定温度下,NiO晶体可以自发地分散并形成“单分子层”,可以认为O2-作密置单层排列,Ni2+填充其中(如图乙),已知O2-的半径为a pm,每平方米面积上分散的该晶体的质量为________g(用含a、NA的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按第26届国际计量大会重新定义,阿伏加德罗常数(NA)有了准确值6.02214076×1023。下列说法正确的是( )
A.12gNaHSO4在熔融状态下可以电离出的阳离子数目0.1NA
B.用23.5gAgI与水制成的胶体中胶体粒子数目为0.1NA
C.标准状况下,2.24LCl2全部溶于水所得溶液中的Cl-与ClO-数目之和为0.2NA
D.1.0L18.4mol/LH2SO4溶液与足量铜在加热的条件下反应,被还原的H2SO4分子数目为9.2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化氯(ClO2)是极易溶于水且不与水发生化学反应的黄绿色气体,沸点为11℃,某小组在实验室中制备ClO2所用装置如图:[已知:SO2+2NaClO3+H2SO4=2ClO2+2NaHSO4]。
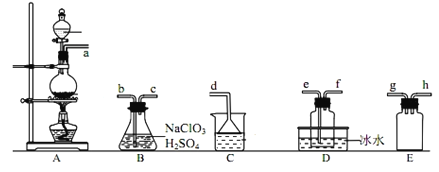
下列说法正确的是( )
A.装置C中装的是饱和食盐水,a流出气体为SO2
B.装置D放冰水的目的是液化二氧化硫防止污染环境
C.连接装置时,导管口a可接h或g,导管口c接e
D.可以选用装置A利用3mo/L盐酸与MnO2反应制备氯气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种利用废干电池中黑色粉末(主要成分MnO2、炭粉及少量Hg2+、Pb2+等重金属盐)制备MnSO4晶体的工艺流程如图:
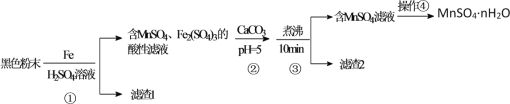
下列说法错误的是( )
A.反应①中1molFe至多还原1.5molMnO2
B.重金属主要在滤渣2中
C.步骤③煮沸可使沉淀颗粒长大,目的是便于固液分离
D.合理处理废旧电池有利于资源再利用并防止汞、铅等重金属污染
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H2S与CO2在高温下发生反应:CO2 (g) + H2S (g) ![]() COS (g) + H2O (g)。在610 K时,将0.10 mol CO2与0.40 mol H2S充入2.5 L的空钢瓶中,反应平衡后水的物质的量分数为0.02。下列说法不正确的是
COS (g) + H2O (g)。在610 K时,将0.10 mol CO2与0.40 mol H2S充入2.5 L的空钢瓶中,反应平衡后水的物质的量分数为0.02。下列说法不正确的是
A. 升高温度,H2S浓度增加,表明该反应是放热反应
B. 通入CO2后,正反应速率先增大后减小
C. H2S的平衡转化率α = 4.5 %
D. 反应平衡常数K = 1/351
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于反应:MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O说法不正确的是
MnCl2+Cl2↑+2H2O说法不正确的是
A.反应中氧化剂与还原剂物质的量之比为1:2
B.要使8.7g MnO2完全反应,需投入含0.4molHCl的浓盐酸
C.每生成标准状况下2.24L Cl2,就有7.3gHCl被氧化
D.若有0.4molHCl被氧化,反应中转移的电子数为0.4×6.02×1023
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(13分)用辉铜矿(主要成分为 Cu2S,含少量Fe2O3、SiO2,等杂质)制备难溶于水的碱式碳酸铜的流程如下:
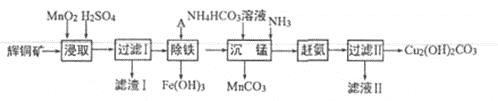
(1)下列措施是为了加快浸取速率,其中无法达到目的的是____(填字母)。
A.延长浸取时间 | B.将辉铜矿粉碎 |
C.充分搅拌 | D.适当增加硫酸浓度 |
(2)滤渣I巾的主要成分是MnO2、S、SiO2,请写出“浸取”反应中生成S的离子方程式:_______。
(3)研究发现,若先除铁再浸取,浸取速率明显变慢,可能的原因是___________。
(4)“除铁”的方法是通过调节溶液pH,使Fe3+转化为Fe(OH)3,则加入的试剂A可以是_______(填化学式);“赶氨”时,最适宜的操作方法是________。
(5)“沉锰”(除Mn2+)过程中有关反应的离子方程式为_______。
(6)滤液Ⅱ经蒸发结晶得到的盐主要是___________(填化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有下列物质:①稀硫酸 ②小苏打 ③氨水 ④二氧化碳 ⑤FeCl3固体 ⑥稀NaOH溶液 ⑦硝酸亚铁溶液。
(1)上述物质中属于电解质的物质序号为______ 。
(2)有两种物质发生反应的离子方程式为:H++OH-=H2O,这两种物质的序号是______。
(3)加入盐酸、NaOH溶液均能发生化学反应的物质序号为______。
(4)能导电的物质序号为_______________。
(5)④与⑥充分反应后,将溶液小火蒸干,得到固体混合物。固体组成成分可能是(用化学式表示)___________________________。
(6)实验室用⑤制备胶体的化学方程式为_______________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com