
【题目】现有下列物质:①稀硫酸 ②小苏打 ③氨水 ④二氧化碳 ⑤FeCl3固体 ⑥稀NaOH溶液 ⑦硝酸亚铁溶液。
(1)上述物质中属于电解质的物质序号为______ 。
(2)有两种物质发生反应的离子方程式为:H++OH-=H2O,这两种物质的序号是______。
(3)加入盐酸、NaOH溶液均能发生化学反应的物质序号为______。
(4)能导电的物质序号为_______________。
(5)④与⑥充分反应后,将溶液小火蒸干,得到固体混合物。固体组成成分可能是(用化学式表示)___________________________。
(6)实验室用⑤制备胶体的化学方程式为_______________________。
【答案】②⑤ ①⑥ ②⑦ ①③⑥⑦ NaOH和Na2CO3 、NaHCO3和Na2CO3 FeCl3+3H2O![]() Fe(OH)3(胶体)+3HCl
Fe(OH)3(胶体)+3HCl
【解析】
根据物质的组成和性进行分析,根据电解质、离子方程式的内涵和外延进行分析。
现有下列物质:①稀硫酸 ②小苏打 ③氨水 ④二氧化碳 ⑤FeCl3固体 ⑥稀NaOH溶液 ⑦硝酸亚铁溶液。
(1)酸、碱、盐、活泼金属的氧化物等物质属于电解质,上述物质中小苏打和FeCl3固体都属于盐,故属于电解质的物质序号为②⑤。
(2)H++OH-=H2O,该离子方程式可表示强酸或强酸的酸式盐与强碱在水溶液中反应生成水和可溶性盐的反应,上属物质中稀硫酸和稀NaOH溶液满足要求,因此这两种物质的序号是①⑥。
(3)小苏打能与盐酸反应生成二氧化碳、氯化钠和水,也能与氢氧化钠溶液反应生成碳酸钠和水;硝酸亚铁溶液中加入盐酸后,硝酸根在酸性条件下表现强氧化性,可以把亚铁离子氧化为铁离子,硝酸亚铁溶液中加入氢氧化钠溶液后可以生成氢氧化亚铁沉淀,因此,加入盐酸、NaOH溶液均能发生化学反应的物质序号为②⑦。
(4)若溶液中有大量自由移动的离子则该溶液能导电。上述物质中,稀硫酸、氨水、稀NaOH溶液和硝酸亚铁溶液均为电解质溶液,满足要求,因此,能导电的物质序号为①③⑥⑦。
(5)二氧化碳与稀NaOH溶液充分反应后,可能生成Na2CO3或NaHCO3,NaOH有可能过量。此溶液小火蒸干,NaHCO3不会完全分解;NaHCO3和NaOH不能大量共存。因此,若得到固体混合物,则固体组成成分可能是NaOH和Na2CO3 或NaHCO3和Na2CO3。
(6)实验室用FeCl3固体配制成饱和溶液,然后向沸水中滴加少量的FeCl3饱和溶液,加热到液体呈红褐色即可得到Fe(OH)3胶体,制备该胶体的化学方程式为FeCl3+3H2O![]() Fe(OH)3(胶体)+3HCl 。
Fe(OH)3(胶体)+3HCl 。


科目:高中化学 来源: 题型:
【题目】一定温度下,三种碳酸盐MCO3(M:Mg2+、Ca2+、Mn2+)的沉淀溶解平衡曲线如下图所示。已知: pM="-lg" c(M),pc(CO32-)=" -lg" cc(CO32-)。下列说法正确的是 ( )

A. MgCO3、CaCO3、MnCO3的Ksp依次增大
B. a 点可表示MnCO3的饱和溶液,且c(Mn2+)= c(CO32-)
C. b 点可表示CaCO3的饱和溶液,且c(Ca2+)<c(CO32-)
D. c 点可表示MgCO3的不饱和溶液,且c(Mg2+)<c(CO32-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】四氯化锡可用作媒染剂。利用如图所示装置可以制备四氯化锡(部分夹持装置已略去);

有关信息如下表:
化学式 | SnCl2 | SnCl4 |
熔点/℃ | 246 | -33 |
沸点/℃ | 652 | 144 |
其他性质 | 无色晶体,易氧化 | 无色液体,易水解 |
回答下列问题:
(1)甲装置中仪器A的名称为___________。
(2)用甲装置制氯气,MnO4- 被还原为Mn2+,该反应的离子方程式为________________。
(3)将装置如图连接好,检查气密性,慢慢滴入浓盐酸,待观察到__________(填现象)后,开始加热丁装置,锡熔化后适当增大氯气流量,继续加热丁装置,此时继续加热丁装置的目的是:
①促进氯气与锡反应;
②_______________________________。
(4)如果缺少乙装置,可能发生的副反应的化学方程式为___________________;己装置的作用是_________________:
A.除去未反应的氯气,防止污染空气
B.防止空气中CO2气体进入戊装置
C.防止水蒸气进入戊装置的试管中使产物水解
D.防止空气中O2进入戊装置的试管中使产物氧化
(5)某同学认为丁装置中的反应可能产生SnCl2杂质,以下试剂中可用于检测是否产生SnCl2 的有_______________(填标号)。
A. H2O2溶液 B. FeCl3溶液(滴有KSCN) C. AgNO3溶液 D. 溴水
(6)反应中用去锡粒1.19g,反应后在戊装置的试管中收集到2.38gSnCl4,则SnCl4的产率为________。(保留3位有效数字)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1).对于下列反应:2SO2 + O2 ![]() 2SO3 , 如果2min内SO2的浓度由6 mol/L下降为2 mol/L,那么,用SO2浓度变化来表示的化学反应速率为__________,用O2浓度变化来表示的反应速率为__________。
2SO3 , 如果2min内SO2的浓度由6 mol/L下降为2 mol/L,那么,用SO2浓度变化来表示的化学反应速率为__________,用O2浓度变化来表示的反应速率为__________。
(2)反应N2+3H2![]() 2NH3 ΔH<0 ,达平衡后,不同时刻改变外界条件时正逆反应速率变化如图,请判断某时刻所改变的条件。
2NH3 ΔH<0 ,达平衡后,不同时刻改变外界条件时正逆反应速率变化如图,请判断某时刻所改变的条件。

可能改变的外界条件:t1__________,t2__________ ,t3__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实不能用平衡移动原理解释的是
A. 夏天打开啤酒瓶盖后产生大量气泡
B. 浓氨水中加入NaOH 固体产生有刺激性气味气体
C. 实验室用排饱和食盐水的方法收集氯气
D. 压缩H2和I2反应的平衡混合气体,气体颜色变深
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高血脂是一种常见的心血管疾病,治疗高血脂的新药I的合成路线如下:

已知:
回答下列问题:
(1)反应①所需试剂、条件分别是____________;F 的化学名称为____________。
(2)②的反应类型是______________;A→B 的化学方程式为_________________。
(3)G 的结构简式为______________;H 中所含官能团的名称是____________。
(4)化合物W 的相对分子质量比化合物C 大14,且满足下列条件,W 的可能结构有__种。
①遇FeCl3 溶液显紫色②属于芳香族化合物③能发生银镜反应其中核磁共振氢谱显示有5 种不同化学环境的氢,峰面积比为2:2:2:1:1,写出符合要求的W 的结构简式____________。
(5)设计用甲苯和乙醛为原料制备 的合成路线,其他无机试剂任选(合成路线常用的表示方式为:
的合成路线,其他无机试剂任选(合成路线常用的表示方式为: )____________。
)____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙醇分子中各种化学键如下图所示,

下列关于反应的断键位置的说明错误的是( )
A. 乙醇和乙酸、浓H2SO4共热时断键②
B. 乙醇和金属钠的反应断键①
C. 乙醇和浓H2SO4共热到170℃时断键②⑤
D. 乙醇在Ag催化下与O2反应时断键①③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以硼氢化合物NaBH4(B元素的化合价为+3价)和H2O2作原料的燃料电池,负极材料采用Pt/C,正极材料采用MnO2,其工作原理如图所示。下列说法正确的是
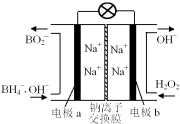
A.电池放电时Na+从b极区移向a极区
B.该电池的负极反应为:BH4-+8OH--8e-===BO2-+6H2O
C.电极a采用MnO2,MnO2既作电极材料又有催化作用
D.每消耗3 mol H2O2,转移的电子为3 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是N2(g)和H2(g)反应生成1molNH3(g)过程中能量变化示意图,下列说法不正确的是

A. 该反应的热化学方程式为N2(g)+3H2(g)![]() 2NH3(g) △H =-92kJ·mol-1
2NH3(g) △H =-92kJ·mol-1
B. 若在反应体系中加入高效催化剂,E1、E2和△H均减小
C. 若已知H-H的键能和N-H的键能,可求得N![]() N的键能
N的键能
D. 反应2NH3(g)![]() N2(g)+3H2(g)的△S>0
N2(g)+3H2(g)的△S>0
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com