
【题目】关于卤素单质(X2)的下列叙述中正确的是
A. 都能与氢气化合发生爆炸B. 都能与水剧烈反应
C. 都能与钠反应生成NaXD. 都能与铁反应生成FeX3
 新思维小冠军100分作业本系列答案
新思维小冠军100分作业本系列答案 名师指导一卷通系列答案
名师指导一卷通系列答案科目:高中化学 来源: 题型:
【题目】某同学用沉淀法测定Na2SO3和NaCl固体混合物中Na2SO3的质量分数.操作流程如下: 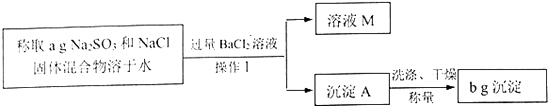
(1)操作I所用到的玻璃仪器有烧杯、玻璃棒、 .
(2)操作I之前,为判断所加BaCl2溶液是否过量,设计如下方案,其中最合理的是 .
A.取少量上层清液,继续滴加稀H2SO4 , 若沉淀产生则说明BaCl2已过量
B.待浊液澄清后,继续滴加BaCl2溶液,若无沉淀产生则说明BaCl2已过量
C.待浊液澄清后,继续滴加稀H2SO4 , 若沉淀产生则说明BaCl2已过量
(3)根据操作流程中的数据计算Na2SO3的质量分数 .
(4)该同学认真分析,上述实验操作均正确,但发现实验结果与预期相差较大,请你推测可能的原因 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲、乙两化学兴趣小组安装两套如图1相同装置,用以探究影响H2O2分解速率的因素. 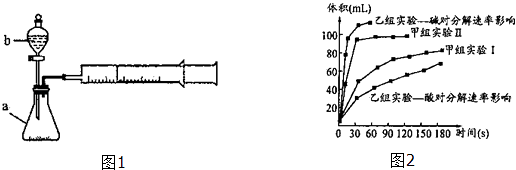
(1)仪器b的名称: .
(2)甲小组有如下实验设计方案,请帮助完成下列填空.
实验编号 | 实验目的 | t℃ | 催化剂 | 浓度 |
甲组实验Ⅰ | 做实验参照 | 25 | 10mL 2%H2O2 | |
甲组实验Ⅱ | 探究浓度对速率的影响 | 25 | 10mL 5%H2O2 |
(3)甲、乙两小组得出如图2数据. ①由甲组实验得出的数据可知:浓度越大,H2O2分解速率(填“越快”、“越慢”);
②由乙组研究的酸、碱对H2O2分解影响因素的数据分析相同条件下,Na2O2和K2O2溶于水放出气体速率较快的是;
③乙组提出可以用BaO2固体与H2SO4溶液反应制H2O2 , 其化学反应方程式为;支持这一方案的理由是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种新型的乙醇电池,它用磺酸类质子溶剂.电池总反应为:C2H5OH+3O2→2CO2+3H2O,电池示意如图,下列说法正确的是( )
A.a极为电池的正极
B.电池工作时电流由a极沿导线经灯泡再到b极
C.电池负极的电极反应为:4H++O2+4e﹣=2H2O
D.电池工作时,1mol乙醇被氧化时就有12mol电子转移
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某100mL溶液可能含有Na+、NH4+、Fe3+、CO32﹣、SO42﹣、Cl﹣中的若干种,取该溶液进行连续实验,实验过程如图:(所加试剂均过量,气体全部逸出)下列说法不正确的是( ) 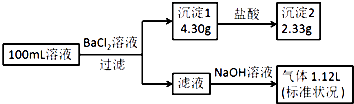
A.原溶液一定存在CO32﹣和SO42﹣ , 一定不存在Fe3+
B.原溶液一定存在Cl﹣ , 可能存在Na+
C.原溶液中c(Cl﹣)≥0.1molL﹣1
D.若原溶液中不存在Na+ , 则c(Cl﹣)<0.1molL﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验中能得到Fe2O3 的是( )
A.铁丝在纯氧中燃烧
B.红热的铁和水蒸气反应
C.将Fe2(SO4)3 溶液蒸干后灼烧
D.加热氢氧化铁固体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知亚硫酸钠在空气中能被氧气氧化生成硫酸钠.某同学为探究Na2SO3溶液是否发生变质,设计如下实验测定1.0molL﹣1Na2SO3溶液的实际浓度. 
(1)分液漏斗中应加入足量的下列哪种试剂?(填选项)
A.浓硝酸
B.65%硫酸
C.浓盐酸
(2)实验前后C装置增重3.2g,则测得Na2SO3溶液的物质的量浓度为molL﹣1 .
(3)该实验装置还存在一个明显的缺陷是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关金属性质的叙述正确的是( )
A.都具有很高的熔点
B.最外层电子数少于 3 个的都是金属
C.都能导电、传热
D.都只能和酸不能和碱发生化学反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com