
【题目】下列说法正确的是
A.氧化还原反应中可能只有一种元素的化合价发生变化
B.金属离子被还原一定得到金属单质
C.阳离子只有氧化性,阴离子只有还原性
D.在氧化还原反应中,氧化剂与还原剂不可能是同一种物质
科目:高中化学 来源: 题型:
【题目】Ⅰ.如图是某学生绘制的实验室分馏石油的装置图:
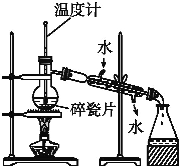
(1)实验室分馏石油的正确操作顺序是E→___→ →A→C→ → 。
A.连接接液管
B.装入碎瓷片(沸石)和石油,塞上带温度计的塞子
C.检查装置气密性
D.连接冷凝管及进出水管
E.在铁架台上放酒精灯,固定好铁圈,放上石棉网
F.固定好蒸馏烧瓶,调节好温度计的位置
G.加热
(2)装置图中有两处错误,它们分别是:
①冷凝管中进水口和出水口接反了;
②______________________________________________________。
Ⅱ. 由石油裂化和裂解得到的乙烯、丙烯来合成丙烯酸乙酯的路线如下:
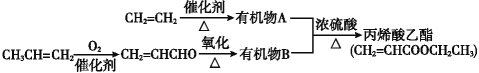
根据以上材料和你所学的化学知识回答下列问题:
(3)由![]() 制得有机物A的化学方程式是________________,反应类型是___。
制得有机物A的化学方程式是________________,反应类型是___。
(4)由A与B合成丙烯酸乙酯的化学方程式是______________________,反应类型是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室按照图1所示装置制备氯酸钾、氯水并进行有关探究实验。
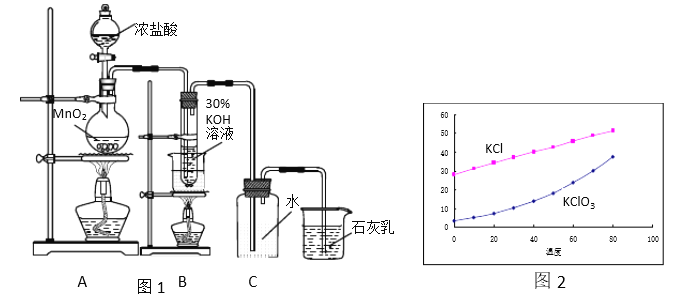
Ⅰ实验一 制取氯酸钾和氯水
(1)A中发生反应的化学方程式是_____________。
(2)制备KClO3需在70℃~80℃进行,写出制备KClO3的离子方程式______。
(3)装置C的作用是_____ 。
(4)KCl 和KClO3的溶解度如图2所示。反应结束后,将装置B中的溶液放到冰水浴中, 20秒后会析出较多晶体X。这样做是因为________(选填a、b、c):
a. KClO3溶解度受温度影响较大而KCl溶解度受温度影响较小
b. 0℃时,KClO3溶解度比KCl小
c. 溶液中的溶质主要是KClO3
所以在冷却过程中晶体X会沉淀析出,X的化学式是_______。
(5)上一步操作会不可避免地使另一种物质同时析出,因此要获得较纯净的X,需要进行的具体的操作步骤是_________________。
Ⅱ实验二 氯酸钾性质研究
(6)在不同条件下KClO3可将KI氧化为不同的产物。该小组设计了如下实验,研究反应条件对反应产物的影响(实验在室温下进行):
0.20 mol·L KI/ mL | KClO3(s) /g | 6.0 mol·L-1 H2SO4/ mL | 蒸馏水/ mL | |
试管1 | 1.0 | 0.10 | 0 | 9.0 |
试管2 | 1.0 | 0.10 | 3.0 | 6.0 |
①该实验的实验目的是__。
②设计试管1实验的作用是_____。
③实验后发现,试管2中产生黄色溶液,该同学预测KI被氧化为I2。用离子方程式表示该同学的预测____________;请设计2种实验方案验证该预测正确(从加入试剂、现象、结论等方面描述)______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某酸H2A在水中存在下列电离:①H2A=H++HA- ②HA- ![]() H++A2- , 下列说法一定正确的是( )
H++A2- , 下列说法一定正确的是( )
A.Na2A溶液中一定有:c(OH-)= c(H+)+c(HA-)
B.Na2A溶液呈碱性,NaHA溶液可能酸性可能呈碱性
C.Na2A溶液中一定有c(Na+)+c(H+)= c(OH-)+c(A2-) +c(HA-)
D.NaHA溶液一定有c(Na+)>c(HA) >c(OH-)>c(H2A) >c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】298K时,二元弱酸H2X溶液中含X微粒的分布分数如图所示。下列叙述正确的是

A. 溶液呈中性时: c(Na+)=2c(X2-)
B. Ka2(H2X)为10-7
C. NaHX溶液c( H+)< c(OH-)
D. 溶液pH由1开至2.6时主要存在的反应是: H2X +OH-=HX-+ H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二硫化钼(MoS2) 被誉为“固体润滑剂之王”,利用低品质的辉钼矿( 含MoS2、SiO2以及CuFeS2等杂质) 制备高纯二硫化钼的一种生产工艺如下:
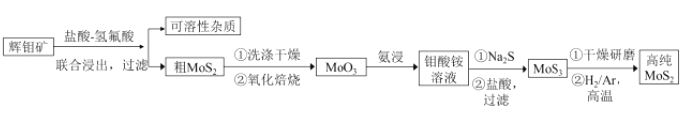
回答下列问题:
(1)钼酸铵的化学式为(NH4)2MoO4,其中Mo的化合价为________.
(2)利用联合浸出除杂时,氢氟酸可除去的杂质化学式为________如改用FeCl3溶液氧化浸出,CuFeS2杂质的浸出效果更好,写出氧化浸出时发生的化学反应方程式________。
(3)加入Na2S后,钼酸铵转化为硫代钼酸铵[(NH4)MoS4],写出(NH4)2MoS4与盐酸生成MoS3沉淀的离子反应方程式____________。
(4)由下图分析产生三硫化钼沉淀的流程中应选择的最优温度和时间是___________。
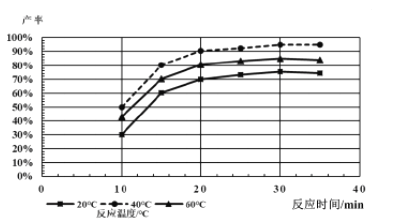
利用化学平衡原理分析低于或高于最优温度时,MoS3的产率均下降的原因:__________。
(5)高纯MoS2中3然会存在极微量杂质,如非整比晶体MoS2.8,则该杂质中Mo4+与Mo6+的物质的量之比为________________。
(6)已知Ksp(BaSO4) =1.1×10-10,Ksp(BaMoO4)=4.0×10-8),钼酸钠品体( NaMoO4·2H2O) 是新型的金属缓蚀剂,不纯的钼酸钠溶液中若含少量可溶性硫酸盐杂质,可加入Ba(OH)2固体除去SO42-(溶液体积变化忽略),则当BaMoO4开始沉淀时,溶液中的c(MoO42-)/c(SO42-)___________(结果保留2位有效数字)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】了解有机物分子中化学键特征以及成键方式是研究有机物性质的基础。下列关于有机物分子的成键方式的描述不正确的是( )
A. 烷烃分子中碳原子均采用sp3杂化轨道成键
B. 炔烃分子中碳碳叁键由1个σ键、2个π键组成
C. 甲苯分子中所有碳原子均采用sp2杂化轨道成键
D. 苯环中存在6个碳原子共有的大π键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表物质与其所含化学键类型、所属化合物类型不正确的一组是( )
选 项 | A | B | C | D |
物 质 | Na2O2 | H2O | HCl | NaCl |
所含化学键类型 | 离子键、共价键 | 共价键 | 离子键 | 离子键 |
所属化合物类型 | 离子化合物 | 共价化合物 | 离子化合物 | 离子化合物 |
A.A
B.B
C.C
D.D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com