
【题目】α—甲基苯乙烯(AMS)在有机合成中用途广泛,以下是用苯为原料合成AMS,并进一步制备香料龙葵醛的路线:
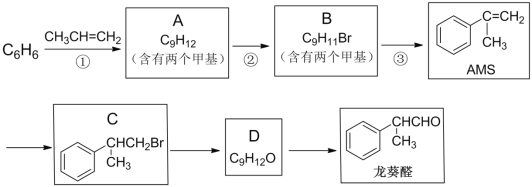
完成下列填空:
(1)反应①的反应类型是____;反应③所需的试剂与条件是____。
(2)写出反应②的化学方程式:____。
(3)AMS可以自身聚合,写出该高聚物的结构简式:____。
(4)写出同时满足下列条件的龙葵醛的一种同分异构体的结构简式:____。
i. 苯环上的一氯代物有两种
ii. 分子中没有甲基
iii. 能与金属钠产生H2
(5)有人认为仅用反应②就能得到C,事实证明产物中C的含量远远小于B。由该事实可以得到的结论是____。
(6)设计一条由AMS合成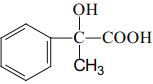 的合成路线____。(合成路线常用的表示方式为:A
的合成路线____。(合成路线常用的表示方式为:A ![]() B。。。
B。。。![]() 目标产物)
目标产物)
【答案】加成反应 NaOH醇溶液、加热 ![]() +Br2
+Br2![]()
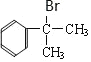 +HBr
+HBr 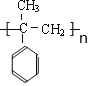
![]() 或
或![]() 或
或![]() 中的任意一种 与苯环直接相连碳上氢更容易被取代(
中的任意一种 与苯环直接相连碳上氢更容易被取代(![]() 氢原子比—CH3氢原子更易被取代)
氢原子比—CH3氢原子更易被取代) ![]()
![]()
【解析】
用苯为原料合成AMS,由合成流程可知反应①为苯与丙烯的加成反应生成![]() ,则A为
,则A为![]() ,在光照条件下发生侧链上取代反应生成B(含两个甲基),则B为
,在光照条件下发生侧链上取代反应生成B(含两个甲基),则B为 ;B发生消去反应生成AMS为
;B发生消去反应生成AMS为![]() ;AMS再与溴化氢发生加成反应生成
;AMS再与溴化氢发生加成反应生成![]() ,
,![]() 在碱性条件下加热,发生水解反应生成B为
在碱性条件下加热,发生水解反应生成B为![]() ,B发生催化氧化反应生成龙葵醛;
,B发生催化氧化反应生成龙葵醛;
(6)由AMS合成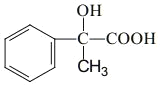 ,先与氯气发生加成反应,再水解,最后发生氧化反应。
,先与氯气发生加成反应,再水解,最后发生氧化反应。
(1)反应①为苯与丙烯的加成反应,其反应类型是加成反应;反应③为 的消去反应,反应所需的试剂与条件是NaOH醇溶液、加热,
的消去反应,反应所需的试剂与条件是NaOH醇溶液、加热,
故答案为:加成反应;NaOH醇溶液、加热;
(2)反应②为苯丙烷与溴单质发生取代反应的过程,其化学方程式为![]() +Br2
+Br2![]()
 +HBr;
+HBr;
(3)AMS可以自身聚合,该高聚物的结构简式为 ;
;
(4)龙葵醛的一同分异构体满足苯环上的一溴代物有两种,则说明苯环上有两个取代基,属于对位关系;能与金属钠产生H2,则说明分子中含有羟基又满足没有甲基的条件,则该分子的结构简式为![]() 或
或![]() 或
或![]() ,
,
故答案为:![]() 或
或![]() 或
或![]() 中的任意一种;
中的任意一种;
(5)取代反应副产物较多,而且取代反应与分子结构有关,若A直接用过取代反应
得到C,则含量远远小于B,因与苯环直接相连碳上氢更容易被取代(![]() 氢原子比—CH3氢原子更易被取代),故答案为:与苯环直接相连碳上氢更容易被取代(
氢原子比—CH3氢原子更易被取代),故答案为:与苯环直接相连碳上氢更容易被取代(![]() 氢原子比—CH3氢原子更易被取代);
氢原子比—CH3氢原子更易被取代);
6)根据上述合成路线可知,由AMS合成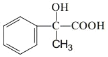 ,先与溴发生加成反应,再水解,最后发生氧化反应,合成流程为:
,先与溴发生加成反应,再水解,最后发生氧化反应,合成流程为:![]()
![]() 。
。


科目:高中化学 来源: 题型:
【题目】下面是某科研小组利用废铁屑还原浸出软锰矿(主要成分为MnO2)制备硫酸锰及电解其溶液制锰的工艺流程图:
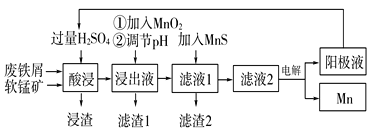
已知:①浸出液中主要含有Fe3+、Fe2+、Co2+、Ni2+等杂质金属离子;
②生成氢氧化物的pH见下表:
物质 | Fe(OH)2 | Fe(OH)3 | Ni(OH)2 | Co(OH)2 | Mn(OH)2 |
开始沉淀的pH | 7.5 | 2.7 | 7.7 | 7.6 | 8.3 |
完全沉淀的pH | 9.7 | 3.7 | 8.4 | 8.2 | 9.8 |
请回答下列问题:
(1)“酸浸”前将原料粉碎的目的是____。
(2)流程图中“①加入MnO2”的作用____,MnO2还可以用其他试剂____(填化学式)代替。
(3)流程图中“②调节pH”可以除去某种金属离子,应将溶液pH调节控制的范围是___~7.6。上述流程中,能循环使用的一种物质是___(填化学式)。
(4)向滤液Ⅰ中加入MnS的作用是除去Co2+、Ni2+等离子,其中可以发生反应为MnS(s)+Ni2+(aq)=NiS(s)+Mn2+(aq)等。当该反应完全后,滤液2中的Mn2+与Ni2+的物质的量浓度之比是___[已知Ksp(MnS)=2.8×10-10,Ksp(NiS)=2.0×10-21]。
(5)在适当条件下,在MnSO4、H2SO4和H2O为体系的电解液中电解也可获得MnO2,其阳极电极反应式为____。
(6)层状镍钴锰三元材料可作为锂离子电池正极材料,其化学式为LiNixCoyMnzO2,其中Ni、Co、Mn的化合价分别为+2、+3、+4。当x=y=![]() 时,z=___。
时,z=___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关物质的转化关系如下图所示。C是海水中最多的盐,D是常见的无色液体。E和G为无色气体,其中E能使湿润的红色石蕊试纸变蓝。B、C、I、J的焰色反应为黄色,其中I可用于制发酵粉或治疗胃酸过多。

⑴F的化学式为______。E的电子式为______。
⑵写出反应①的离子方程式:______。
⑶写出反应②的化学方程式:______。
⑷写出反应③的化学方程式:______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用下列装置验证SO2的某些性质(加热及夹持装置略去)。
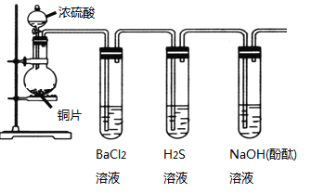
(1)装有浓硫酸的仪器名称是____________。
(2)铜与浓硫酸反应的化学方程式是____________________________________。
(3)能验证SO2具有氧化性的实验现象是_____________________________。
(4)装有BaCl2溶液的试管中无任何现象,将其分成两份,分别滴加氨水和氯水,均产生白色沉淀,沉淀的化学式分别是______,_____。
(5)写出SO2显示还原性并生成白色沉淀的总的离子方程式____________________________。
(6)能验证SO2具有酸性氧化物的通性的实验现象_____。若通入过量的SO2,则其总反应的离子反应方程式是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】牛至是一种质地坚硬、树枝茂密的多年生药草。从牛至精油中提取的三种活性成分的结构简式如图所示。下列说法错误的是( )
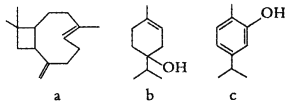
A.a、b、c均能发生加成反应和取代反应
B.b分子存在属于芳香族化合物的同分异构体
C.c分子中至少有8个碳原子共面
D.完全燃烧1mol三种物质时,消耗氧气的量a>b>c
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是 ( )
A.0.1molNH3中含有中含有的原子数为0.3NA
B.0.2molNaCl中含有的离子总数为0.2NA
C.9.8g H2SO4即为0.1mol H2SO4
D.1molH2O中含有2mol氢和1mol氧
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】诺贝尔奖获得者屠呦呦带领团队发现了青蒿素,为中国医药科技创新和人类健康事业作出了巨大贡献,我国化学家在确认青蒿素分子结构后实现了青蒿素的全合成。一种以香茅醛为原料合成青蒿素的流程如图:
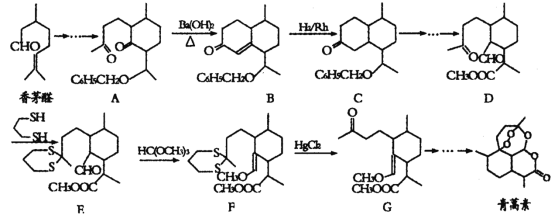
已知:羰基α—H可发生反应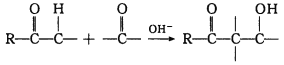
回答下列问题:
(1)青蒿素的分子式为__。根据青蒿素所含官能团,推测其可能具有的性质有___。
a.易溶于水 b.具有氧化性 c.可发生水解反应
(2)香茅醛的同分异构体X含有醛基和六元碳环,且环上只有一个支链,满足上述条件的X有__种,其中核磁共振氢谱峰数最少的物质结构简式为__。
(3)反应A→B实际上可看作两步进行,依次发生的反应类型是__、__。
(4)C中所含官能团名称为__。
(5)通过D→E的反应,分子中引入了硫醚基团,而F→G的反应,分子中硫醚基团又被脱去,这样做的目的是__。
(6)写出由苯甲醛和氯乙烷为原料,制备苄基乙醛(![]() )的合成路线流程__(无机试剂任选)。
)的合成路线流程__(无机试剂任选)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硼酸(H3BO3)是一种重要的化工原料,广泛应用于玻璃、医药、肥料等工艺。一种以硼镁矿(含 Mg2B2O5·H 2O、SiO2 及少量 Fe2O3、Al2O3)为原料生产硼酸及轻质氧化镁的工艺流程如下:

已 知 :H3BO3+H2O![]() H++B(OH)
H++B(OH)![]() ,Ka = 5.81×10 10
,Ka = 5.81×10 10
(1)“吸收”过程中反应的化学方程式为_________________________________。
(2)“滤渣 1”的主要成分有_____。
(3)为检验“过滤 1”后的滤液中是否含有 Fe3+离子,可选用的化学试剂是____________________________。
(4)在“过滤 2”前,将溶液 pH 调节至 3.5,目的是_____。
(5)在“沉镁”中生成 Mg(OH)2·MgCO3 沉淀的离子方程式为________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高铁酸钾(K2FeO4)是一种新型、高效、多功能水处理剂,其消毒后被还原为Fe(OH)3;又可以有净水的功能,是一种无二次污染的绿色水处理剂。工业上制备方法有:①湿法:次氯酸盐氧化法②干法:高温过氧化物法。
(1)湿法制备的主要反应方程为Fe(OH)3+KClO+KOH=K2FeO4+KCl+H2O,配平上述反应化学方程式___。
(2)干法制备中牵涉到的物质有:FeSO4、K2FeO4、K2SO4、K2O2,将氧化剂与还原剂填入空格中,并标出电子转移的方向和数目___。
(3)制备相同质量 K2FeO4 时转移的电子数,湿法制备 ___干法制备(填“>” “<”或“=”)。
(4)高铁酸钾和二氧化氯(其还原产物为 Cl—)都是高效杀菌消毒剂,但消毒效率(单位质量转移的电子数)是不相同的,则高铁酸钾的效率是二氧化氯的___倍。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com