
����Ŀ����Ba(OH)2��Һ����μ���ϡ���ᣬ������������⣺
��1��д����Ӧ�����ӷ���ʽ____________________��
��2��������������£����ӷ���ʽ�루1����ͬ����_____������ţ���
A.��NaHSO4��Һ�У���μ���Ba(OH)2��Һ����Һ������
B.��NaHSO4��Һ�У���μ���Ba(OH)2��Һ��SO42-ǡ����ȫ����
C.��NaHSO4��Һ�У���μ���Ba(OH)2��Һ������
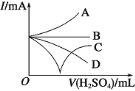
��3������������ϡ����ֱ�����������������л����Һ�ĵ����������õ���ǿ��![]() ��ʾ���ɽ��Ƶ���ͼ�е�_____���߱�ʾ������ţ���
��ʾ���ɽ��Ƶ���ͼ�е�_____���߱�ʾ������ţ���
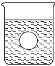
��4������һ����⻬������С��������Ba(OH)2��Һ���룬��ͼ��ʾ������ձ��ﻺ��ע����Ba(OH)2��Һ���ܶȵ�ϡ������ǡ����ȫ��Ӧ���ڴ�ʵ������У�С��_____��ѡ�����ϸ������������������½�������
���𰸡�![]() A C �½�
A C �½�
��������
��1���������������ᷴӦ�������ᱵ������ˮ��
��2��A��NaHSO4��Һ�У���μ���Ba(OH)2��Һ����Һ�����ԣ���Ӧ���������ơ����ᱵ��ˮ��
B����NaHSO4��Һ�У���μ���Ba(OH)2��Һ��SO42-ǡ����ȫ��������Ӧ�������ᱵ���������ƺ�ˮ��
C����NaHSO4��Һ�У���μ���Ba(OH)2��Һ����������Ӧ�������ᱵ���������ƺ�ˮ��
��3������ϡ����ֱ��������ǡ�÷�Ӧʱ������Ϊ0������������Ũ������������ǿ��
��4������С��������Ba(OH)2��Һ���룬˵������С����������ڸ�������ע��ϡ���������Ӧ��Ba2++2OH+2H++SO42�TBaSO4��+2H2O�����ʵ�������С��������Һ���ܶȱ�С�����������ܸ�����С�������ڴ�ʵ������У�С�����½���
��1����Ba(OH)2��Һ����μ���ϡ���ᣬ���ӷ���ʽΪBa2++2OH+2H++SO42�TBaSO4��+2H2O��
�ʴ�Ϊ��Ba2++2OH+2H++SO42�TBaSO4��+2H2O��
��2��A. ��NaHSO4��Һ�У���μ���Ba(OH)2��Һ����Һ�����ԣ���Ӧ�����ӷ���ʽΪ��Ba2++2OH+2H++SO42�TBaSO4��+2H2O��A����ȷ��
B. ��NaHSO4��Һ�У���μ���Ba(OH)2��Һ��SO42ǡ����ȫ��������Ӧ�����ӷ���ʽΪ��Ba2++OH+H++SO42�TBaSO4��+H2O��B�����
C. ��NaHSO4��Һ�У���μ���Ba(OH)2��Һ����������Ӧ�����ӷ���ʽΪ��Ba2++OH+H++SO42=BaSO4��+H2O��C�����
�ʴ�Ϊ��A��
��3������ϡ����ֱ��������ǡ�÷�Ӧʱ������Ϊ0������������Ũ������������ǿ��ͼ��ֻ��C���ϣ�
�ʴ�Ϊ��C��
��4������С��������Ba(OH)2��Һ���룬˵������С����������ڸ�������ע��ϡ���������Ӧ��Ba2++2OH+2H++SO42�TBaSO4��+2H2O�����ʵ�������С��������Һ���ܶȱ�С�����������ܸ�����С�������ڴ�ʵ������У�С�����½���
�ʴ�Ϊ���½���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾ�����ת����ϵ��

�Իش�
(1)д��B�Ļ�ѧʽ____________��C��Һ��______________��
(2)д����Eת���F������Ӧ�Ļ�ѧ����ʽ_______________��
(3)����G��Һ�������ӵIJ���������ʵ������__________________��
(4)��G��Һ�м���A�����ӷ���ʽ____________________��
(5)д��D��Һ�м���AgNO3�õ���ɫ���������ӷ���ʽ__________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ����( )
A. ��ϩ����ȩ����ʹ��ˮ��ɫ�������ķ�Ӧ���Ͷ��Ǽӳɷ�Ӧ
B. ![]() ������������9��̼ԭ�Ӵ���ͬһƽ����
������������9��̼ԭ�Ӵ���ͬһƽ����
C. ����ʽΪC7H8O ������FeCl3������ɫ��Ӧ���л���ṹ��3��
D. ����������Ƿ������ȩ,������Ʒ�м�������NaOH��Һ���кͼ���,����������Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������X��Y��Z����Է���������ϵΪMr(X) < Mr(Y)= 0.5Mr(Z),����˵����ȷ����()
A.ԭ����Ŀ��ȵ���������,����������Z
B.��ͬ������,ͬ��������������,�����ܶ���С����X
C.��һ��������,�������������Ϊ2.24 L,�����ǵ����ʵ���һ����Ϊ0.1 mol
D.ͬ����,�����ͬ���������ֱ��2gY�����1gZ����,����ѹǿ��Ϊ2��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��Һ�д���ƽ�⣺Ca(OH)2(s)![]() Ca2��(aq)��2OH-(aq)����H<0�������йظ�ƽ����ϵ��˵����ȷ����
Ca2��(aq)��2OH-(aq)����H<0�������йظ�ƽ����ϵ��˵����ȷ����
�������¶ȣ�ƽ�������ƶ�
������Һ�м�������̼���Ʒ�ĩ����������ӵ�Ũ��
�۳�ȥ�Ȼ�����Һ�л��е����������ӣ���������Һ�м���������NaOH��Һ
�ܺ����£�����Һ�м���CaO����Һ��pH����
�ݸ���Һ���ȣ���Һ��pH����
������Һ�м���Na2CO3��Һ�����й�����������
������Һ�м�������NaOH���壬Ca(OH)2������������
A. �٢�B. �٢ޢ�C. �ڢۢܢ�D. �٢ڢޢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��NAΪ�����ӵ�������������������ȷ����
��106 g Na2CO3�����������������3NA
��25 �桢1.01��105 Pa����14 g���������ĵ�ԭ����ΪNA
�۱�״���£�22.4LCCl4�������ķ�����ԼΪ6.02��1023
�ܱ�״���£�aL�������͵����Ļ���ﺬ�еķ�����ԼΪ![]() ��6.02��1023
��6.02��1023
�ݳ��³�ѹ����92 g��NO2��N2O4������庬�е�ԭ����Ϊ6NA
A.�٢ڢ�B.�ڢܢ�C.�ۢܢ�D.�ܢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��25 ��ʱ����c(CH3COOH)��c(CH3COO)��0.1 mol��L1��һ����ᡢ�����ƻ����Һ����Һ��c(CH3COOH)��c(CH3COO)��pH�Ĺ�ϵ��ͼ��ʾ�������й���Һ������Ũ�ȹ�ϵ����������ȷ����
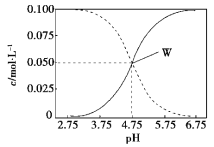
A. pH��5.5����Һ�У�c(CH3COO��)>c(CH3COOH)>c(H��)>c(OH)
B. pH��3.5����Һ�У�c(Na��)��c(H��)c(OH)��c(CH3COOH)��0.1 mol��L1
C. W������ʾ����Һ�У�c(Na��)��c(H��)��c(CH3COOH)��c(OH)
D. ��W������ʾ��1.0 L��Һ��ͨ��0.05 mol HCl����(��Һ����仯�ɺ���)��c(H��)��c(CH3COOH)��c(OH)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��T��ʱ����һ�̶��ݻ����ܱ������з�����Ӧ:A(g)+B(g)![]() C(s)��H<0�����ղ�ͬ��ȳ���A��B���ﵽƽ��ʱ������A��BŨ�ȱ仯��ͼ������(ʵ��)��ʾ�������ж���ȷ����
C(s)��H<0�����ղ�ͬ��ȳ���A��B���ﵽƽ��ʱ������A��BŨ�ȱ仯��ͼ������(ʵ��)��ʾ�������ж���ȷ����

A. T��ʱ���÷�Ӧ��ƽ�ⳣ��ֵΪ4
B. c��û�дﵽƽ�⣬��ʱ��Ӧ���������
C. ��c��Ϊƽ��㣬���ʱ�����ڵ��¶ȸ���T��
D. T��ʱ��ֱ��cd�ϵĵ��Ϊƽ��״̬
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������9�����ʣ����������ڶ�������ϡ�����������BaCl2���壻���������أ���KNO3��Һ����ƾ�(C2H5OH)���������ƣ��뽫�������ʰ�Ҫ������������⣺
��1������Ӧ��ѧʽ��д���пհף������������������_____________�����ڼ������������____________�����ڵ���ʵ���______�����ڷǵ���ʵ���_______�����������գ�
��2��д��NaHCO3���뷽��ʽ��______
��3����˫���ű�ʾCl2���������ķ�Ӧ________
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com