
在火箭推进器中装有强还原剂肼(N2H4)和强氧化剂(H2O2),当它们混合时,即产生大量的N2和水蒸气,并放出大量热。已知0.4mol液态肼和足量H2O2反应,生成氮气和水蒸气,放出256.65kJ的热量。
(1)写出该反应的热化学方程式__________________________________________。
(2)已知H2O(l)====H2O(g);△H=+44kJ·mol-1,则16 g液态肼燃烧生成氮气和液态水时,放出的热量是________kJ。
(3)上述反应应用于火箭推进剂,除释放大量的热和快速产生大量气体外,还有一个很突出的优点是________________________。
(4)已知 N2(g)+2O2(g)====2 NO2(g);△H=+67.7 kJ·mol-1,
N2H4 (g) +O2 (g) = N2(g) +2H2O (g) △H = -543kJ/mol
根据盖斯定律写出肼与NO2完全反应生成氮气和气态水的热化学方程式________________________________。
(5)已知: N2 (g) + 2O2 (g) = 2NO2 (g) △H = + 67.7kJ/mol
N2H4 (g) +O2 (g) = N2(g) +2H2O (g) △H = -543kJ/mol
1/2H2 (g) + 1/2F2 (g) = HF (g) △H = -269kJ/mol
H2 (g) + 1/2O2 (g) = H2O (g) △H = -242kJ/mol
有人认为若用氟代替二氧化氮作氧化剂,则反应释放能量更大,肼和氟反应的
热化学方程式: ________________________________。
(1)N2H4(l)+2 H2O2 (l) === N2(g)+ 4 H2O (g) △H= - 641.625 kJ·mol-1;(2)408.8 (3)生成N2和H2O,对环境无污染;(4)2N2H4(g)+2 NO2 (g) === 3N2(g)+4 H2O(g);△H= - 1153.7kJ·mol-1;(5)N2H4 (g) + F2 (g) = N2(g) +4HF (g) △H = -1135 kJ/mol
【解析】
试题分析:(1)已知0.4mol液态肼和足量双氧水反应生成氮气和水蒸气时放出256.65KJ的热量;肼和双氧水反应的热化学方程式:N2H4(l)+2H2O2(l)═N2(g)+4H2O(g);△H=-641.6KJ/mol,故答案为N2H4(l)+2H2O2(l)═N2(g)+4H2O(g);△H=-641.6KJ/mol;;(2)①N2H4(l)+2H2O2(l)═N2(g)+4H2O(g);△H=-641.6KJ/mol;②H2O(l)=H2O(g);△H=+44KJ/mol,①式-②式x4得出方程式N2H4(l)+2H2O2(l)═N2(g)+4H2O(g)△H=-817.6KJ/mol;故0.5mol肼放出的热量为408.8KJ,答案为408.8KJ;(3)还原剂肼(N2H4)和强氧化剂H2O2,当它们混合时,即产生大量的氮气和水蒸气,除释放大量热量和快速产生大量气体外,还有很突出的优点是,产物为氮气和水,无污染;故答案为:产物为氮气和水,无污染;;(4)2N2H4(g)+2 NO2 (g) === 3N2(g)+4 H2O(g)可由②x2-①得到,△H=2△H2-△H1=-1135 kJ/mol,故答案为2N2H4(g)+2 NO2 (g) === 3N2(g)+4 H2O(g);△H= - 1153.7kJ·mol-1;;(5)N2H4(g) + F2 (g) = N2(g) +4HF (g) △H = -1135 kJ/mol
考点:盖斯定律、热化学方程式书写


 芝麻开花课程新体验系列答案
芝麻开花课程新体验系列答案 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案科目:高中化学 来源:2014-2015学年吉林省高一入学摸底考试化学试卷(解析版) 题型:填空题
在10℃时,氯酸钾的溶解度为5g,在该温度下的氯酸钾的饱和溶液中溶质、溶剂、溶液的质量比为______________.
查看答案和解析>>
科目:高中化学 来源:2014-2015学年吉林延边州汪清六中上第一次月考高一化学试卷(解析版) 题型:选择题
对于危险化学品在包装标签上印有警示性标志.在运输乙醇的包装标签上应选用的标志是
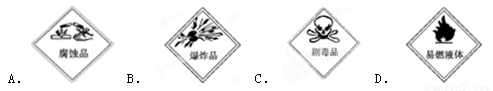
查看答案和解析>>
科目:高中化学 来源:2014-2015学年吉林公主岭市高一上学期第一次月考化学试卷(解析版) 题型:选择题
下列说法正确的是( )
A.摩尔是七个基本物理量之一
B.阿伏伽德罗常数是没有单位的
C.氮气的摩尔质量是28g
D.1molH2O约含有6.02×1023个水分子
查看答案和解析>>
科目:高中化学 来源:2014-2015学年吉林公主岭市高一上学期第一次月考化学试卷(解析版) 题型:选择题
下列实验操作均要用玻璃棒,其中玻璃棒的作用和目的相同的是( )
(1)过滤 (2)蒸发 (3)溶解 (4)向容量瓶转移液体
A.(1)和(2) B.(1)和(3) C.(3)和(4) D.(1)和(4)
查看答案和解析>>
科目:高中化学 来源:2014-2015学年北京市高二上第一次质量检测化学试卷(解析版) 题型:选择题
反应A(g)+3B(g) 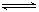 2C(g)+2D(g),在不同情况下测得反应速率,其中反应速率最快的是
2C(g)+2D(g),在不同情况下测得反应速率,其中反应速率最快的是
A.υ(D)=0.4 mol / ?L·s? B.υ(C)=0.5 mol / ?L·s?
C.υ(B)=0.6 mol / ?L·s? D.υ(A)=0.15 mol / ?L·s?
查看答案和解析>>
科目:高中化学 来源:2014-2015学年北京市高二上第一次质量检测化学试卷(解析版) 题型:选择题
完全燃烧一定质量的无水乙醇,放出的热量为Q,为完全吸收生成的CO2,并使之生成正盐Na2CO3,消耗掉0.8mol/L NaOH溶液500mL,则燃烧1mol酒精放出的热量是
A. 0.2Q B. 0.1Q
C. 5Q D. 10Q
查看答案和解析>>
科目:高中化学 来源:2014-2015学年北京市高一上第一次质量检测化学试卷(解析版) 题型:填空题
有一包白色粉末,含有Ba(NO3)2、CaCl2、K2CO3中的2种。为确定其成分,现做以下实验。结合资料卡片中的物质溶解性,试分析:
资料卡片:一些物质的溶解性
| OH- | CO | Cl- | NO |
Na+ | 溶 | 溶 | 溶 | 溶 |
Ca2+ | 微 | 不 | 溶 | 溶 |
Ba2+ | 溶 | 不 | 溶 | 溶 |
Mg2+ | 不 | 微 | 溶 | 溶 |
(1)将少量白色粉末加入足量水中,振荡,有白色沉淀生成。
通过上述现象可初步判断原白色粉末中一定含有的物质是 (填化学式)。
(2)过滤得到(1)中所产生的白色沉淀及滤液。
实验室中进行过滤操作时,通常需要下列玻璃仪器中的 (填序号)。
a. 玻璃棒 b. 普通漏斗 c. 烧杯 d. 容量瓶
(3)再继续向滤液中加入AgNO3溶液和过量稀硝酸,最终有白色沉淀生成。
第(3)步实验及现象说明,原白色粉末中一定还含有的物质是 (填化学式),若将(2)中的白色沉淀溶于稀硝酸时,发生反应的化学方程式是
。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年云南省玉溪市高二上学期期中考试化学试卷(解析版) 题型:选择题
相同体积、相同pH的某一元强酸溶液①和某一元弱酸溶液②分别与足量的锌粉发生反应,下列关于氢气体积(V)随时间(t)变化的示意图正确的是
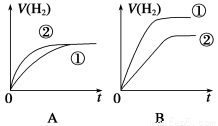
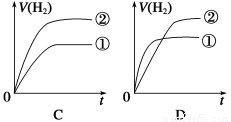
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com