
【题目】将4g氢氧化钠和mg碳酸钠混合并配成溶液,向溶液中滴加一定浓度的稀盐酸,加入盐酸的体积和生成二氧化碳的质量的关系如图所示,回答下列问题:(不考虑二氧化碳的溶解)
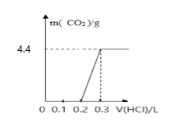
(1)加入盐酸的体积为0.2L时,溶液中溶质的成分为___;
(2)碳酸钠的质量m=___;
(3)盐酸的物质的量浓度为___。
【答案】NaHCO3、NaCl 10.6g 1mol/L
【解析】
向氢氧化钠和碳酸钠的混合溶液中滴加一定浓度的稀盐酸,发生反应的顺序及化学方程式为:①NaOH+HCl=NaCl+H2O ②Na2CO3+HCl=NaHCO3+NaCl ③NaHCO3+ HCl= NaCl +H2O+CO2↑,由反应②③可以看出,盐酸和碳酸钠溶液反应分两步进行,并且这两步消耗的盐酸是等量的。图中混合液完全反应消耗的盐酸为0.3L,加入盐酸体积0~0.1发生反应①,0.1~0.2发生反应②,0.2~0.3发生反应③,再结合图中给出的相关量可以计算碳酸钠的质量和盐酸的物质的量浓度。
(1)加入盐酸的体积为0.2L时,发生的反应是NaOH+HCl=NaCl+H2O和Na2CO3+HCl=NaHCO3+NaCl,此时溶液中的溶质为NaHCO3和NaCl 。
答案为:NaHCO3、NaCl;
(2)图中盐酸体积0.1~0.3时,是盐酸和碳酸钠反应生成二氧化碳的过程,根据关系式:Na2CO3 ~ CO2可以算出,生成4.4g CO2时,对应Na2CO3的质量为10.6g。
答案为:10.6g;
(3)图中盐酸体积0~0.1L时,发生反应为:NaOH+HCl=NaCl+H2O,氢氧化钠质量是4g,物质的量是0.1mol,则盐酸的物质的量也为0.1mol,由公式C=n/V,可以求出盐酸的物质的量浓度为1mol/L。
答案为:1mol/L。


科目:高中化学 来源: 题型:
【题目】用50mL0.50mol·L-1的盐酸与50mL0.55mol·L-1的氢氧化钠溶液在如图所示的装置中进行中和反应,通过测定反应过程中所放出的热量可计算中和热。回答下列问题。

(1)仪器A的名称是_____。
(2)A的材质不能用铁质的代替,其原因是:_____。
(3)实验时氢氧化钠溶液的浓度要用0.55mol·L-1的原因是:____。实验中若改用60mL0.5mol·L-1的盐酸与50mL0.55mol·L-1的氢氧化钠溶液进行反应,与上述实验相比,所放出的热量____(填“相等”或“不相等”),若实验操作均正确,则所求中和热___(填“相等”或“不相等”);
(4)已知在稀溶液中,强酸和强碱发生中和反应生成1molH2O时,放出57.3kJ的热量,则上述反应的热化学方程式为:_____。
(5)若用KOH代替NaOH,对测定结果____(填“有”或“无”)影响;若用醋酸代替HCl做实验,对测定结果_____(填“有”或“无”)影响。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从某废催化剂(含ZnO、CuO、Fe2O3、石墨及MnO2等)中回收金属并制取活性氧化锌的工艺流程如图(已知:Zn及其氧化物、氢氧化物的性质与Al及其相应化合物性质类似):

(1)“氧化”时Mn2+被氧化的离子方程式为___________________________________。
(2)“中和、沉淀”时,若pH过高,则碱式碳酸锌的产率偏小。写出其反应的离子方程式(任写一个即可):_________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各离子①H+ ②Cl- ③Al3+ ④K+ ⑤S2- ⑥OH- ⑦NO3- ⑧NH4+中,不影响水的电离平衡的是( )
A.①③⑤⑦⑧B.②④⑦C.①⑥D.②④⑥⑧
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】羰基硫(COS)可作为一种粮食熏蒸剂,能防止某些昆虫、线虫和真菌的危害。在恒容密闭容器中,将CO和H2S混合加热并达到下列平衡:
CO(g)+H2S(g)![]() COS(g)+H2(g) K=0.1
COS(g)+H2(g) K=0.1
反应前CO物质的量为10mol,平衡后CO物质的量为8mol。下列说法正确的是
A. 升高温度,H2S浓度增加,表明该反应是吸热反应
B. 通入CO后,正反应速率逐渐增大
C. 反应前H2S物质的量为7mol
D. CO的平衡转化率为80%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】相同温度、相同浓度的六种溶液,其pH由小到大的顺序如图所示,图中①②③代表的物质可能分别是
![]()
A.NH4Cl (NH4)2SO4 CH3COONa
B.(NH4)2SO4 NH4Cl CH3COONa
C.(NH4)2SO4 NH4Cl NaOH
D.CH3COOH NH4Cl (NH4)2SO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积固定为2L的密闭容器中,充入![]() 和
和![]() ,在温度
,在温度![]() 时发生反应,
时发生反应,![]() ,
,![]() 的浓度随时间变化如图,下列说法正确的是
的浓度随时间变化如图,下列说法正确的是![]()
![]()
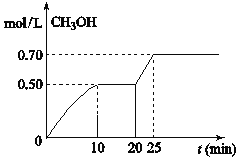
A.从开始到25分钟,![]() 的转化率是
的转化率是![]()
B.从20分钟到25分钟,可能是缩小容器体积
C.其它条件不变,将温度升到![]() ,平衡常数增大
,平衡常数增大
D.从反应开始到10分钟,![]() 的平均反应速率
的平均反应速率![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】a~n10中元素在周期表中的位置如图所示,请回答下列问题:
a | ||||||||
b | c | d | e | |||||
f | g | h | m | n | ||||
…… |
(1)m的阴离子的结构示意图为___。
(2)b的最高价氧化物的化学式为___;用化学方程式表示f、d的单质形成f2d2的过程___。
(3)d、g、n形成的简单离子的半径由大到小的顺序为___(用离子符号表示)。
(4)以上元素组成的物质有下列框图中的转化关系,其中甲为10电子微粒。
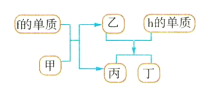
请写出h的单质与乙反应的化学方程式:___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】油脂是重要的营养物质.某天然油脂A可发生下列反应:

已知:A的分子式为C57H106O6.1mol该天然油脂A经反应①可得到1molD、1mol不饱和脂肪酸B和2mol直链饱和脂肪酸C.经测定B的相对分子质量为280,原子个数比为C:H:O=9:16:1;
(1)写出B的分子式:________________________;
(2)写出反应①的反应类型:____________;C的名称(或俗称)是_________;
(3)近日,电视媒体关于“氢化油危害堪比杀虫剂”的报道引发轩然大波,反应②为天然油脂的氢化过程.下列有关说法不正确的是_______________;
a.氢化油又称人造奶油,通常又叫硬化油.
b.植物油经过氢化处理后会产生副产品反式脂肪酸甘油酯,摄入过多的氢化油,容易堵塞血管而导致心脑血管疾病.
c.氢化油的制备原理是在加热植物油时,加入金属催化剂,通入氢气,使液态油脂变为半固态或固态油脂.
d.油脂的氢化与油脂的皂化都属于加成反应
(4)D和足量金属钠反应的化学方程式_____________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com