
【题目】在一定条件下,向饱和的氢氧化钠溶液中加入少量的过氧化钠,充分反应后,恢复原来的温度,下列说法正确的是
A. 溶液中![]() 浓度增大,有
浓度增大,有![]() 放出 B. 溶液pH不变,有固体析出,有
放出 B. 溶液pH不变,有固体析出,有![]() 放出
放出
C. 溶液中![]() 数目增多,有
数目增多,有![]() 放出 D. 溶液中
放出 D. 溶液中![]() 数目不变,有
数目不变,有![]() 放出
放出
科目:高中化学 来源: 题型:
【题目】下表各组物质分类不正确的是( )
选项 | A | B | C | D |
物质 | 液氧、空气、Cl2、铜丝 | HCl、H2SO4、H2O、HNO3 | NaCl溶液、盐酸、CuSO4·5H2O | NH3、NaOH、BaSO4固体 |
分类标准 | 单质 | 酸 | 混合物 | 电解质 |
不属于该 类的物质 | 空气 | H2O | 盐酸 | NH3 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质的名称不正确的是( )
A.FeS2:二硫化亚铁B.CaSO4·2H2O:熟石膏
C.CO(NH2)2:尿素D.CH3CH2CH2CH3:正丁烷
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素 Q、R、T、W 在元素周期表中的位置如图所示,其中T 所处的周期序数与主族序数相等,请回答下列问题:
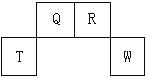
(1)W 在周期表中的位置是____________, Q、R、T 三种元素原子的半径从大 到小排列顺序_____________ (用元素符号表示),Q 的最高价氧化物的电子 式________________,R 气态氢化物分子的结构式为_______________。
(2)元素的原子得电子能力:Q________________W(填“强于”或“弱于”)。
(3)T、Q、R、W 的单质中,固态时属于原子晶体的是______________(填名称)。
(4)现有 8 种元素的性质、数据如下表所列,它们属于短周期:请指出 R 元素在下表中的对应编 号__________________ ,与 T 同周期且最高价氧化物的水化物碱性最强的元素在下表中的对应编 号_____________。
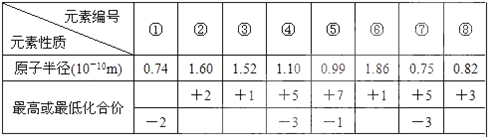
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把500 mL NH4HCO3和Na2CO3的混合溶液分成五等份,取一份加入含a mol氢氧化钠的溶液恰好反应完全,另取一份加入含b mol HCl的盐酸恰好反应完全,则该混合溶液中c(Na+)为( )
A. (![]() -
-![]() ) mol/L B. (2b-a) mol/L
) mol/L B. (2b-a) mol/L
C. (5b-![]() ) mol/L D. (10b-5a) mol/L
) mol/L D. (10b-5a) mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列有关叙述正确的是( )
A.0.1 molL﹣1醋酸溶液加水稀释后,各离子浓度均减小
B.pH=7的NH4Cl和氨水混合溶液中,c(NH4+)=c(Cl﹣)
C.加热滴有酚酞的CH3COONa溶液,溶液颜色变浅
D.0.1 molL﹣1 Na2CO3溶液中,c(HCO﹣3)>c(OH﹣)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】重要的化学品M和N的合成路线如图所示: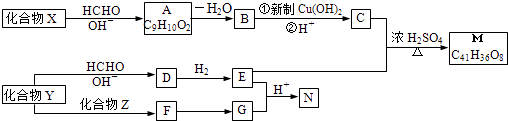
已知:i. ![]()
ii. ![]()
iiiN的结构简式是: 
请回答下列问题:
(1)A中含氧官能团名称是 , C 与E生成M的反应类型是 .
(2)写出下列物质的结构简式:X:Z:E:
(3)C和甲醇反应的产物可以发生聚合反应.该聚合反应的产物是: .
(4)1molG一定条件下,最多能与mol H2发生反应
(5)写出一种符合下列要求G的同分异构体①有碳碳叄键 ②能发生银镜反应 ③一氯取代物只有2种
(6)1,3﹣丙二醇是重要的化工物质,请设计由乙醇合成它的流程图合成路线流程图示例如下:CH2=CH2 ![]() CH3CH2Br
CH3CH2Br ![]() CH3CH2OH.
CH3CH2OH.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素X,Y,Z,W在元素周期表中相对位置如图所示其中Y所处的周期序数与族序数相等.按要求回答下列问题:
X | ||||
Y | Z | W |
(1)写出X的原子结构示意图 .
(2)列举一个事实说明X非金属性强于Z:(用化学方程式表示)
(3)含Y的氯化物呈酸性的原因是(用离子方程式表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现用98%浓硫酸(密度1.84g/cm3)配制浓度为0.5mol/L稀硫酸500mL.
(1)选用的主要仪器有:、、、、;
(2)请将下列操作按照正确的序号填在横线上
A、用量筒量取浓硫酸B、反复颠倒摇匀C、用胶体滴管加水至刻度D、洗净烧杯内壁和玻璃棒,并将洗液转至容量瓶E、稀释浓硫酸F、将溶液转入容量瓶
(3)所需浓硫酸的体积为mL.
(4)将浓硫酸沿着烧杯内壁慢慢注入盛水的烧杯中,不断搅拌的目的是;若搅拌过程中有液体溅出,会使最终结果.(填偏高、偏低或无影响)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com