
【题目】下列各选项中,可用右侧示意图表示的是
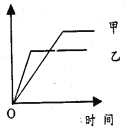
反应 | 纵坐标 | 甲 | 乙 | |
A | 相同质量氨,在同一容器中:2NH3 | 氨气的转化率 | 500℃ | 400℃ |
B | 等质量的钾、钠分别与水反应 | H2的质量 | 钠 | 钾 |
C | 体积比为1︰3的N2、H2,在体积可变的恒压容器中: N2+3H2 | 氨气的浓度 | 活性高的催化剂 | 活性一般的催化剂 |
D | 2mol SO2与1mol O2,在相同温度下:2SO2+O2 | SO3的物质的量 | 10 MPa | 20 MPa |
A. A B. B C. C D. D
 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案 暑假作业北京艺术与科学电子出版社系列答案
暑假作业北京艺术与科学电子出版社系列答案 第三学期赢在暑假系列答案
第三学期赢在暑假系列答案科目:高中化学 来源: 题型:
【题目】根据所学知识完成问题:
(1)尿素在农业生产中起重要作用,其合成过程分两步进行:
2NH3(g)+CO2 (g)NH2COONH4(l)△H=﹣117kJmol﹣1
NH2COONH4(l)(NH2)2CO(g)+H2O(g)△H=+15kJmol﹣1
①由氨气和二氧化碳合成尿素的热化学方程式是:
②第一步反应在11.1Mpa、160°C的条件下反应较快,转化率也较高,第二步反应在相同条件下反应速率较慢,转化率也较低.因此,总反应的反应速率和转化率主要取决于 . (填“第一步”或“第二步”)
③对于第一步反应,能判断该反应一定达到化学平衡状态的依据是(填选项编号).
A.容器中气体的平均相对分子质量不随时间而变化
B.υ正(NH3)=2υ逆(CO2)
C.容器中气体的密度不随时间而变化
D.容器中总质量不随时间而变化
(2)工业上合成氨气的反应为:N2(g)+3H2(g)2NH3(g)△H<0.现将10mol N2和26molH2置于容积可变的密闭容器中,N2的平衡转化率(α)与体系总压强(P)、温度(T)的关系如图所示.
回答下列问题:
①反应达到平衡状态B时,容器的容积10L,则T1时,合成氨反应的平衡常数K= .
②平衡状态由A变到C时,对应的平衡常数K(A)K(C)(填“>”、“<”或“=”).
③平衡状态由A变到B时,对应的平衡常数K(A)K(B)(填“>”、“<”或“=”).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在相同温度下,有相同体积的甲、乙两容器,甲容器中充入1g N2和1g H2,乙容器中充入2g N2和2g H2。下列叙述中错误的是
A. 化学反应速率:乙>甲 B. 平衡混合气中H2的体积分数:乙>甲
C. H2的转化率:乙>甲 D. 平衡后N2的浓度:乙>甲
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】标准状况下VL氨气溶解在1L水中(水的密度近似为1g/ml),所得溶液的密度为ρ g/ml,质量分数为w,物质浓度为cmol/L,则下列关系中不正确的是( )
A.ρ= ![]()
B.W= ![]()
C.W= ![]()
D.C= ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】无机化合物可根据其组成和性质进行分类: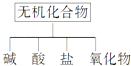
(1)如图所示的物质分类方法名称是 .
(2)以Na、K、H、O、C、S中任意两种或三种元素组成合适的物质,分别填在表②③⑥的后面.
物质类别 | 酸 | 碱 | 盐 | 氧化物 |
化学式 | ①HCl | ③ | ⑤Na2CO3 | ⑦CO2 |
(3)写出⑦转化为⑤的离子方程式: .
(4)实验室制备⑦常用和反应(写物质的化学式),检验该气体的方法是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在某无色溶液中缓慢地滴入NaOH溶液直至过量,产生沉淀的质量与加入NaOH溶液体积的关系如图所示,由此确定,原溶液中含有的离子可能是( ) 
A.Mg2+、Al3+、Fe3+
B.H+、Mg2+、Al3+
C.H+、Ba2+、Al3+
D.Na+、Mg2+、Al3+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【加试题】ClO2是一种优良的消毒剂,浓度过高时易发生分解,常将其制成NaClO2固体,以便运输和贮存。过氧化氢法制备NaClO2固体的实验装置如图1所示。
已知:2NaClO3+H2O2+H2SO4===2ClO2↑+O2↑+Na2SO4+2H2O
2ClO2+H2O2+2NaOH===2NaClO2+O2↑+2H2O
ClO2熔点-59℃、沸点11℃;H2O2沸点150℃
请回答:
(1)仪器A的作用是;冰水浴冷却的目的是(写两种)。
(2)空气流速过快或过慢,均降低NaClO2产率,试解释其原因。
(3)Clˉ存在时会催化ClO2的生成。反应开始时在三颈烧瓶中加入少量盐酸,ClO2的生成速率大大提高,并产生微量氯气。该过程可能经两步反应完成,将其补充完整:①(用离子方程式表示),②H2O2+Cl2===2Clˉ+O2+2H+。
(4)H2O2浓度对反应速率有影响。通过图2所示装置将少量30% H2O2溶液浓缩至40%,B处应增加一个设备。该设备的作用是 , 馏出物是。
(5)抽滤法分离NaClO2过程中,下列操作不正确的是( )
A.为防止滤纸被腐蚀,用玻璃纤维代替滤纸进行抽滤
B.先转移溶液至漏斗,待溶液快流尽时再转移沉淀
C.洗涤沉淀时,应使洗涤剂快速通过沉淀
D.抽滤完毕,断开水泵与吸滤瓶间的橡皮管后,关闭水龙头
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积为1.00L的容器中,通入一定量的N2O4,发生反应N2O4(g) ![]() 2NO2(g),随温度升高,混合气体的颜色变深。
2NO2(g),随温度升高,混合气体的颜色变深。
(1)反应的ΔH________0(填“大于”或“小于”);100 ℃时,体系中各物质浓度随时间变化如图所示。在0~60 s时段,反应速率v(N2O4)为________mol·L-1·s-1;反应的平衡常数K1为_____________。

(2)100 ℃时达到平衡后,改变反应温度为T,c(N2O4)以0.0020 mol·L-1·s-1的平均速率降低,经10 s又达到平衡。T______100 ℃(填“大于”或“小于”),判断理由是____________________________________________。
(3)温度T时反应达平衡后,将反应容器的容积减少一半,平衡向________(填“正反应”或“逆反应”)方向移动,判断理由是____________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com