
【题目】在某无色溶液中缓慢地滴入NaOH溶液直至过量,产生沉淀的质量与加入NaOH溶液体积的关系如图所示,由此确定,原溶液中含有的离子可能是( ) 
A.Mg2+、Al3+、Fe3+
B.H+、Mg2+、Al3+
C.H+、Ba2+、Al3+
D.Na+、Mg2+、Al3+
 53随堂测系列答案
53随堂测系列答案科目:高中化学 来源: 题型:
【题目】等物质的量的下列各电解质处于以下状态时:①熔融的NaHSO4 ②NaHSO4水溶液 ③NaHCO3水溶液 ④H2CO3溶液,自由移动的离子数目由大到小的排列顺序正确的是
A. ②③①④ B. ④②③① C. ①②③④ D. ②①③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】自然界中的许多植物中含有醛,其中有些具有特殊香味,可作为植物香料使用,例如桂皮含肉桂醛( ![]() ),杏仁含苯甲醛(
),杏仁含苯甲醛( ![]() )。下列说法错误的是( )
)。下列说法错误的是( )
A.肉桂醛能发生加成反应、取代反应和加聚反应
B.可用新制氢氧化铜悬浊液检验肉桂醛分子中的含氧官能团
C.肉桂醛和苯甲醛互为同系物
D.苯甲醛分子中所有原子可能位于同一平面内
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用如图所示装置进行下列实验,将X溶液逐滴加入固体Y中,下列关于试管中的现象描述不正确的是( )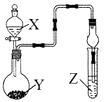
选项 | X溶液 | 固体Y | Z溶液 | 现象 |
A | 稀硫酸 | Na2O2 | 氢硫酸 | 产生淡黄色沉淀 |
B | 浓氨水 | 碱石灰 | 氯化铝溶液 | 产生白色沉淀 |
C | 浓硝酸 | Cu | 硅酸钠溶液 | 产生白色沉淀 |
D | 稀盐酸 | CaCO3 | 氯化钡溶液 | 产生白色沉淀 |
A.A
B.B
C.C
D.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各选项中,可用右侧示意图表示的是
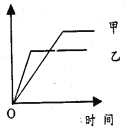
反应 | 纵坐标 | 甲 | 乙 | |
A | 相同质量氨,在同一容器中:2NH3 | 氨气的转化率 | 500℃ | 400℃ |
B | 等质量的钾、钠分别与水反应 | H2的质量 | 钠 | 钾 |
C | 体积比为1︰3的N2、H2,在体积可变的恒压容器中: N2+3H2 | 氨气的浓度 | 活性高的催化剂 | 活性一般的催化剂 |
D | 2mol SO2与1mol O2,在相同温度下:2SO2+O2 | SO3的物质的量 | 10 MPa | 20 MPa |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某一反应体系有反应物和生成物共五种物质:O2、H2CrO4、Cr(OH)3、H2O、H2O2已知该反应中H2O2只发生如下过程:H2O2→O2
(1)该反应中的还原剂是 .
(2)该反应中,发生还原反应的过程是→ .
(3)写出该反应的化学方程式,并标出电子转移的方向和数目 .
(4)如反应转移了0.3mol电子,则产生的气体在标准状况下体积为 .
(5)已知下列分子或离子在酸性条件下都能氧化KI,自身发生如下变化: H2O2→H2O IO ![]() →I2 MnO
→I2 MnO ![]() →Mn2+ HNO2→NO
→Mn2+ HNO2→NO
如果分别用等物质的量的这些物质氧化足量的KI,得到I2最多的是
A.H2O2
B.IO ![]()
C.MnO ![]()
D.HNO2 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[化学——选修3:物质结构与性质]
“摩尔盐”是分析化学中的重要试剂,化学式为(NH4)2Fe(SO4)2·6H2O。“摩尔盐”在一定条件下分解的方程式为:4[(NH4)2Fe(SO4)2·6H2O] ![]() 2Fe2O3+3SO3+5SO2↑+N2↑+6NH3↑+31H2O。回答下列问题:
2Fe2O3+3SO3+5SO2↑+N2↑+6NH3↑+31H2O。回答下列问题:
(1)铁元素在元素周期表中的位置为 , 其价层电子排布图为。
(2)组成“摩尔盐”的非金属元素中第一电离能最大的元素为。“摩尔盐”的分解产物中属于非极性分子的化合物是。
(3)NH3的沸点比N2O的沸点(填“高”或“低”),其主要原因是。
(4)K3[Fe(CN)6]常用于检验Fe2+ , K3[Fe(CN)6]中除了离子键以外还存在的化学键为 , 与CN—互为等电子体的单质的分子式为_。HCN分子中σ键和π键的个数之比为。
(5)FeO晶胞结构如下图所示,FeO晶体中Fe2+配位数为 , 若该晶胞边长为acm,则该晶胞密度为。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】聚芳酯(PAR)是分子主链上带有苯环和酯基的特种工程塑料,在航空航天等领域应用广泛.下图是利用乙酰丙酸(α)合成聚芳酯E的路线(省略部分产物): 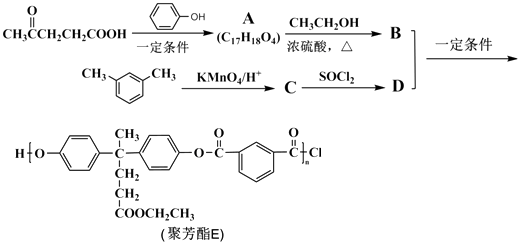
已知: ![]() +R′OH→
+R′OH→ ![]() +HCl
+HCl![]()
(R、R′表示烃基)
(1)A中含有的官能团是(填官能团名称).
(2)B与D的反应类型为 , B的结构简式为 .
(3)C生成D的反应化学方程式为 .
(4)C分子的核磁共振氢谱中有个吸收峰;同时符合下列要求的C的同分异构体有种.①能发生银镜反应 ②能与NaHCO3溶液反应 ③遇FeCl3溶液显紫色, F与C属于官能团异构的同分异构体,且只含一种官能团,则1mol F与足量NaOH溶液反应时消耗NaOH的物质的量为 .
(5)根据合成聚芳酯E的路线,请你以苯酚及2﹣丙醇为原料(无机试剂任选),设计合成G: ![]() 的路线. .
的路线. .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚氯酸钠(NaClO2)一种高效氯化剂、漂白剂,在NaOH溶液中ClO2与H2O2反应可以得到亚氯酸钠.
(1)ClO2中氯元素的化合价是;在制备亚氯酸钠的反应中ClO2做(填“氧化剂”或“还原剂”);若反应中生成1molNaClO2 , 转移电子物质的量为mol;
(2)写出该反应的化学方程式为;
(3)科学家经研究发现NaClO2也可用于制取自来水消毒剂ClO2 . 2NaClO2+Cl2═2ClO2+2NaCl,还原产物为 , 用单线桥法标出电子转移的方向和数目 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com