
【题目】下列有关说法不正确的是
A. C3H8中碳原子都采用的是sp3杂化
B. O2、CO2、N2都是非极性分子
C. 酸性:H2CO3<H3PO4<H2SO4<HClO
D. CO的一种等电子体为NO+,它的电子式为![]()
科目:高中化学 来源: 题型:
【题目】某同学按下图进行实验,在A中放的是干燥的红色纸条,B中放的是湿润的红色纸条,C中盛放的是氢氧化钠溶液。请回答下列问题。
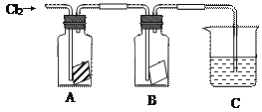
(1)通入Cl2一段时间后,A、B装置中,红色纸条的现象和结论为:
装置 | 现象 | 结论 |
A | ______________ | 潮湿的氯气______(填能或不能)使红色纸条褪色,因为反应生成的____________具有漂白性 |
B | ______________ |
(2)C装置的作用是__________________________
写出装置C中反应的化学方程式:_________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列表示对应化学反应的离子方程式正确的是 ( )
A. 向稀HNO3中滴加Na2SO3溶液: SO32-+2H+SO2↑+H2O
B. Na2CO3溶液中CO32-的水解:CO32-+H2O==HCO3-+OH-
C. 向Al2(SO4)3溶液中加入过量的NH3·H2O: Al3++4NH3·H2O[Al(OH)4]-+4N![]()
D. 向CuSO4溶液中加Na2O2:2Na2O2+2Cu2++2H2O4Na++2Cu(OH)2↓+O2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列措施对增大反应速率明显有效的是( )
A.Al在氧气中燃烧生成Al2O3 , 将Al粉改为Al片
B.Fe与稀盐酸反应制取H2时,改用氢离子浓度相同的稀硫酸
C.Zn与稀硫酸反应时,适当提高溶液的温度
D.Na与水反应时增大水的用量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】热化学方程式2H2(气) + O2(气) = 2H2O(气) + 483.6 kJ/mol ,化学计量(系数)表示的是
A. 体积数 B. 物质和质量 C. 物质的量 D. 物质的质量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钢制构件在镀锌前需要经过酸洗,其基本原理是用盐酸除去其表面的Fe2O3·H2O及FeO等杂质。回收废酸同时生产含铁产品的流程如下:

已知:
i.酸洗钢制构件后得到废酸的主要成分如下表所示。

ii.pH <4时,Fe2+不易被氧气氧化。
(1)用离子方程式解释废酸中不含Fe3+的原因______________________________。
(2)过程II中,发生的主要反应:FeCl2(s)十H2SO4(aq) ![]() FeSO4(s)+2HCl( aq)。
FeSO4(s)+2HCl( aq)。
①加入过量H2SO4的作用是__________________________________(写出一点即可)。
②用化学平衡原理解释鼓入空气的目的:_________________________________。
(3)过程III中,FeSO4隔绝空气焙烧得到的尾气中含有两种可用于生产硫酸的氧化物,此过程发生反应的化学方程式是_________________________________________。
(4)过程V:阴离子交换树脂可将FeCl4-选择性吸附分离,其过程可表示为ROH +X-![]() RX +OH-(X-表示FeCl4-)。当树脂吸附饱和后可直接用水洗涤树脂进行脱附,同时脱附过程发生反应:FeCl4-
RX +OH-(X-表示FeCl4-)。当树脂吸附饱和后可直接用水洗涤树脂进行脱附,同时脱附过程发生反应:FeCl4-![]() Fe3+ +4C1-。
Fe3+ +4C1-。
①吸附后溶液的pH将会_______________。(填“升高”、“降低”或“不变”)
②洗脱液经处理后有许多用途,下列用途合理的是_________________。
A、刻蚀印刷铜线路板 B、净化污水 C、自来水消毒 D、浸泡生物标本
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有下列反应:
①2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O
②CaO+H2O=Ca(OH)2
③Ba(OH)2+H2SO4=BaSO4↓+2H2O
④Zn+2HCl=ZnCl2+H2↑
⑤2KClO3![]() 2KCl+3O2↑
2KCl+3O2↑
⑥CaCO3![]() CaO+CO2↑
CaO+CO2↑
⑦2CO+O2![]() 2CO2
2CO2
⑧SO42-+Ba2+=BaSO4↓
(1)既是分解反应又是氧化还原反应的是_____,既是化合反应又是氧化还原反应的是______(均填序号)。
(2)请用单向桥表示反应①的电子转移的方向和数目:________________。其中,该反应的氧化产物是___________,还原产物是__________。
(3)反应③的离子反应方程式为_________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由CH3CH2CH2Br制备CH3CH(OH)CH2OH,依次发生的反应类型和反应条件都正确的是
选项 | 反应类型 | 反应条件 |
A | 加成、取代、消去 | KOH醇溶液/加热、KOH水溶液/加热、常温 |
B | 消去、加成、取代 | NaOH醇溶液/加热、常温、KOH水溶液/加热 |
C | 氧化、取代、消去 | 加热、KOH醇溶液/加热、KOH水溶液/加热 |
D | 消去、加成、水解 | NaOH水溶液/加热、常温、NaOH醇溶液/加热 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)在臭氧发生器中装入100mLO2,经反应3O2=2 O3,最后气体体积变为95mL(体积均为标准状况下测定),则反应后混合气体的密度为____________。
(2)将溶质质量分数为a%NaOH溶液蒸发掉m g水后,变成VmL 2a%的NaOH不饱和溶液,则蒸发后的溶液的物质的量浓度是__________。
(3)amolH2SO4中含有b个氧原子,则阿伏加德罗常数可以表示为_______。
(4)现有CO、CO2、O3(臭氧)三种气体,它们分别都含有1mol氧原子,则三种气体的质量之比为________(最简整数比)。
(5)标准状况下,密度为0.75g/L 的NH3与CH4组成的混合气体中,NH3的体积分数为__________,该混合气体对氢气的相对密度为_____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com