
【题目】如图所示物质的转化关系中,A是一种固体单质,E是一种白色沉淀.请回答下列问题: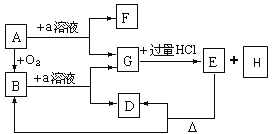
(1)B的化学式是___ , 目前B已被用作___的主要原料.
(2)B和a溶液反应的离子方程式是___ .
(3)A和a溶液反应的离子方程式是___ .
(4)C和过量的盐酸反应的离子方程式是___ .
【答案】 SiO2 光导纤维 SiO2+2OH﹣═SiO32﹣+H2O Si+2OH﹣+H2O═SiO32﹣+2H2↑ SiO32﹣+2H+═H2SiO3↓
【解析】G和过量的盐酸反应产生不溶于盐酸的白色沉淀,可知E可能为是硅酸,A可能是硅,带入题目进行验证,a溶液是强碱溶液或氢氟酸溶液,而硅和二氧化硅与氢氧化钠溶液反应均生成硅酸钠溶液,硅酸钠溶液与过量的盐酸反应产生氯化钠和硅酸白色沉淀;硅酸加热分解为二氧化硅和水,与题意相符,硅、二氧化硅与氢氟酸反应均生成四氟化硅,四氟化硅与盐酸不反应,与题意矛盾;因此A是Si、B是SiO2、C是 Na2SiO3 或K2SiO3 、 D是H2O、E是 H2SiO3 、F是H2、 a是NaOH或KOH。
(1)B的化学式是SiO2, 目前SiO2已被用作光导纤维的主要原料;正确答案:SiO2 、光导纤维。
(2)SiO2与强碱溶液反应生成可溶性的硅酸盐和水,离子方程式是SiO2+2OH﹣═SiO32﹣+H2O;正确答案:SiO2+2OH﹣═SiO32﹣+H2O。
(3)Si和强碱溶液反应生成可溶性硅盐酸和氢气,离子方程式是Si+2OH﹣+H2O═SiO32﹣+2H2↑;正确答案:Si+2OH﹣+H2O═SiO32﹣+2H2↑。
(4)硅酸盐与过量的盐酸反应生成白色沉淀硅酸,离子方程式是SiO32﹣+2H+═H2SiO3↓;
正确答案:SiO32﹣+2H+═H2SiO3↓。


科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A.1mol H2约含有6.02×1023个微粒
B.水的摩尔质量是18g
C.氯化氢的摩尔质量就是它的相对分子质量
D.相同物质的量的SO2和SO3,含氧原子个数之比为2:3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】若pH=3的酸溶液和pH=11的碱溶液等体积混合后溶液呈酸性,其原因是( )
A.生成一种强酸弱碱盐
B.弱酸溶液和强碱溶液
C.弱酸与弱碱溶液反应
D.一元强酸溶液与一元强碱溶液反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物M 的结构简式如下:下列有关M 叙述不正确的是( )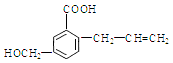
A.M的分子式为C11H12O3
B.能使溴的四氯化碳溶液褪色
C.一定条件下,M能生成高分子化合物
D.能发生加成反应不能发生取代反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为实验室制取少量乙酸乙酯的装置图。下列关于该实验的叙述中不正确的是( )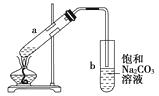
A.向a试管中先加入浓硫酸,然后边摇动试管边慢慢加入乙醇,再加冰醋酸
B.试管b中导气管下端管口不能浸入液面的原因是防止实验过程中发生倒吸现象
C.实验时加热试管a的目的是及时将乙酸乙酯蒸出并加快反应速率
D.试管b中饱和Na2CO3溶液的作用是吸收随乙酸乙酯蒸出的少量乙酸和乙醇
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式书写正确的是
A. Cl2通入水中:Cl+H2O![]() 2H++Cl-+ClO-
2H++Cl-+ClO-
B. 铝粉投入到NaOH溶液中:2Al+2OH-=2AlO2-+H2↑
C. NaHCO3溶液跟足量的Ca(OH)2反应:HCO3-+Ca2++OH-=CaCO3↓+H2O
D. H2SO4溶液中加入足量的Ba(OH)2溶液:SO42-+H++Ba2++OH-=BaSO4↓+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)在标准状况下,将充满NO2的试管倒扣到盛水的水槽中,一段时间后,试管内气体的体积是试管体积的________________,假设试管内溶质不扩散,则试管内溶液中溶质的物质的量浓度为___________________。
(2)某铁的“氧化物”样品,用5mol/L的盐酸100mL恰好完全溶解,所得溶液还能吸收标准状况下1.12L氯气,使其中Fe2+恰好全部转化为Fe3+,发生反应的离子方程式为_________,该样品中Fe和O的个数比为_______________。
(3)向盛有10mL1mol/LNH4Al(SO4)2溶液的烧杯中滴加1mol/LNaOH溶液,沉淀物质的量随NaOH溶液体积变化示意图如下:(已知NH4++OH-=NH3·H2O)
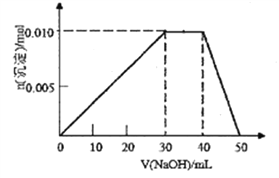
①写出滴加NaOH溶液40~50mL时反应的离子方程式:__________________。
②若10mL1mol/LNH4Al(SO4)2溶液中改加20mL1.15mol/LBa(OH)2溶液,充分反应后,溶液中产生沉淀的物质的量为_________________mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】弱电解质的电离平衡、盐类的水解平衡和难溶物的溶液平衡均属于化学平衡. I、已知H2A在水中存在以下平衡:H2AH++HA﹣ , HA﹣H++A2﹣ .
(1)NaHA溶液的pH(填大于、小于或等于) Na2A溶液的pH.
(2)某温度下,若向0.1mol/L的NaHA溶液中逐滴滴加0.1mol/L KOH溶液至溶液呈中性.此时该混合溶液中下列关系中,一定正确的是 . a.c(H+)c(OH﹣)=1×10﹣14 b.c(Na+)+c(K+)=c(HA﹣)+2c(A2﹣)
c.c(Na+)>c(K+) d.c(Na+)+c(K+)=0.05mol/L
(3)已知常温下H2A的钙盐(CaA)饱和溶液中存在以下平衡:CaA(s)Ca2+(aq)+A2﹣(aq)△H>0. ①降低温度时,Ksp(填“增大”、“减小”或“不变”).
②滴加少量浓盐酸,c(Ca2+)(填“增大”、“减小”或“不变”).
(4)II、含有Cr2O72﹣的废水毒性较大,某工厂废水中含5.00×10﹣3 molL﹣1的Cr2O72﹣ . 为使废水能达标排放,作如下处理: Cr2O72﹣ ![]() Cr3+、Fe3+
Cr3+、Fe3+ ![]() Cr(OH)3、Fe(OH)3
Cr(OH)3、Fe(OH)3
①该废水中加入绿矾(FeSO47H2O)和H+ , 发生反应的离子方程式为: .
②欲使10L该废水中的Cr2O72﹣完全转化为Cr3+ , 理论上需要加入g FeSO47H2O.
③若处理后的废水中残留的c(Fe3+)=2×10﹣13molL﹣1 , 则残留的Cr3+的浓度为 . (已知:Ksp[Fe(OH)3]=4.0×10﹣38 Ksp[Cr(OH)3]=6.0×10﹣31)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com