
ΓΨΧβΡΩΓΩΟΨΦΑΤδΜ·ΚœΈο‘Ύœ÷¥ζΙΛ“Β÷–”–Ή≈ΙψΖΚΒΡ”ΟΆΨΓΘ
(1Θ©Ήι≥…ΈΣMg17Al12ΒΡΟΨ¬ΝΚœΫπ «“Μ÷÷«±‘ΎΒΡ÷ϋ«β≤ΡΝœΘ§Β±Τδ÷ϋ«βΉν¥οΒΫΉν¥σ÷Β ±Ήι≥…±δΈΣΓΑ17MgH2+12AlΓ±Θ§‘ρMgΓΔAlΓΔMg17Al12»ΐ÷÷Έο÷ Α¥»έΒψ”…ΗΏΒΫΒΆΒΡΥ≥–ρ≈≈Ν–ΈΣ_______, 1molΓΑ17MgH2+12AlΓ±”κΉψΝΩNa0H»ή“ΚΖ¥”Π ±…ζ≥…ΒΡΤχΧεΒΡ÷ ΝΩ «___________gΓΘ
(2Θ©ΟΨΩ…”κSiO2ΖΔ…ζΕύ÷÷Ζ¥”ΠΘ§«“ΧθΦΰ≤ΜΆ§ ±ΒΟΒΫΒΡ≤ζΈο“≤≤ΜΆ§ΓΘΒ±Εΰ’Ώ‘ΎΗΏΈ¬ΧθΦΰœ¬ΖΔ…ζ÷ΟΜΜΖ¥”Π ±Θ°ΜΙ‘≠≤ζΈο «_________Θ§»τΟΨΙΐΝΩΘ§‘ρ≤ζΈοΈΣΝΫ÷÷ΟΨΒΡΕΰ‘ΣΜ·ΚœΈοΘ§–¥≥ωΖ¥”ΠΒΡΜ·―ßΖΫ≥Χ ΫΘΚ______ΓΘ
(3Θ©Φν ΫΧΦΥαΟΨ[MgCO3ΓΛ3H2O] «÷Ί“ΣΒΡΜ·ΙΛ‘≠ΝœΘ§œ¬ΆΦ±μ ΨΒΡ «÷Τ±ΗΥϋΒΡ“Μ÷÷ΙΛ“’Νς≥ΧΓΘ

ΩΣ Φ≥ΝΒμ ±ΒΡPH | Άξ»Ϊ≥ΝΒμ ±ΒΡpH | |
Fe(OH)3 | 2.7 | 3.7 |
Mg(OH)2 | 9.7 | 11 |
ΔΌ Mg9FeSi5O20÷–Χζ‘ΣΥΊΒΡΜ·ΚœΦέΈΣ____Θ§pHΒΡΒςΫΎΖΕΈß «______.
ΔΎ ‘ΦΝa «“Μ÷÷≥Θ”ΟΒΡ¬Χ…Ϊ―θΜ·ΦΝΘ§Φ”»κaΚσΖ¥”ΠΒΡάκΉ”ΖΫ≥Χ ΫΈΣ__________ΓΘ
Δέ –¥≥ωΝœ‘ϋΔρΒΡ“Μ÷÷”ΟΆΨΘΚ______ΓΘ“ΜΑψ»œΈΣc(Mg2+)Γή1ΓΝ10-5mol/L ±Θ§Mg2+“―Άξ»Ϊ≥ΝΒμΘ§‘ρMg(OH)2ΒΡKsp=______ΓΘ–¥≥ω…ζ≥…Φν ΫΧΦΥαΟΨΒΡάκΉ”ΖΫ≥Χ ΫΘΚ____________ΓΘ
ΓΨ¥πΑΗΓΩ Al>Mg>Mg17Al12 104 Si 4Mg+SiO2![]() 2MgO+Mg2Si +2 3.7ΓήpH<9.7 2Fe2++2H++H2O2=2Fe3++2H2O Φ”»»Fe(OH)3÷Τ±ΗΧζΚλ 1ΓΝ10-11 2Mg2++3CO32-+5H2O=Mg2CO3ΓΛMg(OH)2ΓΛ3H2O+2HCO3-
2MgO+Mg2Si +2 3.7ΓήpH<9.7 2Fe2++2H++H2O2=2Fe3++2H2O Φ”»»Fe(OH)3÷Τ±ΗΧζΚλ 1ΓΝ10-11 2Mg2++3CO32-+5H2O=Mg2CO3ΓΛMg(OH)2ΓΛ3H2O+2HCO3-
ΓΨΫβΈωΓΩΘ®1Θ©ΚœΫπΒΡ»έΒψ“ΜΑψΒΆ”ΎΗς≥…Ζ÷Ϋπ τΒΡ»έΒψΘ§ΟΨάκΉ”ΑκΨΕ¥σ”Ύ¬ΝάκΉ”ΑκΨΕΘ§“ρ¥ΥΫπ τΟΨΒΡ»έΒψΗΏ”Ύ¬ΝΘ§‘ρ‘ρMgΓΔAlΓΔMg17Al12»ΐ÷÷Έο÷ Α¥»έΒψ”…ΗΏΒΫΒΆΒΡΥ≥–ρ≈≈Ν–ΈΣ Al>Mg>Mg17Al12ΘΜ 1molΓΑ17MgH2+12AlΓ±”κΉψΝΩNaOH»ή“ΚΖ¥”Π ±¬ΝΚΆ«β―θΜ·ΡΤ»ή“ΚΖ¥”ΠΘ§12mol¬Ν…ζ≥…12molΓΝ1.5=18mol«βΤχΘ§MgH2”κΥ°Ζ¥”Π…ζ≥…«β―θΜ·ΟΨΚΆ«βΤχΘ§Έο÷ ΒΡΝΩ «34molΘ§Υυ“‘…ζ≥…ΒΡΤχΧεΒΡ÷ ΝΩ «52molΓΝ2g/molΘΫ104gΓΘ (2Θ©ΟΨΩ…”κSiO2ΖΔ…ζΕύ÷÷Ζ¥”ΠΘ§«“ΧθΦΰ≤ΜΆ§ ±ΒΟΒΫΒΡ≤ζΈο“≤≤ΜΆ§ΓΘΒ±Εΰ’Ώ‘ΎΗΏΈ¬ΧθΦΰœ¬ΖΔ…ζ÷ΟΜΜΖ¥”Π ±…ζ≥…―θΜ·ΟΨΚΆSiΘ§ΤδΜΙ‘≠≤ζΈο «SiΘΜ»γΙϊΟΨΙΐΝΩΘ§ΙηΚΆΟΨΜ·Κœ…ζ≥…ΙηΜ·ΟΨΘ§Ζ¥”ΠΒΡΜ·―ßΖΫ≥Χ ΫΈΣ4Mg+SiO2![]() 2MgO+Mg2SiΓΘ(3Θ©ΔΌMg9FeSi5O20÷–―θ‘ΣΥΊ «Θ≠2ΦέΘ§Ιη «ΘΪ4ΦέΘ§ΟΨ «ΘΪ2ΦέΘ§ΗυΨί’ΐΗΚΦέ¥ζ ΐΚΆΈΣ0Ω…÷ΣΧζ‘ΣΥΊΒΡΜ·ΚœΦέΈΣΘΪ2ΦέΓΘΒςΫΎpHΒΡΡΩΒΡ «≥ΝΒμΧζάκΉ”Θ§Υυ“‘pHΒΡΒςΫΎΖΕΈß « 3.7ΓήpH<9.7ΘΜΔΎ ‘ΦΝa «“Μ÷÷≥Θ”ΟΒΡ¬Χ…Ϊ―θΜ·ΦΝΘ§a «ΥΪ―θΥ°Θ§Φ”»κaΚσΖ¥”ΠΒΡάκΉ”ΖΫ≥Χ ΫΈΣ2Fe2++2H++H2O2=2Fe3++2H2OΓΘΔέΝœ‘ϋΔρ ««β―θΜ·ΧζΘ§Ω…”Οά¥÷Τ±ΗΧζΚλ―θΜ·ΧζΓΘ“ΜΑψ»œΈΣc(Mg2+)Γή1ΓΝ10-5mol/L ±Θ§Mg2+“―Άξ»Ϊ≥ΝΒμΓΘΗυΨί±μ÷– ΐΨίΩ…÷ΣΆξ»Ϊ≥ΝΒμ ±«β―θΗυ≈®Ε» «0.001mol/LΘ§‘ρMg(OH)2ΒΡKsp=10Θ≠5ΓΝ(0.001)2ΘΫ1ΓΝ10-11ΓΘΗυΨί‘≠Ή” ΊΚψΚΆΒγΚ… ΊΚψΩ…÷Σ…ζ≥…Φν ΫΧΦΥαΟΨΒΡάκΉ”ΖΫ≥Χ ΫΈΣ2Mg2++3CO32-+5H2O=Mg2CO3ΓΛMg(OH)2ΓΛ3H2O+2HCO3-ΓΘ
2MgO+Mg2SiΓΘ(3Θ©ΔΌMg9FeSi5O20÷–―θ‘ΣΥΊ «Θ≠2ΦέΘ§Ιη «ΘΪ4ΦέΘ§ΟΨ «ΘΪ2ΦέΘ§ΗυΨί’ΐΗΚΦέ¥ζ ΐΚΆΈΣ0Ω…÷ΣΧζ‘ΣΥΊΒΡΜ·ΚœΦέΈΣΘΪ2ΦέΓΘΒςΫΎpHΒΡΡΩΒΡ «≥ΝΒμΧζάκΉ”Θ§Υυ“‘pHΒΡΒςΫΎΖΕΈß « 3.7ΓήpH<9.7ΘΜΔΎ ‘ΦΝa «“Μ÷÷≥Θ”ΟΒΡ¬Χ…Ϊ―θΜ·ΦΝΘ§a «ΥΪ―θΥ°Θ§Φ”»κaΚσΖ¥”ΠΒΡάκΉ”ΖΫ≥Χ ΫΈΣ2Fe2++2H++H2O2=2Fe3++2H2OΓΘΔέΝœ‘ϋΔρ ««β―θΜ·ΧζΘ§Ω…”Οά¥÷Τ±ΗΧζΚλ―θΜ·ΧζΓΘ“ΜΑψ»œΈΣc(Mg2+)Γή1ΓΝ10-5mol/L ±Θ§Mg2+“―Άξ»Ϊ≥ΝΒμΓΘΗυΨί±μ÷– ΐΨίΩ…÷ΣΆξ»Ϊ≥ΝΒμ ±«β―θΗυ≈®Ε» «0.001mol/LΘ§‘ρMg(OH)2ΒΡKsp=10Θ≠5ΓΝ(0.001)2ΘΫ1ΓΝ10-11ΓΘΗυΨί‘≠Ή” ΊΚψΚΆΒγΚ… ΊΚψΩ…÷Σ…ζ≥…Φν ΫΧΦΥαΟΨΒΡάκΉ”ΖΫ≥Χ ΫΈΣ2Mg2++3CO32-+5H2O=Mg2CO3ΓΛMg(OH)2ΓΛ3H2O+2HCO3-ΓΘ


 ΧλΧλœρ…œ“Μ±ΨΚΟΨμœΒΝ–¥πΑΗ
ΧλΧλœρ…œ“Μ±ΨΚΟΨμœΒΝ–¥πΑΗ
| ΡξΦΕ | ΗΏ÷–ΩΈ≥Χ | ΡξΦΕ | ≥θ÷–ΩΈ≥Χ |
| ΗΏ“Μ | ΗΏ“ΜΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θ“Μ | ≥θ“ΜΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
| ΗΏΕΰ | ΗΏΕΰΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θΕΰ | ≥θΕΰΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
| ΗΏ»ΐ | ΗΏ»ΐΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θ»ΐ | ≥θ»ΐΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΫΪ9gΆ≠ΚΆΧζΒΡΜλΚœΈοΆΕ»κ100mlœΓœθΥα÷–Θ§≥δΖ÷Ζ¥”ΠΚσΒΟΒΫ±ξΉΦΉ¥Ωωœ¬1.12LNOΘ§ Θ”ύ4.8gΫπ τΘΜΦΧ–χΦ”»κ100mlΒ»≈®Ε»ΒΡœΓœθΥαΘ§Ϋπ τΆξ»Ϊ»ήΫβΘ§”÷ΒΟΒΫ±ξΉΦΉ¥Ωωœ¬1.12LNOΓΘ»τœρΖ¥”ΠΚσΒΡ»ή“Κ÷–Φ”»κKSCN»ή“ΚΘ§»ή“Κ≤Μ±δΚλΘ§‘ρœ¬Ν–ΥΒΖ®’ΐ»ΖΒΡ «
A. ‘≠ΜλΚœΈο÷–Ά≠ΚΆΧζΗς0.065mol
B. œΓœθΥαΒΡΈο÷ ΒΡΝΩ≈®Ε»ΈΣ4.0molΓΛLΘ≠1
C. ΒΎ“Μ¥Έ Θ”ύΒΡ4.8gΫπ τΈΣΆ≠ΚΆΧζ
D. œρΖ¥”ΠΚσΒΡ»ή“Κ÷–‘ΌΦ”»κΗΟœΓœθΥα100mlΘ§”÷ΒΟΒΫΒΡNO‘Ύ±ξΉΦΉ¥Ωωœ¬ΒΡΧεΜΐΈΣ0.56L
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ‘Ύ’τΖΔΟσ÷–Φ”»»’τΗ…‘ΌΦ”»»(ΒΆ”Ύ400Γφ)œ¬Ν–Έο÷ ΒΡ»ή“ΚΘ§Ω…“‘ΒΟΒΫΗΟΈο÷ ΙΧΧεΒΡ «Θ® Θ©
AΘ°¬»Μ·¬Ν BΘ°ΧΦΥα«βΡΤ CΘ°ΝρΥα―«Χζ DΘ°ΝρΥαΟΨ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ≥ΘΈ¬œ¬Θ§‘Ύ20mL0.1mol/L HR »ή“Κ÷–ΒΈΦ”0.1000mol/LNaOH»ή“ΚΘ§ΜλΚœ»ή“ΚΒΡPH”κΥυΦ”NaOH»ή“ΚΧεΜΐΒΡΙΊœΒ»γΆΦΥυ ΨΓΘœ¬Ν–ΆΤΕœ’ΐ»ΖΒΡ «

A. ΔΌΓΔΔΎΓΔΔέ»ΐΒψ÷–Θ§ΔέΕ‘”ΠΒΡ»ή“Κ÷–cΥ°(H+)ΓΛcΥ°(OH-)Ήν¥σ
B. HR»ή“Κ÷–÷Μ¥φ‘ΎH+ΓΔR-ΓΔOH-ΓΔH2OΥΡ÷÷ΈΔΝΘ
C. ΔΎΒψ»ή“Κ÷–“ΜΕ®¥φ‘Ύc(Na+)>c(R-)>c(H+)=c(OH-)
D. NaRΒΡΥ°Ϋβ≥Θ ΐKaΚΆΥ°Ϋβ≥ΧΕ»ΘΚΔέ>ΔΎ>ΔΌ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ…ηNAΈΣΑΔΖϋΦ”Β¬¬ό≥Θ ΐΒΡ÷ΒΓΘœ¬Ν–ΥΒΖ®’ΐ»ΖΒΡ «
A. ±ξΉΦΉ¥Ωωœ¬Θ§6.0g NOΚΆ2.24L O2ΜλΚœΘ§ΥυΒΟΤχΧεΒΡΖ÷Ή” ΐΡΩΈΣ0.2NA
B. ≥ΘΈ¬≥Θ―Ιœ¬Θ§0.1mol Na2OΚΆNa2O2Ήι≥…ΒΡΜλΚœΈο÷–Θ§“θάκΉ”ΒΡ ΐΡΩΈΣ0.1NA
C. C2H4ΚΆC3H6ΒΡΜλΚœΈοΒΡ÷ ΝΩΈΣmg,ΥυΚ§ΧΦ«βΦϋΒΡ ΐΡΩΈΣ3m/14NA
D. 1molΦΉΜυΘ®![]() Θ©ΥυΚ§ΒΡΒγΉ” ΐΈΣ7NA
Θ©ΥυΚ§ΒΡΒγΉ” ΐΈΣ7NA
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΔώΓΔΡ≥Έ¬Ε» ±Θ§‘Ύ“ΜΗω2LΒΡΟή±’»ίΤς÷–Θ§XΓΔYΓΔZ»ΐ÷÷ΤχΧεΈο÷ ΒΡΈο÷ ΒΡΝΩΥφ ±ΦδΒΡ±δΜ·«ζœΏ»γΆΦΥυ ΨΓΘΗυΨίΆΦ÷– ΐΨίΧνΩ’ΘΚ
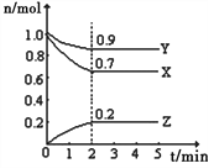
Θ®1Θ©ΗΟΖ¥”ΠΒΡΜ·―ßΖΫ≥Χ ΫΈΣ_______________________ΓΘ
Θ®2Θ©Ζ¥”ΠΩΣ Φ÷Ν2minΘ§“‘ΤχΧεX±μ ΨΒΡΤΫΨυΖ¥”ΠΥΌ¬ ΈΣ_________ΓΘΖ¥”Π¥οœόΕ» ±Θ§YΒΡΉΣΜ·¬ ΈΣ________Θ§Ζ¥”ΠΩΣ Φ ±”κΖ¥”Π¥οΤΫΚβΉ¥Χ§ ±ΒΡ―Ι«Ω÷°±»ΈΣ__________ΓΘ
Θ®3Θ©»τ…œ ωΖ¥”Π‘ΎΦΉΓΔ““ΝΫΗωœύΆ§»ίΤςΡΎΆ§ ±Ϋχ––Θ§Ζ÷±π≤βΒΟΦΉ÷–v(X)ΘΫ9 mol/(LΓΛmin)Θ§““÷–v(Y)ΘΫ0.1 mol/(LΓΛs)Θ§‘ρ__________÷–Ζ¥”ΠΗϋΩλΓΘ
ΔρΓΔΡ≥―ßœΑ–ΓΉι”Ο»γœ¬ΆΦΥυ ΨΉΑ÷ΟAΓΔBΖ÷±πΧΫΨΩΫπ τ–Ω”κœΓΝρΥαΒΡΖ¥”ΠΘ§ Β―ιΙΐ≥Χ÷–A…’±≠ΡΎΒΡ»ή“ΚΈ¬Ε»…ΐΗΏΘ§B…’±≠ΒΡΒγΝςΦΤ÷Η’κΖΔ…ζΤΪΉΣΘ§«κΜΊ¥π“‘œ¬Έ ΧβΓΘ

Θ®4Θ©B÷–ZnΑε «_________ΦΪΘ§ΖΔ…ζΒΡΒγΦΪΖ¥”Π «_________Θ§CuΑε…œΒΡœ÷œσ «___________ΓΘ
Θ®5Θ©¥”ΡήΝΩΉΣΜ·ΒΡΫ«Ε»ά¥Ω¥Θ§ A÷– «ΫΪΜ·―ßΡήΉΣ±δΈΣ_________Θ§B÷–÷ς“Σ «ΫΪΜ·―ßΡήΉΣ±δΈΣ_________ΓΘ
Θ®6Θ©ΗΟ–ΓΉιΆ§―ßΖ¥ΥΦ‘≠Βγ≥ΊΒΡ‘≠άμΘ§Τδ÷–ΙέΒψ’ΐ»ΖΒΡ «_________Θ®ΧνΉ÷ΡΗ–ρΚ≈Θ©ΓΘ
AΘ°‘≠Βγ≥ΊΖ¥”ΠΒΡΙΐ≥Χ÷–“ΜΕ®”–ΒγΉ”ΉΣ“Τ
BΘ°‘≠Βγ≥ΊΉΑ÷ΟΒγΉ”ΝςœρΘΚΗΚΦΪΓζΆβœΏ¬ΖΓζ’ΐΦΪΓζΒγΫβ÷ ΓζΗΚΦΪ
CΘ°ΒγΦΪ“ΜΕ®≤ΜΡή≤ΈΦ”Ζ¥”Π
DΘ°―θΜ·Ζ¥”ΠΚΆΜΙ‘≠Ζ¥”ΠΩ…“‘≤πΩΣ‘ΎΝΫΦΪΖΔ…ζ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩœ¬Ν–ΥΒΖ®≤Μ’ΐ»ΖΒΡ «Θ®ΓΓΓΓΘ©
A. Β―ι “”ΠΫΪΡΤ±Θ¥φ‘ΎΟΚ”Ά÷–
B.Ζ÷“Κ¬©ΕΖΚΆ»ίΝΩΤΩ‘Ύ Ι”Ο«ΑΕΦ“ΣΦ묩
C.Ω…”ΟΨΤΨΪ¥ζΧφCCl4ίΆ»ΓΒβΥ°÷–ΒΡΒβΒΞ÷
D.Ϋπ τΟΨ ßΜπ≤ΜΩ…”ΟΥ°ά¥ΟπΜπ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩάύΆΤΥΦΈ§ «Μ·―ßΫβΧβ÷–≥Θ”ΟΒΡ“Μ÷÷ΥΦΈ§ΖΫΖ®Θ§œ¬Ν–”–ΙΊΖ¥”ΠΖΫ≥Χ ΫΒΡάύΆΤ’ΐ»ΖΒΡ «
“― ÷Σ | άύ ΆΤ | |
A | ΫΪΧζΖέΆΕ»κœΓΝρΥα÷– Fe+H2SO4(œΓ)= FeSO4+H2Γϋ | ΫΪΧζΖέΆΕ»κœΓœθΥα÷– Fe+2HNO3(œΓ)= Fe(NO3)2+H2Γϋ |
B |
|
|
C | ΫΪ““œ©Ά®»κδεΥ°÷– CH2ΘΫCH2+Br2ΓζCH2BrCH2Br | ΫΪ±ϊœ©Ά®»κδεΥ°÷– CH3CHΘΫCH2+Br2ΓζCH3CHBrCH2Br |
D | ““œ©‘Ύ Β±ΧθΦΰœ¬÷ΤΨέ““œ© nCH2ΘΫCH2 | ±ϊœ©‘Ύ Β±ΧθΦΰœ¬÷ΤΨέ±ϊœ© nCH3CHΘΫCH2 |
A. A B. B C. C D. D
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ≥ΘΈ¬œ¬Θ§”Ο0.1000molΓΛL-1ΒΡ―ΈΥαΒΈ 0.1000molΓΛL-1Na2CO3»ή“Κ25.00mLΓΘ”ΟpH¥ΪΗ–Τς≤βΒΟΜλΚœ»ή“ΚΒΡpH±δΜ·«ζœΏ»γΆΦΘ§œ¬Ν–ΥΒΖ®’ΐ»ΖΒΡ «

A. cΓζdΒψΖΔ…ζΒΡ÷ς“ΣάκΉ”Ζ¥”ΠΘΚHCO3-+H+=H2O+CO2
B. ‘ΎbΒψ ±Θ§c(CO32-)>c(HCO3-)>c(OH-)
C. ‘ΎdΒψ ±Θ§ c(OH-)=c(H+)+c(HCO3-)+2c(H2CO3)
D. ‘ΎeΒψ ±Θ§ c(H+)=2c(CO32-)+c(HCO3-)+c(OH-)
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΙζΦ ―ß–Θ”≈―Γ - ΝΖœΑ≤αΝ–±μ - ‘ΧβΝ–±μ
Κΰ±± ΓΜΞΝΣΆχΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΤΫΧ® | Άχ…œ”–ΚΠ–≈œΔΨΌ±®Ή®«χ | Βγ–≈’©Τ≠ΨΌ±®Ή®«χ | …φάζ Ζ–ιΈό÷ς“ε”–ΚΠ–≈œΔΨΌ±®Ή®«χ | …φΤσ«÷»®ΨΌ±®Ή®«χ
ΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΒγΜΑΘΚ027-86699610 ΨΌ±®” œδΘΚ58377363@163.com