
【题目】莫尔法是用硝酸银标准溶液测定卤离子含量的沉淀滴定法。某实验兴趣小组将无水FeC13与氯苯混合发生反应:2FeCl3+C6H5Cl![]() 2FeC12+C6H4C12+HC1↑,将生成的HC1用水吸收,利用莫尔法测出无水FeC13的转化率,同时得到常用的还原剂FeC12。按照如图装置,在三颈烧瓶中放入162.5g无水FeC13与225g氯苯,控制反应温度在130℃下加热3h,冷却、过滤、洗涤、干燥得到粗产品。有关数据如下:
2FeC12+C6H4C12+HC1↑,将生成的HC1用水吸收,利用莫尔法测出无水FeC13的转化率,同时得到常用的还原剂FeC12。按照如图装置,在三颈烧瓶中放入162.5g无水FeC13与225g氯苯,控制反应温度在130℃下加热3h,冷却、过滤、洗涤、干燥得到粗产品。有关数据如下:
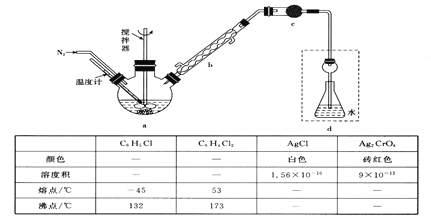
回答下列问题:
(1)仪器c的名称是_______________,盛装的试剂是___________________。
(2)仪器b球形冷凝管的作用是_________________________________。
(3)下列各装置(盛有蒸馏水)能代替图中虚线框内部分的是____________(填序号)。
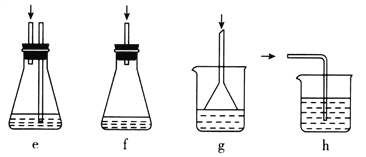
(4)如何从滤液中回收过量的氯苯:_______________________________________。
(5)将锥形瓶内的溶液稀释至1000mL,从中取10.00mL,滴加几滴K2CrO4作指示剂,用0.2000mol·L-1AgNO3溶液进行滴定,当达到终点时,消耗22.50mL AgNO3溶液。
①滴定终点的现象是________________________,使用棕色滴定管进行滴定的原因是________________________________________。
②无水FeC13的转化率![]() =__________%。
=__________%。
【答案】 干燥管 无水氯化钙 冷凝回流及导气 eg 蒸馏滤液,收集132℃的馏分 当滴入最后一滴时,出现红色沉淀 防止AgNO3溶液见光分解 90
【解析】在三颈烧瓶中放入162.5g无水FeC13与225g氯苯,控制反应温度在130℃下加热3h,发生反应2FeCl3+C6H5Cl![]() 2FeC12+C6H4C12+HC1↑,将生成的HC1用水吸收,由于无水氯化铁能够水解,因此应该保证反应装置中没有水存在,c中可以盛放能够干燥氯化氢气体的干燥剂,如无水氯化钙、五氧化二磷等固体干燥剂。
2FeC12+C6H4C12+HC1↑,将生成的HC1用水吸收,由于无水氯化铁能够水解,因此应该保证反应装置中没有水存在,c中可以盛放能够干燥氯化氢气体的干燥剂,如无水氯化钙、五氧化二磷等固体干燥剂。
(1)根据图示,仪器c球形干燥管,盛装的试剂可以是无水氯化钙、五氧化二磷等,故答案为:干燥管;无水氯化钙;
(2)仪器b球形冷凝管可以冷凝回流氯苯等,同时兼导气的作用,故答案为:冷凝回流及导气;
(3)吸收氯化氢需要防止倒吸,能代替图中虚线框内部分的有eg,故答案为:eg;
(4)根据C6H5Cl和C6H4C12的沸点数据可知,二者沸点相差较大,利用通过蒸馏的方法回收过量的氯苯,故答案为:蒸馏滤液,收集132℃的馏分;
(5)①将锥形瓶内的溶液稀释至1000mL,从中取10.00mL,滴加几滴K2CrO4作指示剂,用0.2000mol·L-1AgNO3溶液进行滴定,当滴入最后一滴时,出现红色沉淀,表示达到了滴定终点,由于硝酸银容易见光分解,使用棕色滴定管进行滴定可以防止AgNO3溶液见光分解,故答案为:当滴入最后一滴时,出现红色沉淀;防止AgNO3溶液见光分解;
②根据反应的方程式可知,FeC12~2AgNO3,因此n(FeC13)= n(FeC12)=2×0.2000mol·L-1×0.02250L=0.009mol,则无水FeC13的转化率![]() =
=![]() ×100%=90%,故答案为:90%。
×100%=90%,故答案为:90%。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】“神舟六号”的成功发射和返回,第一次实现了我国有人参与的空间科学实验。整个飞船应用了许多尖端的合成材料。下列物质中,不属于合成材料的是( )
A. 人造丝 B. 有机玻璃 C. 硅橡胶 D. 黏合剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质:①金刚石和石墨; ②H、D和T;③苯和乙苯;④CH3(CH2)2CH3和(CH3)2CHCH3中,互为同位素的是(填序号,下同) , 互为同素异形体的是 , 互为同系物的是 , 属于同分异构体的是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图两瓶体积相等的气体,在同温同压时瓶内气体的关系一定正确的是( )

A. 所含原子数相等 B. 气体密度相等C.气体质量相等 D.摩尔质量相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学要在奥运五连环中填入物质,使相连物质间能发生反应,不相连物质间不能发生反应。你认为“五连环”中有空缺的一环应填入的物质是( )

A. 硫酸 B. 氧气 C. 二氧化碳 D. 氧化钙
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某二元酸H2A在水中的电离方程式是H2A = H+ + HA﹣,HA﹣![]() H+ + A2﹣.回答下列问题:
H+ + A2﹣.回答下列问题:
(1)Na2A溶液显______________(填“酸性”、“中性”或“碱性”),理由是________________________________(用离子方程式或必要的文字说明).
(2)常温下,已知0.1molL﹣1NaHA溶液pH=2,则0.1molL﹣1H2A溶液中氢离子的物质的量浓度可能______0.11molL﹣1(填“大于”、“等于”或“小于”),理由是_____________________.
(3)0.1molL﹣1NaHA溶液中各种离子浓度由大到小的顺序是_________.
(4)Na2A溶液中,下列表述正确的是_________.
A.c(Na+) + c(H+)= c(HA﹣)+ 2c(A2﹣)+ c(OH﹣)
B. c(OH﹣)= c(HA﹣)+ c(H+)
C.c(OH﹣)= c(HA﹣)+ c(H+)+ 2c(H2A)
D.c (Na+)= 2[c(HA﹣)+ c(A2﹣) + c(H2A)]
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物H(4-苯基-2-丁酮)是一种重要的医药中间体。以下是合成H的一种路线:
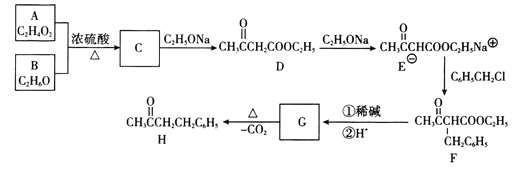
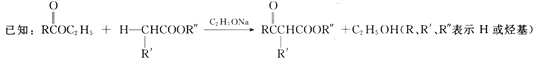
回答下列问题:
(1)A的化学名称为__________________。
(2)D中官能团的名称为___________,E→F的化学反应类型为___________________。
(3)G的结构简式为________________________。
(4)写出C→D的化学反应方程式:__________________________________________。
(5)H存在多种同分异构体,满足下列条件的同分异构体共___________种,其中核磁共振氢谱有5组峰,峰面积比为6:2:2:1:1的结构简式为__________________________。
①含有苯环且只有一个支链;②能发生银镜反应
(6)结合信息,写出用乙酸乙酯为原料制备化合物丙酮(CH3COCH3)的合成路线:___________________________________________________________(其他试剂任选)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇是重要的化工原料。利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇,可能发生的反应如下:
i. CO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g) △H1
CH3OH(g)+H2O(g) △H1
ii. CO2(g)+ H2(g)![]() CO(g)+H2O(g) △H2
CO(g)+H2O(g) △H2
iii. CH3OH(g)![]() CO(g) +2H2(g) △H3
CO(g) +2H2(g) △H3
回答下列问题:
(1)已知反应ⅱ中相关化学键键能数据如下:

由此计算△H2=__________kJ·mol-1。已知△H3=99kJ·mol-1,则△H1=_________kJ·mol-1。
(2)一定比例的合成气在装有催化剂的反应器中反应12小时。体系中甲醇的产率和催化剂的催化活性与温度的关系如图1所示。

①温度为470K时,图中P点_______ (填“是”或“不是”)处于平衡状态。在490K之前,甲醇产率随着温度升高而增大的原因是_______;490K之后,甲醇产率下降的原因是_______。
②一定能提高甲醇产率的措施是______________。
A.增大压强 B,升高温度 C.选择合适催化剂 D.加入大量催化剂
(3)图2为一定比例的CO2/H2,CO/H2、CO/CO2/H2条件下甲醇生成速率与温度的关系。
①490K时,根据曲线a、c判断合成甲醇的反应机理是_________ (填“I”或“II")。
![]()
②490K时,曲线a与曲线b相比,CO的存在使甲醇生成速率增大,从热力学与动力学角度,并结合反应i、ⅱ分析原因_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com