
����Ŀ����+6�۸�����ˮ����Ⱦ��������Ƴ������Ķ�ͭ��ˮ����������һ������![]() �������÷�ˮ���û�ԭ�������������������£�
�������÷�ˮ���û�ԭ�������������������£�

��1���������ϡ�������pH����ѡ�������ԭ����______________________________��
��2����֪ÿ����1mol Na2S2O3ת��8mol e-�������Na2S2O3��Һʱ������Ӧ�����ӷ���ʽΪ��_________________________________________________________��
��3����֪Cr(OH)3�Ļ�ѧ������Al(OH)3���ơ�����ڼ���NaOH��ҺʱҪ������Һ��pH���ܹ��ߣ�����Ϊ___________________________________________(�����ӷ���ʽ��ʾ)��
��4��������Һ�п��Դ�������������Na2S2O3��Һ��ѵ���__________(��ѡ�����)��
A��FeSO4��Һ B��ŨH2SO4C��Na2SO3��Һ D������KMnO4��Һ
��5��ij����ˮ�к�1.50��10-3mol/L��![]() ������ˮ�����õ����Բ���Cr0.5Fe1.5FeO4(Cr�Ļ��ϼ�Ϊ+3��Fe�Ļ��ϼ�����Ϊ+3��+2)�ɱ��Ϊ������ʹ1 L�÷�ˮ�е�
������ˮ�����õ����Բ���Cr0.5Fe1.5FeO4(Cr�Ļ��ϼ�Ϊ+3��Fe�Ļ��ϼ�����Ϊ+3��+2)�ɱ��Ϊ������ʹ1 L�÷�ˮ�е�![]() ��ȫת��ΪCr0.5Fe1.5FeO4����������Ҫ����__________gFeSO4��7H2O��(��֪FeSO4��7H2O��Ħ������Ϊ278g/mol)
��ȫת��ΪCr0.5Fe1.5FeO4����������Ҫ����__________gFeSO4��7H2O��(��֪FeSO4��7H2O��Ħ������Ϊ278g/mol)
���𰸡�![]() ������������C1-������������Ⱦ����
������������C1-������������Ⱦ���� ![]() Cr(OH)3+OH-=
Cr(OH)3+OH-=![]() +2H2O C 4.17
+2H2O C 4.17
��������
��Cr2O72-���ӵķ�ˮ����Na2S2O3��Һ������ҺpH=2~3���ظ�������ӱ���ԭΪCr3+���ӣ��ټ�������������Һ������ҺpH����Cr��OH��3��Cr(OH)3�Ļ�ѧ������Al(OH)3���ƣ������������м���NaOH��ҺʱҪ������Һ��pH���ܹ��ߣ���ֹCr(OH)3�ܽ⡣
��1��������������Cr2O72-����ǿ�����ԣ�����Cl- ���ӷ���������ԭ��Ӧ��������������ɻ�����Ⱦ���������������������
��2����֪ÿ����1mol Na2S2O3ת��8mol e-�����ݵ���ת���غ㣬��֪S2O32����������SO42����Cr2O72���ӱ���ԭΪCr3+���ӣ���ƽ�ɵ����ӷ���ʽΪ��3S2O32+4Cr2O72+26H+�T6SO42+8Cr3++13H2O��
��3��Cr(OH)3�Ļ�ѧ������Al(OH)3���ƣ�Cr(OH)3�����ܽ��ڹ���������������Һ�У���Ӧ����NaCrO2��H2O����Ӧ���ӷ���ʽΪ��Cr(OH)3+OH=CrO2+2H2O��
��4�����Դ�������������Na2S2O3��Һ����Ҫ���л�ԭ�ԣ��ܻ�ԭ�ظ�������ӣ�
A��FeSO4��Һ ���������Ӿ��л�ԭ�ԣ����Ի�ԭCr2O72���ӣ������������µ��������������ӣ���A�����ϣ�
B��ŨH2SO4 ���������ԣ���B�����ϣ�
C��Na2SO3��Һ ������������Ӿ��л�ԭ��,���Ի�ԭCr2O72����C���ϣ�
D������KMnO4��Һ��ǿ���������ܻ�ԭCr2O72����D�����ϣ�
�ʴ�ѡC��
��5��1L��ˮ�к�n(Cr2O72)=1.50��103mol������Crԭ�ӡ�Feԭ���غ㣬�ɵã�
Cr2O724Cr0.5Fe1.5FeO410FeSO47H2O��
����������n(FeSO47H2O)=10n(Cr2O72)=1.50��103mol��10=0.015mol��
����m(FeSO47H2O)��0.015mol��278g/mol=4.17g��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1����ȫȼ��0.1 molij����ȼ�ղ�������ͨ��Ũ���ᡢŨ��Һ��ʵ������Ƶ�Ũ��������9 g��Ũ��Һ����17.6 g�������Ļ�ѧʽΪ____����д�������п��ܵĽṹ��ʽ��________��
��2��ij����O2����ȫȼ�գ�����6.6 g CO2��3.6 g H2O���ڱ�״̬�¸������ܶ�Ϊ1.964 3 g��L1�����仯ѧʽΪ_______��
��3��ij��������Է�������Ϊ128���������Ļ�ѧʽΪ_______��
��4����120 ����101 kPa�������£�ij��̬����һ�������������Ļ�������ڵ�ȼ��ȫ��Ӧ���ٻָ���ԭ�����¶�ʱ�����������С�ˣ�����������ڵ���ԭ�Ӹ���___(�����)��
A��С��4 B������4 C������4 D�����ж�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ͼװ�ý���ʵ�飬�����ƶ���ȷ����(����)
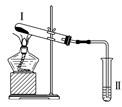
ѡ�� | �����Լ� | �����Լ������� | �ƶ� |
A | �Ȼ�� | ��̪��Һ�����ɫ | �Ȼ���ȶ� |
B | �������� | Ʒ����Һ��ɫ | FeSO4�ֽ�����FeO��SO2 |
C | Ϳ��ʯ���͵����Ƭ | ���Ը��������Һ��ɫ | ʯ���ͷ����˻�ѧ�仯 |
D | ������ˮ���� | ����ˮð�� | ������ˮ���������˷�Ӧ |
A. A B. B C. C D. D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij����С����ʵ��������ͼ��ʾװ�ÿ�����ȡ������֤����ijЩ���ʣ�ͬʱ�ռ����������ĵ�������ش�
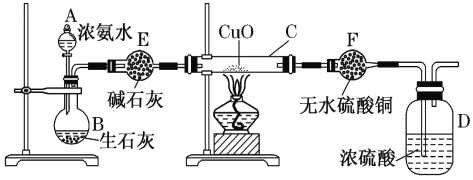
(1)д������ʯ�Һ�Ũ��ˮ��Ӧ�ư��Ļ�ѧ����ʽ____________________________�����ͷų�NH3��ԭ��_______________________________________________________��
(2)ʵ�����һ��ʱ�䣬�۲쵽Ӳ�ʲ������ں�ɫ����ͭ��ĩ��Ϊ��ɫ��ʢ��ˮ����ͭ�ĸ�����ڳ�����ɫ�����������ij������ܿڴ��ռ�������������ĵ�����������Щ����д����Ӳ�ʲ������ڷ�����Ӧ�Ļ�ѧ����ʽ��___________________________________��
(3)�����ij������ܿڴ��ռ���������ĵ������ռ�������________��
A���ſ����� B����ˮ�� C���������ռ�
(4) E�еļ�ʯ��________(������������������)����CaCl2��
(5) ��Ũ�����з���ͭƬ����ͭ��ʣ�࣬��ʼ��Ӧ�Ļ�ѧ����ʽΪ __________________��
(6) ����12.8 gͭ��һ������Ũ���ᷴӦ��ͭ������ʱ��������NO��NO2 ����V L(��״��)����������������һ�������������ǡ�ñ�һ������NaOH��Һ��������������,��ͨ�����������ʵ�����_____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧʵ���ǻ�ѧѧϰ����Ҫ���ݡ����������յ�֪ʶ������������ݡ�
![]() ʵ������Ҫ����0.1 mol��L-1NaOH��Һ230mL����ش��������⣺
ʵ������Ҫ����0.1 mol��L-1NaOH��Һ230mL����ش��������⣺
![]() Ӧѡ��____mL������ƿ������ƽ��ȡ____g NaOH��
Ӧѡ��____mL������ƿ������ƽ��ȡ____g NaOH��
![]() �ܽ�NaOH�����Һ����ȴ�����º���ת��������ƿ�С�������ת�ƻ�ʹ��Һ��Ũ��______(����ƫ��������ƫС������ͬ)����ϴ���ձ��Ͳ������Ĺ����У�ÿ��ϴ��Һ����ע������ƿ��������ʧ���Һ�壬����ᵼ����Һ��Ũ��______��
�ܽ�NaOH�����Һ����ȴ�����º���ת��������ƿ�С�������ת�ƻ�ʹ��Һ��Ũ��______(����ƫ��������ƫС������ͬ)����ϴ���ձ��Ͳ������Ĺ����У�ÿ��ϴ��Һ����ע������ƿ��������ʧ���Һ�壬����ᵼ����Һ��Ũ��______��
![]() ������Ϊ�������ַ���ֻ������0.1 mol��L-1��NaOH��Һ�������õ�0.1000 mol��L-1��NaOH��Һ�����������������__________________________________________��
������Ϊ�������ַ���ֻ������0.1 mol��L-1��NaOH��Һ�������õ�0.1000 mol��L-1��NaOH��Һ�����������������__________________________________________��
![]() ѡ������ʵ�鷽���������ʣ������뷽����������ں����ϡ�
ѡ������ʵ�鷽���������ʣ������뷽����������ں����ϡ�
![]() ��ȡ��Һ
��ȡ��Һ ![]() ����
���� ![]() �ᾧ
�ᾧ ![]() ����
���� ![]() ����
���� ![]() ��Һ
��Һ
![]() ���뱥��ʳ��ˮ��ɳ�ӵĻ����______��
���뱥��ʳ��ˮ��ɳ�ӵĻ����______��
![]() ������غ��Ȼ��ƵĻ��Һ�л�������______��
������غ��Ȼ��ƵĻ��Һ�л�������______��
![]() �ӵ�ˮ����ȡ�ⵥ��______��
�ӵ�ˮ����ȡ�ⵥ��______��
![]() ����ˮ�����͵Ļ����______��
����ˮ�����͵Ļ����______��
![]() ����
����![]() �е�Ϊ
�е�Ϊ![]() �ͼױ�
�ͼױ�![]() �е�Ϊ
�е�Ϊ![]() �Ļ����______��
�Ļ����______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ���ǣ� ��
A. NH3��CH4������ԭ�Ӷ���sp3�ӻ�
B. ��̬ԭ�ӵĺ�������Ų�Ϊ[Kr]4d105s1��Ԫ������d��
C. SO2��CO2����ֱ���η��ӣ�������ԭ�Ӷ���sp�ӻ�
D. �����ɵ��ܼ�ԾǨ���ϸ��ܼ�ʱ����ͨ��������ֱ����ȡԭ�ӵķ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£�������Һ�У��й������ʵ���Ũ�ȹ�ϵ��ȷ����( )
A. 0.1mol��L-1(NH4)2Fe(SO4)2��Һ��c(![]() )>c(
)>c(![]() )>c(H+)>c(Fe2+)
)>c(H+)>c(Fe2+)
B. ��100mL 0.1mol��L-1Na2CO3��Һ��εμӵ�100mL 0.1mol��L-1�����У�c(Na+)>c(C1-)>c(![]() )>c(
)>c(![]() )
)
C. pH=12��NaOH��Һ������pH=2�Ĵ�����Һ��Ϻ�c(CH3COO-)>c(Na+)>c(H+)>c(OH-)
D. 0.1mol��L-1NaHCO3��Һ��c(H+)+2c(H2CO3)=c(OH-)+c(![]() )
)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��1999�����ʱ�����̷��ܶ��fӢ��Ⱦ�¼������fӢ��һ����廯����Ķ��ȴ���������ܳƣ��ṹ�ȶ������Ա���Ȼ�ֽ⣬�ǹ��ϵ���Σ�յ��°�����֮һ��2,3,7,8-���ȶ��������fӢ�����е�һ�֣��ṹ��ͼ������˵���в���ȷ���� ( )
![]()
A. ���ķ���ʽΪC12H4O2Cl4B. �����ܷ����ӳɷ�Ӧ
C. ����һ��ȡ������һ��D. �˷����й�ƽ���ԭ�������22��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵������ȷ���ǣ� ��
A.һ����̼��Ħ��������6.02��1023���������ӵ���������ֵ�����
B.6.02��1023��N2��6.02��1023��O2�������ȵ���7�U8
C.3.2gO2������ԭ����ĿԼΪ0.2��6.02��1023
D.���¡���ѹ�£�0.5��6.02��1023��������̼����������44g
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com