
【题目】根据物质结构有关性质和特点,回答下列问题:
(1)基态As原子的价层电子的电子云轮廓图形状为_____________。
(2)Na3AsO3可用于碘的微量分析。Na3AsO3中所含阴离子的立体构型为_____________,写出一种与其互为等电子体的分子:_____________(填化学式)。
(3)丙烯腈(CH2=CH-CN)分子中碳原子轨道杂化类型是____________。
(4)Ni与Ca处于同一周期,且核外最外层电子构型相同,但金属Ni的熔点和沸点均比金属Ca的高,其原因为___________。区分晶体Ni和非晶体Ni的最可靠的科学方法为___________。
(5)钛存在两种同素异形体,α—Ti采纳六方最密堆积,β—Ti采纳体心立方堆积,由α—Ti转变为β—Ti晶体体积____________(填“膨胀”或“收缩”)。
(6)某镍白铜合金的立方晶胞结构如图所示。若合金的密度为d g·cm-3,晶胞参数a=______ nm。

【答案】球形、哑铃形(或纺锤形) 三角锥形 PCl3、PBr3、NF3、NCl3等 sp2 sp Ni的原子半径较小,价层电子数目较多,金属键较强 X-射线衍射法 膨胀 ![]() ×107
×107
【解析】
(1)基态As原子的价层电子排布在4s24p3;
(2)AsO33-中As原子的杂化轨道数是![]() ;等电子体是原子数、价电子数相同的离子或分子,AsO33-的原子数是4、价电子数是26;
;等电子体是原子数、价电子数相同的离子或分子,AsO33-的原子数是4、价电子数是26;
(3)丙烯腈(CH2=CH-CN)中双键碳是sp2杂化、叁键碳是sp杂化;
(4)金属键的强弱与原子半径、价层电子数有关。X-射线衍射法可以区分晶体和非晶体;
(5)六方最密堆积空间利用率74%,体心立方堆积空间利用率68%;
(6)根据均摊原则,晶胞中铜原子数是![]() 、镍原子数是
、镍原子数是![]() 。
。
(1)基态As原子的价层电子排布在4s24p3,s轨道为球形、p轨道为哑铃形;
(2)AsO33-中As原子的杂化轨道数是![]() ,有1个孤电子对,所以立体构型为三角锥形;等电子体是原子数、价电子数相同的离子或分子,AsO33-的原子数是4、价电子数是26,与AsO33-互为等电子体的分子是PCl3、PBr3、NF3、NCl3等;
,有1个孤电子对,所以立体构型为三角锥形;等电子体是原子数、价电子数相同的离子或分子,AsO33-的原子数是4、价电子数是26,与AsO33-互为等电子体的分子是PCl3、PBr3、NF3、NCl3等;
(3)丙烯腈(CH2=CH-CN)中有2个双键碳、1个叁键碳,碳原子轨道杂化类型是sp2、sp;
(4)与Ca相比 ,Ni的原子半径较小,价层电子数目较多,金属键较强,所以Ni的熔点和沸点均比金属Ca的高;区分晶体Ni和非晶体Ni的最可靠的科学方法为X-射线衍射法;
(5)六方最密堆积空间利用率74%,体心立方堆积空间利用率68%,由α—Ti转变为β—Ti晶体体积膨胀;
(6)根据均摊原则,晶胞中铜原子数是![]() 、镍原子数是
、镍原子数是![]() ;晶胞的摩尔质量是(64×3+59)g/mol;所以
;晶胞的摩尔质量是(64×3+59)g/mol;所以![]() ,a=
,a=![]() ×107nm。
×107nm。


 精英口算卡系列答案
精英口算卡系列答案 应用题点拨系列答案
应用题点拨系列答案科目:高中化学 来源: 题型:
【题目】某工厂采用电解法处理含铬废水,利用耐酸电解槽阴阳极,槽中盛放含铬废水,原理示意如图,下列说法不正确的是( )

A.a为电源正极
B.阳极区溶液中发生的氧化还原反应为Cr2O72—+6Fe2++14H+==2Cr3++6Fe3++7H2O
C.若不考虑气体的溶解,当收集到H213.44L(标准状况)时,有0.2 molCr2O72—被还原
D.阴极区附近溶液pH增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】同温同压下,等质量的 SO2气体和 SO3气体相比较,正确的说法是
A. 密度比为 4:5 B. 物质的量之比为 4:5
C. 体积比为 1:1 D. 原子数之比为 3:4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碘在地壳中主要以NaIO3的形式存在,在海水中主要以I-的形式存在,几种粒子之间有如图所示关系,根据图示转化关系推测下列说法不正确的是

A. 可用KI淀粉试纸和食醋检验加碘盐中是否含有碘
B. 足量Cl2能使湿润的KI淀粉试纸变白的原因可能是5Cl2+I2+6H2O==2HIO3+10HCl
C. 由图可知氧化性的强弱顺序为Cl2>I2>IO3-
D. 途径Ⅱ中若生成1 mol I2,反应中转移的电子数为10NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学结合所学知识探究Na2O2与H2能否反应,设计装置如下,下列说法正确的是( )
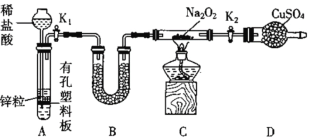
A.若D中无水硫酸铜变蓝,则说明Na2O2与H2反应生成水
B.装置B中盛放浓硫酸,目的是除去A中挥发出来的少量水蒸气
C.装置C加热前,用试管在干燥管管口处收集气体点燃,通过声音判断气体纯度
D.装置A也可直接用于二氧化锰与浓盐酸反应制取氯气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用电解乙二醛制备乙二酸(HOOC-COOH)的装置如图所示,通电后,Pt2电极上产生的氯气将乙二醛氧化为乙二酸,下列说法正确的是

A. Pt2接电源的负极,发生还原反应
B. 盐酸的作用是提供Cl-和增强导电性
C. 电路上每转移1mol电子产生45g乙二酸
D. Pt1极上的电极反应为:2H2O-4e-=== O2↑ + 4H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.高铁酸盐在能源,环保等方面有着广泛的用途。高铁酸钾(K2FeO4)不仅是一种理想的水处理剂,而且高铁电池的研制也在进行中。如图1是高铁电池的模拟实验装置:

(1)该电池放电时正极的电极反应式为_________________;若维持电流强度为lA,电池工作10 min,理论消耗Zn______g(己知F=965OOC/mol,计算结果小数点后保留一位数字)。
(2)盐桥中盛有饱和KCl溶液,此盐桥中氯离子向______(填“左”或“右”,下同)池移动;若用阳离子交换膜代替盐桥,则钾离子向______移动。
(3)图2为高铁电池和常用的高能碱性电池的放电曲线.由此可得出高铁电地的优点有______________。

Ⅱ.第三代混合动力车,可以用电动机,内燃机或二者结合推动车辆。汽车上坡或加速时,电动机提供推动力.降低汽油的消耗;在刹车或下坡时,电池处于充电状态。
(4)混合动力车的内燃机以汽油为燃料,汽油(以辛烷C8H18计)和氧气充分反应,生成1 mol 水蒸气放热550kJ;若1 g水蒸气转化为液态水放热2.5kJ,则辛烷燃烧热的热化学方程式为_____________。
(5)混合动力车目前一般使用镍氢电池,该电池中镍的化合物为正极,储氢金属(以M表示)为负极,碱液(主要为KOH)为电解质溶液。镍氢电池充放电原理示意如图,其总反应式为:
H2+2NiOOH![]() 2Ni(OH)2。
2Ni(OH)2。
根据所给信息判断,混合动力车上坡或加速时.乙电极周围溶液的pH______(填“增大”,“减小”或“不变”),该电极的电极反应式为_______________。

(6)远洋轮船的钢铁船体在海水中易发生电化学腐蚀中的______腐蚀。利用如图装置,可以模拟铁的电化学防护。

若X为碳棒,为减缓铁的腐蚀,开关K应置于______处。
若X为锌,开关K置于M处,该电化学防护法称为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法正确的有( )个
①20℃,101kPa,22.4LCl2通入足量的NaOH溶液充分反应,有NA个电子转移
②64g灼热的铜丝在硫黄蒸气里完全反应后,失去的电子数为2NA
③标准状况下,NA个NO分子和0.5NA个O2分子充分反应后气体体积为22.4 L
④7.8g Na2S与Na2O2的混合物中阴离子数大于0.1NA
⑤0℃,101kPa,含有lmol硫原子的SO2与SO3的混合物,其体积小于22.4L
⑥常温常压下,17g甲基(-14CH3)所含的中子数为9NA
A. 1 B. 2 C. 3 D. 4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有一可逆反应:2A(g)+3B(g) ![]() xC(g)+4D(g),若按下列两种配比在同温同体积的密闭容器中进行反应:①0.8 mol A+1.2 mol B+1.2 mol C+2.4 mol D②1.4 mol A+2.1 mol B+0.6 mol C+1.2 mol D达平衡后,C的质量分数相等,则方程式中x的值为( )
xC(g)+4D(g),若按下列两种配比在同温同体积的密闭容器中进行反应:①0.8 mol A+1.2 mol B+1.2 mol C+2.4 mol D②1.4 mol A+2.1 mol B+0.6 mol C+1.2 mol D达平衡后,C的质量分数相等,则方程式中x的值为( )
A. 1B. 2C. 3D. 4
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com