
����Ŀ����3�������Ϊ1 L�ĺ����ܱ������з�����Ӧ��SO2(g)��2NO(g)![]() 2NO2(g)��S(s)���ı�����I�ķ�Ӧ�¶ȣ�ƽ��ʱc( NO2)���¶ȵĹ�ϵ����ͼ��ʾ������˵����ȷ����
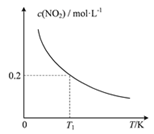
2NO2(g)��S(s)���ı�����I�ķ�Ӧ�¶ȣ�ƽ��ʱc( NO2)���¶ȵĹ�ϵ����ͼ��ʾ������˵����ȷ����
���� ��� | �¶�/K | ��ʼ���ʵ���/mol | |||
SO2 | NO | NO2 | S | ||
�� | 0.5 | 0.6 | 0 | 0 | |
�� | T1 | 0.5 | 1 | 0.5 | 1 |
�� | T2 | 0.5 | 0.2 | 1 | 1 |
A. �÷�Ӧ�Ħ�H<0
B. T1ʱ���÷�Ӧ��ƽ�ⳣ��Ϊ![]()
C. �����������������T1ʱ�ﵽƽ�⣬��ѹǿ֮��С��1:2
D. ��T2<T1���ﵽƽ��ʱ����������NO���������С��40%
���𰸡�AD
��������A������ͼ���¶����ߣ�ƽ��ʱNO2Ũ�Ƚ��ͣ�˵���¶����߿�ʹ��ѧƽ������
B��T1�¶ȷ�Ӧ�ﵽƽ��ʱc��NO2��=0.2mol/L�����ݷ�Ӧ����ʽ���㣻
C������pV=nRT�����������ݻ��ͷ�Ӧ�¶�һ������ϵ��ѹǿ����ϵ�л������������ʵ��������ȣ�
D���¶Ƚ��ͣ������ڻ�ѧ��Ӧ������У����ݷ�Ӧ����ʽ�͵�Чƽ���֪ʶ������
A������ͼ���¶����ߣ�ƽ��ʱNO2Ũ�Ƚ��ͣ�˵���¶����߿�ʹ��ѧƽ�������������ӦΪ���ȷ�Ӧ������H��0��A��ȷ��
B��T1�¶ȷ�Ӧ�ﵽƽ��ʱc��NO2��=0.2mol/L����ƽ��ʱc��SO2��=0.5mol/L-0.1mol/L=0.4mol/L��c��NO��=0.6mol/L-0.2mol/L=0.4mol/L�����Է�Ӧ�Ļ�ѧƽ�ⳣ��ΪK=c2(NO2)/c2(NO)c(SO2)=
0.22/0.42��0.4=5/8��B����
C��������������״̬����pV=nRT�����������ݻ��ͷ�Ӧ�¶�һ������ϵ��ѹǿ����ϵ�л������������ʵ��������ȣ��������൱�ڰ�0.75molSO2��1.5molNO��0.75molS��ʼ������S�ǹ��壬���ı�Ũ���̣����������з�Ӧ�ﵽƽ��ʱ������ymolSO2����ƽ��ʱ������ѹ����ΪpI/pII=(0.4+0.4+0.2+0.1)/(2y)��1/(2y)��1/2��C����
D��T2��T1�����¶Ƚ��������ڻ�ѧ��Ӧ������У��������൱����1molSO2��1.2molNO��0.5molS��ʼ��S���Ի�ѧ��Ӧ��ƽ�����Ӱ�죬Ҳ���൱�ڶ��������ѹ����ƽ�ⲻ�����ƶ�����ƽ��ʱNO���������Ϊ40%����������Ļ�ѧ��Ӧ������г̶ȱ�����I������ﵽƽ��ʱ����������NO���������С��40%��D��ȷ����ѡAD��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ǻ��ʹ�ҵ�ͻ�����������Ҫԭ�ϣ���ҵ�Ϻϳɰ�ʹ�õ�������Ҫ���Ժϳ���(CO��H2�������)����ش��������⣺
��1����ҵ�Ϻϳɰ��ķ�Ӧԭ��ΪN2(g)��3H2(g)![]() 2NH3(g) ��H �� ��֪��
2NH3(g) ��H �� ��֪��
��ѧ�� | H��H | N��N | N��H |
����/kJ��mol-1 | 436 | 945.6 | 391 |
��ѧ���ļ������γɻ����1 mol ��ѧ���ų������յ���������λΪkJ/mol��������Ӧ����H________________��
��2���������ֳ��£�N2H4������д�������ĵ���ʽ_________�������ֿ���Ϊ�����������ȼ�ϣ���������N2O4��Ӧ����N2��ˮ������
��֪��2N2H4(l)��N2O4(l)=3N2(g)��4H2O(g) ��H1
N2H4(l)��O2(g)= N2(g)��2H2O(g) ��H2
��N2(g)��2O2(g)=N2O4 (l) ��H3��_________
��3�����������������з���ȼ�ϵ���ǵ�ǰ���е�һ���ȵ㡣��ȼ�ϵ��ʹ�õĵ������Һ��KOH��Һ����װ����ͼ��ʾ��a�缫��ӦʽΪ________������ȼ�ϵ�����ı�״����6.72 L����(���������O2�������Ϊ20%)��������������NH3������Ϊ_______g��

��4���״�ȼ�ϵ��������Ӧ��Ҳ�ܹ㷺�����¶�Ϊ650���������ȼ�ϵ�����ü״���������CO2�Ļ����������Ӧ������缫����Li2CO3��Na2CO3�����������ʡ�д���õ�صĸ�����Ӧʽ______________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������ͭ�Ƚ������仯�������ճ�������Ӧ�ù㷺�����������ʵ��ش�����:
(1)�����к���һ����̼������X(Fe3C)��X�������Ŀ����и������գ������д��ԵĹ���Y����Y���ڹ����������Һ�к��еĴ�����������___��
(2)ij��Һ����Mg2+��Fe2+��Al3+��Cu2+���������ӣ������м��������NaOH��Һ���ˣ��������������ղ������պ�Ĺ���Ͷ�������ϡ�����У�������Һ��ԭ��Һ��ȣ���Һ�д������ٵ���������______________��
A.Mg2+ B.Fe2+ C.Al3+ D.Cu2+
(3)����������Ҫ��ҵ���ϣ��÷���м�Ʊ������������£�
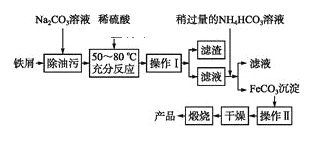
�ش���������:
�ٲ������������____���������������____����д���ڿ���������FeCO3�Ļ�ѧ����ʽ________________��
(4)��Щͬѧ��ΪKMnO4��Һ�ζ�Ҳ�ܽ�����Ԫ�غ����IJⶨ��
a.��ȡ2.850 g�̷�(FeSO4��7H2O)��Ʒ���ܽ⣬��250 mL����ƿ�ж��ݣ�
b.��ȡ25.00 mL������Һ������ƿ�У�
c.�������ữ��0.01000 mol��L-1KMnO4��Һ�ζ����յ㣬����KMnO4��Һ�����ƽ��ֵΪ20.00 mL��
�ٴﵽ�ζ��յ�ʱ������____��
��ijͬѧ��Ƶ����еζ���ʽ,���������____��(�гֲ�����ȥ)(����ĸ���)
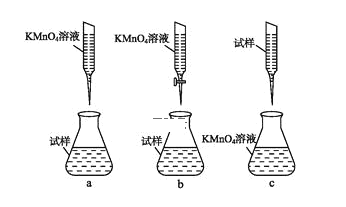
�ۼ���������Ʒ��FeSO4��7H2O����������Ϊ____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ͭ�Ͻ��Դ�ͭΪ�������һ�ֻ�������Ԫ�������ɵĺϽ�������ʹ������Ľ������ϡ�
��1����⾫��ͭ��ʵ����ʹ�õĴ�ͭ����Cu��������Zn��Ag��Au��Cu2Te�������������д����⾫��ͭʱ�����������ĵ缫��Ӧʽ__________��______________��
��2���Ӵ�ͭ������������(��Ҫ����Cu2Te)����ȡ���ڵ�һ�ֹ���������ͼ������֪TeO2���������������ˮ��������ǿ���ǿ��)
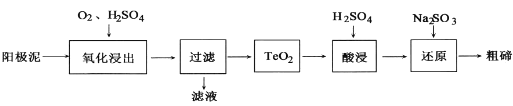
�١�����������ʱΪʹ��Ԫ�س������Ӧ������Һ��pHΪ4.5~5.0������TeO2���������H2SO4��������Һ��ȹ��������ڳ�������ȫ��ԭ����_____.
�ڡ����ˡ��õ��IJ���������____��
�ۡ���ԭ��ʱ���������ӷ���ʽ��________��
���жϴ���ϴ���ķ�����_________��
������Һ����μ��백ˮ���������ȳ�����ɫ����������ܽ��γ�����ɫ������Һ��д������ɫ�����ܽ�����ӷ���ʽ_______����������ʵ���ж�NH3��H2O��Cu2+����λ������NH3_____H2O�������������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£���100 mL pH��2������һԪ��x��y��ϡ������pH����Һ����Ĺ�ϵ����ͼ��ʾ����

A. xΪǿ�ᣬyΪ����
B. ����ϡ�͵Ľ��У�y�ĵ���̶ȼ�С
C. ϡ��ǰx��y�����ʵ���Ũ�����
D. ϡ�ͺ��x��y�ֱ�ֱ���������п��Ӧ��y�ų���������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��300��ʱ��������X������Y��0.16 mol����10 L�����ܱ������У�������Ӧ��X(g) +Y(g)![]() 2Z(g) ��H��0��һ��ʱ���ﵽƽ�⡣��Ӧ�����вⶨ���������±���
2Z(g) ��H��0��һ��ʱ���ﵽƽ�⡣��Ӧ�����вⶨ���������±���
t/min | 2 | 4 | 7 | 9 |
n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
�ش��������⣺
��1����Ӧ0~2 min Z��ƽ������v(Z)=_____________
��2�����жϸ÷�Ӧ�Ѿ��ﵽƽ��״̬����_____________
A������X������������Z�����ʵ�2��
B��������ѹǿ���ֲ���
C��������������ܶȱ��ֲ���
D�������ڸ������Ũ�ȱ��ֲ���
��3��Ҫ���������Ӧ��ת���ʣ��ɲ�ȡ�Ĵ�ʩ��_____________����дһ�֣���
��4���¶�Ϊ300��ʱ���÷�Ӧ�Ļ�ѧƽ�ⳣ��K��_______________
��5������ʼʱ��������г���X��Y��Z��0.20 mol����Ӧ����____����������������������Ӧ������У���ƽ��ʱZ���������������ƽ�����______������������������С��������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1��ȡ300mL 0.2mol/L��KI��Һ��һ����������KMnO4��Һǡ�÷�Ӧ�����ɵ����ʵ�����I2��KIO3��������KMnO4�����ʵ�������______mol��
��2����Fe��NO3��3��Һ�м���Na2SO3��Һ����Һ�����ػ�ɫ��Ϊdz��ɫ����һ���ֱ�Ϊ�ػ�ɫ����Һ�ȱ�Ϊdz��ɫ�����ӷ���ʽ��________���ֱ�Ϊ�ػ�ɫ��ԭ���������ӷ���ʽ����___________________________��
��3����100mLFeBr2��Һ��ͨ������2.24LCl2����Һ��Һ����1/4��Br- �������ɵ���Br2����ԭFeBr2��Һ��FeBr2�����ʵ���Ũ��Ϊ_________________��
��4����Al��Al2O3��Al(OH)3�Ļ����ǡ����NaOH��Һ��Ӧ����Ӧ����Һ�����ʵĻ�ѧʽ_________����Ӧ�����Һ��ͨ�����CO2����Ӧ�����ӷ���ʽΪ______��
��5����������(NF3)��һ����ɫ����ζ�����壬�������ӹ�ҵ�����Ĺؼ�ԭ��֮һ�����������ڳ�ʪ�Ŀ�������ˮ�����ܷ���������ԭ��Ӧ���䷴Ӧ�IJ����У�HF��NO��HNO3�������Ҫ��ش��������⣺
��д���÷�Ӧ�Ļ�ѧ����ʽ___________����Ӧ������0.2mol HNO3��ת�Ƶĵ�����ĿΪ_______��
��NF3��ɫ��������һ���ڿ�����й©���������ڷ��֣��жϸ�����й©ʱ��������________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ����()
![]() ���ӻ����ﺬ���Ӽ���Ҳ���ܺ����Լ���Ǽ��Լ�
���ӻ����ﺬ���Ӽ���Ҳ���ܺ����Լ���Ǽ��Լ�
![]() ��������Դ���̼������ԣ����Էǽ�����
��������Դ���̼������ԣ����Էǽ�����![]()
![]() ������Ԫ�صĻ����ﲻһ�������ӻ�����
������Ԫ�صĻ����ﲻһ�������ӻ�����
![]() �ɷǽ���Ԫ����ɵĻ�����һ���ǹ��ۻ�����
�ɷǽ���Ԫ����ɵĻ�����һ���ǹ��ۻ�����
![]() ����״̬�ܵ���Ļ����������ӻ�����
����״̬�ܵ���Ļ����������ӻ�����
![]() �ɷ�����ɵ�������һ�����ڹ��ۼ�
�ɷ�����ɵ�������һ�����ڹ��ۼ�
A. ![]() B.
B. ![]() C.
C. ![]() D.
D. ![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����л�ѧ��Ӧ�IJ�����������ͬ���칹�����
��CH3CH2CH2Br�ڼ�����Һ��ˮ�⡡�ڼױ��ڴ�����������Cl2���������ϵ�ȡ����Ӧ����2���ȶ�����NaOH�Ҵ���Һ���ȷ�Ӧ �� �ڴ����Ĵ�����������ȫ�ӳ� �������ϩ��
�ڴ����Ĵ�����������ȫ�ӳ� �������ϩ�� ��������ʵ�����Br2�����ӳɷ�Ӧ
��������ʵ�����Br2�����ӳɷ�Ӧ
A. �٢ڢ� B. �٢ڢ� C. �ڢۢ� D. �ڢۢ�
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com