
【题目】短周期主族元素 W、X、Y、Z 的原子序数依次增大,X 的质子数是 W 与 Z 的质子数之和的一半。m、n、p 是由这些元素组成的二元化合物,r 是元素 Y 的气体单质,n 为淡黄色粉末, 相关物质转化关系如图所示。室温下,0.01mol/L s 溶液 pH 为 12。下列说法误错的是
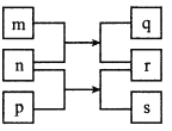
A.Z 是所在周期中原子半径最大的元素
B.简单离子半径大小:Y﹥Z﹥W
C.电负性:Y﹥X﹥W
D.n 中阴阳离子个数比为 1:1
科目:高中化学 来源: 题型:
【题目】乳酸亚铁晶体〔CH3CH(OH)COO〕2Fe·2H2O是一种很好的食品铁强化剂,可由乳酸钙与FeCl2反应制得,制备流程如下:
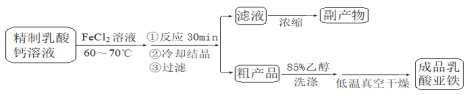
反应装置如下图所示:
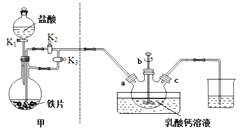
已知:①潮湿的乳酸亚铁易被氧化
②物质的溶解性:
乳酸钙:溶于冷水,易溶于热水;乳酸亚铁:溶于冷水和热水,难溶于乙醇。
请回答:
(1)装置甲的气密性检查操作为_________
(2)部分实验操作过程如下,请按正确操作顺序填入字母,其正确的操作顺序是:检查气密性![]() 按图示要求加入试剂
按图示要求加入试剂![]() 将三颈烧瓶置于水浴中
将三颈烧瓶置于水浴中![]() (____)
(____)![]() (____)
(____)![]() (____)
(____)![]() (____)
(____)![]() (____)
(____)![]() (____)
(____)![]() 开动搅拌器
开动搅拌器![]() ……
……
a.关闭K1;
b.盖上分液漏斗上口玻璃塞;
c.关闭K3,打开K2;
d.关闭K2,打开K3;
e.打开分液漏斗上口玻璃塞;
f打开K1
(3)该装置制备乳酸亚铁的优点是_________副产物为_________
(4)下列说法正确的是_________
A.装置甲中的主要仪器是球形分液漏斗和蒸馏烧瓶
B.本实验采用较大铁片而不是铁粉的主要原因是控制反应速率,防止进入三颈烧瓶的氯化亚铁过多,反应过于剧烈
C.乳酸亚铁悬浊液应从b口倒出进行抽滤,并用滤液洗涤三颈烧瓶,将洗涤液倒入布氏漏斗再次抽滤
D.粗产品的洗涤液,经蒸馏后所得的残留液,与滤液混合可提高副产物的产量
(5)在实验过程中FeCl2溶液和乳酸钙溶液混合即出现浑浊,继续在60℃-70℃下反应30分钟,静置冷却、抽滤、洗涤、低温真空干燥,得到成品,经测定得到反应温度和成品中Fe3+含量关系如图,60℃之后Fe3+含量明显较低的可能的原因是_________
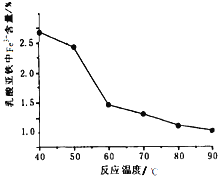
(6)有同学提出可直接用KMnO4滴定法测定样品中的Fe2+量进而计算纯度,但实验后发现结果总是大于100%,其主要原因可能是_________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水是自然界中普遍存在的一种物质,也是维持生命活动所必需的一种物质。
信息一:水的性质存在许多反常现象,如固态密度小于液态密度使冰浮在水面上,沸点相对较高使水在常温常压下呈液态等。
信息二:在20 ℃、1个大气压下,水可以结成冰,称为“热冰”(如下图):
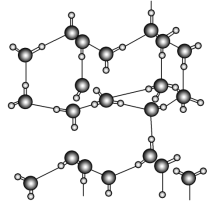
试根据以上信息回答下列问题:
(1)s轨道与s轨道重叠形成的共价键可用符号表示为ds-s,p轨道以“头碰头”方式重叠形成的共价键可用符号表示为dp-p,则H2O分子中含有的共价键用符号表示为________。
(2)下列物质熔化时,所克服的微粒间的作用与“热冰”熔化时所克服的作用类型完全相同的是________。
A 金刚石 B 干冰 C 食盐 D 固态氨
(3)已知:2H2O=H3O++OH-,H3O+的立体构型是________,H3O+中含有一种特殊的共价键是________。
(4)根据等电子原理,写出短周期元素原子形成的与H3O+互为等电子体的分子或离子________。
(5)水的分解温度远高于其沸点的原因是________________。
(6)从结构的角度分析固态水(冰)的密度小于液态水的密度的原因是_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】同温同压下,若A容器中充满气体O2和B容器中充满气体O3
(1)若所含分子总数相等,则A容器和B容器的容积之比是____。
(2)若两容器中所含原子总数相等,则A容器和B容器的容积比是___。
(3)若A容器和B容器的体积比为3∶2,则气体O2和气体O3质量之比为___,密度之比为____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、M、W五种短周期元素。X原子的质子数与电子层数相同,W原子核外电子数是M原子最外层电子数的2倍,Y、Z、M、W在周期表中的相对位置如图所示。下列说法不正确的是
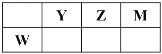
A. 原子半径:W>Y>Z>M>X
B. 热稳定性:XM>X2Z
C. 仅由X、Y、Z三种元素形成的化合物中不可能含离子键
D. WM4分子中每个原子最外层均满足8电子结构
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有一份澄清溶液,可能含有 Na+、K+、NH4+、Ca2+、Fe3+、SO42-、CO32-、SO32-、Cl-、I-中的若干种,且离子的物质的量浓度均为 0.1mol·L-1(不考虑水解和水的电离)。往该溶液中加入过量的盐酸酸化 BaCl2溶液,无沉淀生成。另取少量原溶液,设计并完成如下实验:
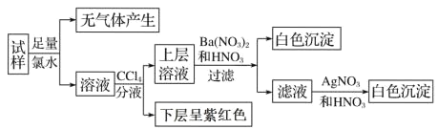
则关于原溶液的判断中不正确的是
A.是否存在 Na+、K+需要通过焰色反应来确定
B.通过 CCl4层的颜色变化,能判断出溶液中 I-肯定存在
C.试样加足量氯水无气体产生,说明溶液中 CO32-肯定不存在
D.肯定不存在的离子是 Ca2+、Fe3+、SO42-、CO32-、Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】植物可以通过光合作用在体内合成有机物,被称为生物质(以淀粉为代表),具有广阔的应用前景。已知生物质的主要转化途径及主要产物如图所示:
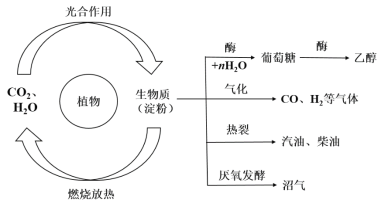
请回答:
(1)农村燃烧沼气供能的反应类型为下列的______。
A.吸热反应 B.放热反应 C.氧化还原反应 D.非氧化还原反应
(2)写出葡萄糖的化学式________________,上图由葡萄糖得到乙醇的反应中另一种气体产物的结构式为__________________。
(3)下列说法不正确的是______。
A.生物质中的能量本质上来自于太阳能
B.生物质气化产物中所含的能量既属于化学能,又属于生物质能
C.上图中生物质的所有转化均为化学反应
D.直接燃烧生物质是一种高效利用能源的方式
(4)已知18 g的葡萄糖固体被氧气完全氧化生成两种气体产物时放出热量254 kJ,写出该反应的热化学方程式_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在体积均为1.0 L的两恒容密闭容器中加入足量的相同的碳粉,再分别加入0.1 mol CO2和0.2 mol CO2,在不同温度下反应CO2(g)+C(s)![]() 2CO(g)达到平衡,平衡时CO2的物质的量浓度c(CO2)随温度的变化如图所示(图中Ⅰ、Ⅱ、Ⅲ点均处于曲线上)。下列说法正确的是
2CO(g)达到平衡,平衡时CO2的物质的量浓度c(CO2)随温度的变化如图所示(图中Ⅰ、Ⅱ、Ⅲ点均处于曲线上)。下列说法正确的是

A.反应CO2(g)+C(s) ![]() 2CO(g)的ΔS>0、ΔH<0
2CO(g)的ΔS>0、ΔH<0
B.体系的总压强p总:p总(状态Ⅱ)<2p总(状态Ⅰ)
C.体系中c(CO):c(CO,状态Ⅱ)<2c(CO,状态Ⅲ)
D.逆反应速率:v逆(状态Ⅰ)>v逆(状态Ⅲ)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】![]() 代表阿伏加德罗常数的值,下列叙述正确的是( )
代表阿伏加德罗常数的值,下列叙述正确的是( )
A.1mol ![]() 中含有
中含有![]() 个
个![]()
B.4.6g分子式为![]() 的有机物中碳氢键数目一定是
的有机物中碳氢键数目一定是![]()
C.电解精炼铜中转移1mol电子,阳极质量减少32g
D.将含0.1mol![]() 的饱和溶液滴入沸水中,形成的胶体粒子的数目少于
的饱和溶液滴入沸水中,形成的胶体粒子的数目少于![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com