
【题目】25℃时,二元酸H3PO3的pKa1、pKa2(pK=-lgK)依次为1.30、6.60,氨水的pKb为4.75。常温时,下列指定溶液中微粒物质的量浓度关系正确的是( )
A.0.1 mol·L-1NH4H2PO3溶液中:c(H3PO3)>c(NH3·H2O)>c(H+)>c(OH-)
B.0.1 mol·L-1H3PO3溶液用NaOH溶液滴定至pH=6.60:c(H2PO3-)=c(HPO32-)
C.0.1 mol·L-1H3PO3溶液用氨水滴定至pH=7.0:c(NH4+)=c(H2PO3- )+c(HPO32-)
D.0.4 mol·L-1氨水与0.2 mol·L-1NaH2PO3等体积混合(体积变化可忽略):c(NH3·H2O)<c(H2PO3-)+2c(H3PO3)+0.1 mol·L-1
【答案】BD
【解析】
A. 二元酸H3PO3的pKa1=1.3小于氨水的pKb为4.75,铵根离子的水解能力强,c(NH3·H2O)>c(H3PO3),故A错误;
B. 0.1 mol·L-1H3PO3溶液用NaOH溶液滴定至pH=6.60,ka2=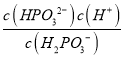 =c(H
=c(H![]() +)=10-6.60,所以c(H2PO3-)=c(HPO32-),故B正确;
+)=10-6.60,所以c(H2PO3-)=c(HPO32-),故B正确;
C. 0.1 mol·L-1H3PO3溶液用氨水滴定至pH=7.0,c(H+)=c(OH-),根据电荷守恒c(H+)+c(NH4+)=c(H2PO3- )+2c(HPO32-)+c(OH-),即:c(NH4+)=c(H2PO3- )+2c(HPO32-),故C错误;
D. 0.4 mol·L-1氨水与0.2 mol·L-1NaH2PO3等体积混合(体积变化可忽略),相当于0.1 mol·L-1Na(NH4)HPO3溶液和0.1 mol·L-1氨水等体积混合,根据电荷守恒:①c(H+)+c(NH4+)+c(Na+)=c(H2PO3- )+2c(HPO32-)+c(OH-),再由物料守恒:②c(NH4+)+c(NH3·H2O)=2c(H2PO3- )+2c(HPO32-)+2c(H3PO3),③c(Na+)=0.1 mol·L-1,②-①得c(NH3·H2O)+c(OH-)=c(H2PO3-)+2c(H3PO3)+c(Na+)+c(H+),将③代入,溶液呈碱性c(H+)<c(OH-),整理得:c(NH3·H2O)<c(H2PO3-)+2c(H3PO3)+0.1 mol·L-1,故D正确;
故选BD。


科目:高中化学 来源: 题型:
【题目】实验室用标准盐酸溶液测定某NaOH溶液的浓度,用甲基橙作指示剂,下列操作中可能使测定结果偏低的是( )
A.滴定前平视读数,滴定后仰视读数
B.滴定结束后,滴定管尖嘴处有一悬挂液滴
C.取NaOH溶液时先平视读数,后仰视读数
D.盛NaOH溶液的锥形瓶滴定前用NaOH溶液润洗2次~3次
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据氨气还原氧化铜的反应,可设计测定铜元素相对原子质量(近似值)的实验。先称量反应物氧化铜的质量m(CuO),反应完全后测定生成物水的质量m(H2O),由此计算铜元素相对原子质量。提供的实验仪器及试剂如下(根据需要可重复选用,加入的氯化铵与氢氧化钙的量足以产生使氧化铜完全还原的氨气):
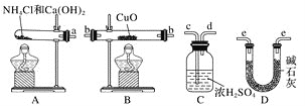
请回答下列问题:
(1)氨气还原炽热氧化铜的化学方程式为__。
(2)从所提供的仪器及试剂中选择并组装本实验的一套合理、简单的装置,按气流方向的连接顺序为(用图中标注的导管口符号表示)a→__。
(3)在本实验中,若测得m(CuO)=ag,m(H2O)=bg,则Ar(Cu)=__。
(4)在本实验中,使测定结果Ar(Cu)偏大的是__(填序号)。
①氧化铜未完全起反应 ②氧化铜不干燥 ③氧化铜中混有不反应的杂质 ④碱石灰不干燥 ⑤氯化铵与氢氧化钙混合物不干燥
(5)在本实验中,还可通过测定__和__,或__和__达到实验目的。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CH3CH2OH和 ![]() 互为同分异构体,将两种物质分别放在下列检测仪上进行检测,显示出的信号完全相同的是
互为同分异构体,将两种物质分别放在下列检测仪上进行检测,显示出的信号完全相同的是
A.李比希元素分析仪B.红外光谱仪C.核磁共振仪D.质谱仪
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(化学---选修2:化学与技术)
南海某小岛上,可利用的淡水资源相当匮乏,解放军战士为了寻找合适的饮用水源,对岛上山泉水进行分析化验,结果显示山泉水属于硬水。
(1)硬水是指含有较多______________的水,硬水加热后产生沉淀的离子方程式为:________________________________(写出生成一种沉淀物的即可) 。
(2)硬度为1°的水是指每升水含10 mg CaO或与之相当的物质(如7.1 mg MgO),已知水的硬度在8°以下的称为软水,在8°以上的称为硬水。已知岛上山泉水中c( Ca2+)=1.2×10-3 mol/L,c(Mg2+) =6×l0-4mol/L,那么此水______(填“是”或“否”)属于硬水。
(3)离子交换法是软化水的常用方法。聚丙烯酸钠是一种离子交换树脂,写出聚丙烯酸钠单体的结构简式__________________。
(4)解放军战士通常向水中加入明矾净水,请用离子方程式解释其净水原理:______________。
(5)岛上还可以用海水淡化来获得淡水。下面是海水利用电渗析法获得淡水的原理图,已知海水中含Na+、Cl-、Ca2+、Mg2+、SO42-等离子,电极为惰性电极。请分析下列问题:
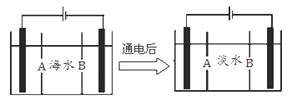
①阳离子交换膜是指___________(填A或B)。
②写出通电后阳极区的电极反应式____________,阴极区的现象是:_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲、乙都是二元固体化合物,将32g的粉末加入足量浓硝酸并加热,完全溶解得蓝色溶液,向该溶液中加入足量![]() 溶液,过滤、洗涤、干燥得沉淀
溶液,过滤、洗涤、干燥得沉淀![]() ;滤液中再滴加NaOH溶液,又出现蓝色沉淀。
;滤液中再滴加NaOH溶液,又出现蓝色沉淀。
含乙的矿石自然界中储量较多,称取一定量的乙,加入稀盐酸使其完全溶解,溶液分为A、B两等分,向A中加入足量NaOH溶液,过滤、洗涤、灼烧得到红棕色固体28g,经分析乙与红棕色固体组成元素相同,向B中加入![]() 铜粉充分反应后过滤、洗涤、干燥得固体
铜粉充分反应后过滤、洗涤、干燥得固体![]() 。
。
![]() 写出构成甲的阴离子的结构示意图______,32g甲在足量浓硝酸中反应转移的电子数为______。
写出构成甲的阴离子的结构示意图______,32g甲在足量浓硝酸中反应转移的电子数为______。
![]() 乙的化学式______;稀硫酸溶解乙的化学方程式______。
乙的化学式______;稀硫酸溶解乙的化学方程式______。
![]() 将甲在足量氧气中充分灼烧的气体产物通入一定量A溶液中,该反应的离子方程式为______,设计实验证明此步反应后的溶液中金属元素的化合价______。
将甲在足量氧气中充分灼烧的气体产物通入一定量A溶液中,该反应的离子方程式为______,设计实验证明此步反应后的溶液中金属元素的化合价______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关工业生产的叙述正确的是( )
A.合成氨生产中将NH3液化分离,可提高N2、H2的转化率,增大了反应速率
B.硫酸工业中,在接触室安装热交换器是为了利用SO3转化为H2SO4时放出的热量
C.电解饱和食盐水制烧碱采用离子交换膜法,可防止阴极室产生的C12进入阳极室
D.侯氏制碱法是将氨气和二氧化碳先后通入饱和氯化钠溶液中,制得碳酸氢钠固体,再在高温下灼烧,转化为碳酸钠固体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合成芳香炔化合物的方法之一是在催化条件下,含炔氢的分子与溴苯发生反应,如:

甲 乙 丙
根据上式,请回答:
(1)甲的分子式是___;丙能发生的反应是(选填字母)___。
a.取代反应 b.加成反应 c.水解反应 d.消去反应
(2)以苯为原料生成乙的化学方程式是____。
(3)乙与NaOH溶液反应的化学方程式_____。
(4)由丙制备 ![]() 的反应条件是_______。
的反应条件是_______。
(5)符合下列条件的丙的同分异构体有__种(不包括顺反异构)。①分子中除苯环外不含其他环状结构;②苯环上只有2个取代基,且其中一个是醛基。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某科研小组设计出利用工业废酸(l0%)来堆浸某废弃的氧化铜锌矿的方案,实现废物综合利用,如图所示。
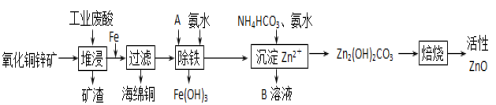
已知:各离子开始沉淀及完全沉淀时的pH如表所示。
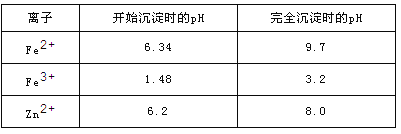
请回答下列问题:
(1)堆浸时,为了提高浸出效率可采取的措施有(写两种):___、___。
(2)物质A的作用是___,可使用下列物质中的___。
A.KMnO4 B.O2 C.H2O2 D.Cl2
(3)除铁过程中加入氨水的目的是调节溶液的pH,pH应控制在___范围之间。
(4)物质B可直接用作氮肥,则B的化学式是___。
(5)除铁后得到的Fe(OH)3可用KClO溶液在碱性环境下将其氧化得到一种高效的多功能水处理剂——K2FeO4,写出该反应的离子方程式___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com