
【题目】现代工业常以氯化钠为原料制备纯碱,部分工艺流程如下:
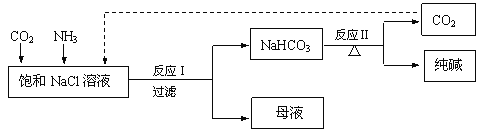
已知反应I为:NaCl + CO2 + NH3 + H2O === NaHCO3↓+ NH4Cl
(1)海水中含有大量的NaCl,以及少量的Ca2+、Mg2+、SO42等离子。
① 为得到纯净的饱和NaCl溶液,进行了如下操作。请补全操作步骤:
a.向浓缩后的海水中加入过量的氢氧化钠溶液后,过滤;
b.向滤液中加入过量___________________(填试剂名称),过滤;
c.向滤液中加入过量___________________(填试剂名称),过滤;
d.向滤液中加入足量的稀盐酸;
e.加热煮沸一段时间,得到饱和NaCl溶液。
② 步骤c中反应的离子方程式是______________________。
(2)反应II的化学方程式是_________________________。
(3)制得的纯碱中含有少量NaCl。取5.5 g纯碱样品加入足量稀硫酸,得到标准状况下1120 mL CO2。则样品中纯碱的质量分数是_________%(保留1位小数)。
【答案】BaCl2溶液或Ba(OH)2溶液Na2CO3溶液Ca2+ + CO32 === CaCO3↓,Ba2+ + CO32 === BaCO3↓2NaHCO3 ![]() Na2CO3 + CO2↑+ H2O96.4
Na2CO3 + CO2↑+ H2O96.4
【解析】(1)①加入氢氧化钠溶液的目的是为了除去Mg2+;除去SO42-用BaCl2溶液,除去Ca2+和过量的Ba2+用Na2CO3溶液,故可知步骤b中应加入BaCl2溶液或Ba(OH)2溶液,步骤c应加入过量的Na2CO3溶液;
②步骤c是加入过量的Na2CO3溶液以除去Ca2+和过量的Ba2+,故离子方程式为Ca2++CO32-═CaCO3↓、Ba2++CO32-═BaCO3↓;
(3)NaHCO3固体加热即可分解为CO2和Na2CO3和水,方程式为:2NaHCO3![]() Na2CO3+CO2↑+H2O;
Na2CO3+CO2↑+H2O;
(4)二氧化碳的物质的量n=![]() =0.05mol,而1molNa2CO3~1molCO2,故Na2CO3的物质的量为0.05mol,则Na2CO3的质量m=nM=0.05mol×106g/mol=5.3g,故纯碱的质量分数=
=0.05mol,而1molNa2CO3~1molCO2,故Na2CO3的物质的量为0.05mol,则Na2CO3的质量m=nM=0.05mol×106g/mol=5.3g,故纯碱的质量分数=![]() ×100%=96.4%。
×100%=96.4%。


 同步练习河南大学出版社系列答案
同步练习河南大学出版社系列答案 同步练习西南大学出版社系列答案
同步练习西南大学出版社系列答案 补充习题江苏系列答案
补充习题江苏系列答案 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案科目:高中化学 来源: 题型:
【题目】下列实验操作或处理事故的方法正确的是( )
A. 用分液漏斗分离乙酸乙酯和水的混合物时,水从下口放出,乙酸乙酯从上口倒出
B. 在耐高温的石英坩埚中进行熔化氢氧化钠固体的实验
C. 用干燥的pH试纸测定NaClO溶液的pH
D. 欲配制质量分数为10%的硫酸铜溶液,可准确称取10 g硫酸铜晶体溶于90 g水中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】运用所学知识,回答下列问题。
I、向硫酸铜溶液中逐滴加入KI溶液至恰好反应完全,观察到产生白色沉淀CuI,蓝色溶液变为棕色。该反应的离子方程式为__________;取一定量上述反应后的上层棕色清液于一支试管中,加入一定量的苯,振荡,此时观察到的现象是________。
II、工业上用铝土矿(主要成分为Al2O3,只含Fe2O3杂质)为原料冶炼铝的工艺流程如下:
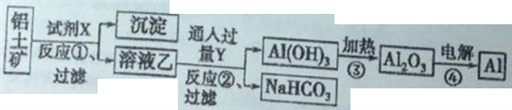
回答下列问题:
(1)上述反应是否都是氧化还原反应_________(填“是”或“否”);写出反应①的化学方程式_____。
(2)反应①后过滤的沉淀为_______,简述确定此物质中金属元素及其价态的操作过程_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学家借助太阳能产生的电能和热能,用空气和水作原料成功地合成了氨气。下列有关说法正确的是
A. 该合成中所有的电能和热能全部转化为化学能
B. 该合成氨过程不属于氮的固定
C. 空气、水、太阳能均为可再生资源
D. 断裂N2中的N≡N键会释放出能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将5.1g镁铝合金溶于70ml4mol/L硫酸中,当合金完全溶解后,再加入70ml8mol/L的NaOH溶液,得沉淀的质量为13.6g,则加入硫酸时,产生H2的物质的量为
A. 0.2mol B. 0.25mol C. 0.3mol D. 0.35mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列过程没有发生化学反应的是( )
A. 用浸泡过高锰酸钾溶液的硅藻土保鲜水果
B. 用热碱水清除炊具上残留的油污
C. 用活性炭去除冰箱中的异味
D. 用含硅胶、铁粉的透气小袋与食品一起密封包装
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上用硫铁矿石(主要成分FeS2)在沸腾炉中焙烧,经过一系列反应,得到硫酸,焙烧后的矿渣用于炼铁。其转化过程如下图所示(部分条件、反应物和产物已略去):
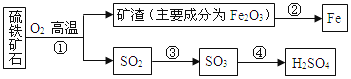
请回答下列问题:
(1)在上面转化过程中,硫元素被氧化的反应是________(填反应编号)。
(2)写出反应②中炼铁的化学方程式_____________。若用1000t含杂质28%的矿渣炼铁,理论上可得到含铁96%的生铁质量为_____________ t.
(3)写出反应①的化学方程式 ,若有12.0g FeS2参加反应,则发生转移的电子数为 。
(4)烟气中SO2的排放会造成酸雨,工业上常用Na2SO3溶液来吸收SO2以减少对环境的危害。
①常温下,将SO2通入一定体积的1.0mol·L-1Na2SO3溶液中,溶液pH不断减小。当溶液pH约为6时,吸收SO2的能力显著下降,此时溶液中c(SO32-)的浓度是0.2mol·L-1,则溶液中c(HSO3-)是 mol·L-1。用化学平衡原理解释此时溶液显酸性的原因 。
②向①中pH约为6时的吸收液中通入足量O2充分反应。取反应后溶液10mL与10mLBaCl2溶液混合,欲使混合时能生成沉淀,所用BaCl2溶液的浓度不得低于 mol·L-1。[已知25℃时,Ksp(BaSO3)=5.48×10-7, Ksp(BaSO4)= 1.08×10-10]
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列金属防腐的措施中,使用牺牲阳极的阴极保护法的是( )
A. 水中的钢闸门连接电源的负极 B. 金属护栏表面涂漆
C. 汽车底盘喷涂高分子膜 D. 地下钢管连接镁块
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在下列氧化还原反应中,水既不作氧化剂又不作还原剂的是()
①2Na+2H2O=2NaOH+H2↑
②2H2O![]() 2H2↑+O2↑
2H2↑+O2↑
③2F2+2H2O=O2+4HF
④3NO2+H2O=2HNO3+NO
⑤NaH+H2O=NaOH+H2↑
⑥2Na2O2+2H2O=4NaOH+O2↑
A. ③④⑥ B. ②③⑤ C. ①②③⑤ D. ④⑥
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com