
【题目】化学反应 A2+B2 = 2AB 的能量变化如图所示,则下列说法正确的是( )

A.该反应是吸热反应
B.断裂1molA-A键和1molB-B键能放出x kJ 的能量
C.2molAB的总能量高1mol A2和1molB2和的总能量
D.断裂2molA-B键需要吸收y kJ的能量
科目:高中化学 来源: 题型:
【题目】已知图①一④的相关信息,下列相应叙述正确的是
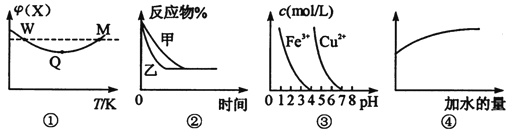
A.图①表示向恒容密闭容器中充入X和Y发生反应:2X(g)+Y(g)![]() 3Z(g) △H<0,W点X的正反应速率等于M点X的正反应速率
3Z(g) △H<0,W点X的正反应速率等于M点X的正反应速率
B.图②表示压强对可逆反应A(g)+2B(g)![]() 3 C(g)+D(s)的影响,乙的压强比甲压强小
3 C(g)+D(s)的影响,乙的压强比甲压强小
C.据图③,若要除去CuSO4溶液中的Fe3+,可加入NaOH溶液至pH在4左右
D.常温下,稀释0.1 mol·L-1Na2CO3溶液,图④中的纵坐标可以表示溶液中HCO3-的数目
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验方案中,能达到相应实验目的的是
实验方案 |
|
|
|
|
目的 | A.比较乙醇分子中羟基氢原子和水分子中氢原子的活泼性 | B.除去乙烯中的二氧化硫 | C.制银氨溶液 | D.证明碳酸酸性强于苯酚 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,在20mL0.1mol/L HR 溶液中滴加0.1000mol/LNaOH溶液,混合溶液的PH与所加NaOH溶液体积的关系如图所示。下列推断正确的是

A. ①、②、③三点中,③对应的溶液中c水(H+)·c水(OH-)最大
B. HR溶液中只存在H+、R-、OH-、H2O四种微粒
C. ②点溶液中一定存在c(Na+)>c(R-)>c(H+)=c(OH-)
D. NaR的水解常数Ka和水解程度:③>②>①
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:图甲是由某温度下![]() 、
、![]() 分别在溶液中达到沉淀溶解平衡后,改变溶液pH,金属阳离子浓度的变化图.图乙是常温下向100mL
分别在溶液中达到沉淀溶解平衡后,改变溶液pH,金属阳离子浓度的变化图.图乙是常温下向100mL![]() 溶液中逐滴加入
溶液中逐滴加入![]() 溶液,混合溶液的pH变化图.如图所示与推测的结论相符的是
溶液,混合溶液的pH变化图.如图所示与推测的结论相符的是
图甲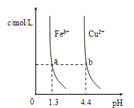 图乙
图乙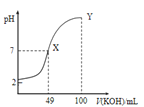
A.由图甲知:![]()
B.由图甲知:a、b点溶液中![]() ,b点的大
,b点的大
C.由图乙知:HA为强酸
D.由图乙知:Y点对应的溶液中![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】往含Cl-和I-的稀溶液中滴入AgNO3溶液,沉淀的质量与加入AgNO3溶液体积的关系如图所示。下列说法正确的是
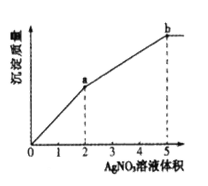
A.KSP (AgCl) < KSP (AgI)
B.c( Cl- ) :c( I-) =3:2
C.m( AgCl ) :m( AgI ) =" 2" :3
D.a~b段产生黄色沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】测得某温度下0.5mol·L-1 HNO2(亚硝酸)溶液的pH约为2。
(1)写出HNO2的电离方程式___。
(2)将溶液加水稀释至10倍后,c(NO2-)___(填“增大”、“减小”或“不变”),n(H+)___(填“增大”、“减小”或“不变”),pH区间范围是___。
A.1~2 B.2~3 C.3~4 D.4~5
(3)分别取同浓度同体积的盐酸与亚硝酸,以同样的操作与足量NaOH溶液反应,测得反应溶液的最高温度盐酸要高于亚硝酸,说明可能的原因___。
(4)0.1mol·L-1 NaNO2溶液pH___7(填“>”、“<”或“=”),溶液中含有___种分子,溶液中c(Na+)___c(NO2-)(填“>”、“<”或“=”),下列措施能提高溶液中c(OH-)的是___。
A.适当升高温度 B.增加压强 C.加水 D.加入NH4Cl固体 E.加入Na2CO3固体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Bodensteins 研究了反应 2HI(g)![]() I2(g)+ H2(g),某温度下,上述反应中,正反应速率为υ正=k正c2(HI),逆反应速率为υ逆=k逆c(I2)·c(H2),,其中k正、k逆为速率常数,根据以上内容得出的结论,不正确的是
I2(g)+ H2(g),某温度下,上述反应中,正反应速率为υ正=k正c2(HI),逆反应速率为υ逆=k逆c(I2)·c(H2),,其中k正、k逆为速率常数,根据以上内容得出的结论,不正确的是
A.反应物浓度越大,正反应速率越大
B.生成物浓度越大,逆反应速率越大
C.该反应的平衡常数K =k正/k逆
D.速率常数的大小与反应程度无关系
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在实验室中,可以有如下两种方法制备二氧化氯(ClO2),回答下列问题
Ⅰ.![]()
Ⅱ.![]()
(1)NaClO3中Cl的化合价为______________。
(2)Ⅰ中还原产物是______________。
(3)Ⅱ的离子方程式为__________________________________________,若反应中有0.1mol电子转移,则产生的ClO2气体在标准状况下的体积为_____________L。
(4)二氧化氯是一种在水处理等方面有广泛应用的高效安全消毒剂。“有效氯含量”可用来衡量含氯消毒剂的消毒能力,其定义是:每克含氯消毒剂的氧化能力(得失电子数)相当于多少克C12的氧化能力(Cl均转化为Cl-)。ClO2的有效氯含量为_________________(计算结果保留两位小数)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com