
【题目】下列叙述正确的是![]()
①含有大量![]() 的溶液中,
的溶液中,![]() 、
、![]() 、
、![]() 、
、![]() 可以大量共存
可以大量共存
②![]() 的
的![]() 溶液中,
溶液中,![]() 、
、![]() 、
、![]() 、
、![]() 可以大量共存
可以大量共存
③向![]() 溶液中加入过量的稀氨水,发生反应:
溶液中加入过量的稀氨水,发生反应:![]()
④加入铝粉能放出![]() 的溶液中,
的溶液中,![]() 、
、![]() 、
、![]() 、
、![]() 一定能够大量共存
一定能够大量共存
⑤用NaOH溶液除去铝条表面的氧化膜:![]()
⑥依据铝热反应原理,能发生反应
⑦向明矾溶液中加入过量![]() 溶液,发生反应:
溶液,发生反应:![]()
⑧常温下,铝可溶于过量浓硝酸,也可溶于过量NaOH溶液
A.⑤⑦B.②③⑤C.④⑤⑥D.②⑦⑧
【答案】A
【解析】
①含有大量![]() 的溶液显碱性,
的溶液显碱性,![]() 、OH-和
、OH-和![]() 不能大量共存,故①错误;
不能大量共存,故①错误;
②![]() 的
的![]() 溶液中,Al3+和
溶液中,Al3+和![]() 发生相互促进水解生成氢氧化铝沉淀和二氧化碳,不能大量共存,故②错误
发生相互促进水解生成氢氧化铝沉淀和二氧化碳,不能大量共存,故②错误
③氢氧化铝不溶于氨水,向![]() 溶液中加入过量的稀氨水生成氢氧化铝,发生反应:Al3++3NH3H2O=Al(OH)3↓+3NH4+,故③错误
溶液中加入过量的稀氨水生成氢氧化铝,发生反应:Al3++3NH3H2O=Al(OH)3↓+3NH4+,故③错误
④加入铝粉能放出![]() 的溶液可能为酸性,也可能为碱性,酸性条件下,
的溶液可能为酸性,也可能为碱性,酸性条件下,![]() 和
和![]() 发生氧化还原反应,碱性条件下,
发生氧化还原反应,碱性条件下,![]() 和OH-结合形成沉淀,一定不能够大量共存,故④错误;
和OH-结合形成沉淀,一定不能够大量共存,故④错误;
⑤氧化铝为两性氧化物,既可与强酸反应,又可与强碱反应,用NaOH溶液除去铝条表面的氧化膜:![]() ,故⑤正确;
,故⑤正确;
⑥依据铝热反应原理,金属铝可与比铝活泼性差的金属氧化物反应,置换出活泼性差的金属单质,镁比铝活泼,铝和氧化镁不能发生铝热反应,故⑥错误;
⑦向明矾溶液中加入过量![]() 溶液,发生反应:
溶液,发生反应:![]() ,故⑦正确;
,故⑦正确;
⑧铝可溶于过量NaOH溶液,浓硝酸具有强氧化性,常温下,能使铝发生钝化,反应无法进行,故⑧错误;
答案选A。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】我国科学家合成了一种新的化合物,其结构式如图所示。该物质中 W、X、Y、Z、M是短周期中常见元素,且原子序数依次增大;已知M元素原子核外电子总数是Y元素原子核外 电子总数的两倍。下列说法中错误的是
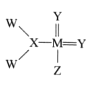
A.由X和Y两种元素形成的化合物有多种
B.W和Z元素位于周期表中同一主族
C.元素的非金属性强弱顺序为:Z>Y>X
D.Y、M元素的气态氢化物沸点高低为:Y>M
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将4 mol A气体和2 mol B气体在2 L的容器中混合并在一定条件下发生如下反应:2A(气)+B(气)![]() 2C(气)。若经2 s(秒)后测得C的浓度为0.6 mol·L-1,现有下列几种说法:
2C(气)。若经2 s(秒)后测得C的浓度为0.6 mol·L-1,现有下列几种说法:
①用物质A表示的反应平均速率为0.3 mol·L-1·s-1
②用物质B表示的反应的平均速率为0.6 mol·L-1·s-1
③2s时物质A的转化率为70%
④2s时物质B的浓度为0.7 mol·L-1
其中正确的是:
A.①③B.①④C.②③D.③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】矿盐主要成分是NaCl,还含有![]() 等其他可溶性杂质离子。下列有关说法正确的是
等其他可溶性杂质离子。下列有关说法正确的是
A.用酚酞试液可鉴别饱和食盐水和饱和纯碱溶液
B.工业上通过电解氯化钠溶液制备金属钠和氯气
C.室温下,AgCl在水中的溶解度小于在食盐中的溶解度
D.由矿盐生成食盐,除去![]() 最合适的试剂是
最合适的试剂是![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质性质的叙述一定不正确的是
A. 向FeCl2溶液中滴加NH4SCN溶液,溶液显红色
B. KAl(SO4) 2·12H2O溶于水可形成 Al(OH)3胶体
C. NH4Cl与Ca(OH)2混合加热可生成NH3
D. Cu与FeCl3溶液反应可生成CuCl2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定量的铜粉加入到0.5 L 0.3 mol·L-1 Fe2(SO4)3和0.1 mol·L-1 H2SO4的混合溶液中,铜粉完全溶解后,得到溶液X。下列说法正确的是( )
A.溶液X中Cu2+与Fe2+的物质的量之比为2∶1
B.向溶液X中加入足量铁粉,充分反应后,铁粉质量减少11.2 g
C.向溶液X中滴加KSCN溶液,未变红色,则加入铜粉质量为12.8 g
D.向溶液X中加入0.18 L 5 mol·L-1 NaOH溶液可使溶液中的金属离子完全沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A是一种分子量为28的气态烃,现以A为主要原料合成一种具有果香味的物质E,其合成路线如右图所示

请回答下列问题:
(1)写出A的结构简式________。
(2)B、D分子中的官能团名称分别是_____、_______。
(3)写出反应①的化学方程式: ____________ ; 反应类型:___________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】100℃的纯水KW=10-12,在该温度下pH均为11的NaOH和NaCN溶液中,由水电离出的c(OH-)之比为( )
A.1:1B.10-10:1C.11:3D.10-8:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各项叙述中,正确的是![]()
A.N、P、As的电负性随原子序数的增大而增大
B.价电子排布为![]() 的元素位于第四周期第ⅤA族,是p区元素
的元素位于第四周期第ⅤA族,是p区元素
C.2p和3p轨道形状均为哑铃形,能量也相等
D.镁原子由![]() 时,原子释放能量,由基态转化成激发态
时,原子释放能量,由基态转化成激发态
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com