
����Ŀ��ѧ��Ԫ����������֮��ijͬѧ��̽����̼����Ԫ�طǽ����Ե����ǿ�����������'ʵ�飺
�ش��������⣺
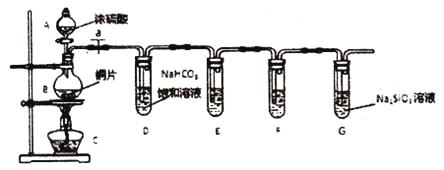
��1����д��ʾ�������ƣ�A_________��B___________��
��2��ʵ�鲽�裺����������________����ҩƷ��a��Ȼ�����Ũ���ᣬ���ȡ���ƿ�з�Ӧ�Ļ�ѧ����ʽΪ___________________________________��
��3������̽����
���Թ�D�з�����Ӧ�����ӷ���ʽ��_________________________��
����ͬѧ����װ��E����ʢƷ����Һ��ɫ�����Ա仯��F����ʢ����ʯ��ˮ����ǣ��ݴ��϶���Ԫ�صķǽ�����ǿ��̼������ͬѧ��ͬ��Ĺ۵㣬��������_______________________________��
��װ��G�г��ֵ�ʵ������Ϊ______________������֤��̼Ԫ�صķǽ�����ǿ�ڹ�Ԫ�ء�
���𰸡���Һ©�� Բ����ƿ ���װ�õ������� Cu+2H2SO4(Ũ)![]() CuSO4+ SO2��+2H2O SO2+2HCO3- = SO32-+ H2O+CO2���� SO2+HCO3-=HSO3-+CO2�� ��������������������Ӧˮ���������ǿ��̼���˵����ķǽ�����ǿ �а�ɫ��������
CuSO4+ SO2��+2H2O SO2+2HCO3- = SO32-+ H2O+CO2���� SO2+HCO3-=HSO3-+CO2�� ��������������������Ӧˮ���������ǿ��̼���˵����ķǽ�����ǿ �а�ɫ��������
��������
��1������װ��ͼ��֪A�Ƿ�Һ©����B��Բ����ƿ��
��2��ʵ�鲽�裺��������������װ����������μӷ�Ӧ������Ӧ�ü��װ�õ������ԡ���ҩƷ��a��Ȼ�����Ũ���ᣬ���ȡ���ƿ�з�Ӧ�Ļ�ѧ����ʽΪCu+2H2SO4(Ũ)![]() CuSO4+ SO2��+2H2O��
CuSO4+ SO2��+2H2O��
��3������������H2SO3>H2CO3������SO2����ͨ�뵽����NaHCO3��Һ���Թ�D�У�������Ӧ�����ӷ���ʽ��SO2+2HCO3- = SO32-+ H2O+CO2���� SO2+HCO3-=HSO3-+CO2����
����ͬѧ����װ��E����ʢƷ����Һ��ɫ�����Ա仯��F����ʢ����ʯ��ˮ����ǣ��ݴ��϶���Ԫ�صķǽ�����ǿ��̼������ͬѧ��ͬ��Ĺ۵㣬����������������������������Ӧˮ���������ǿ��̼���˵����ķǽ�����ǿ��
���������ԣ�H2CO3>H2SiO3�����ҹ���������ˮ������װ��G�лᷢ����Ӧ��CO2+Na2SiO3+H2O=Na2CO3+H2SiO3�������ֵ�ʵ������Ϊ�а�ɫ�������ɣ�����֤��̼Ԫ�صķǽ�����ǿ�ڹ�Ԫ�ء�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��25��ʱ��Fe(OH)2��Cu(OH)2�ı�����Һ�У����������ӵ����ʵ���Ũ�ȵĸ�����[һlg c(M2+)]����ҺpH�ı仯��ϵ��ͼ��ʾ����֪���¶��£�Ksp[Cu(OH)2]2]������˵����ȷ���� �� ��

A. b�߱�ʾFe(OH)2������Һ�еı仯��ϵ����Ksp[Fe(OH)2]=10-15.1
B. ��Fe(OH)2��Cu(OH)2��������ʱ����Һ�У�C(Fe2+)��C(Cu2+)��1��104.6
C. ��X���Ӧ�ı�����Һ�м�������NaOH����ת��ΪY���Ӧ����Һ
D. ��ȥCuSO4��Һ�к��е�����Fe2+���ɼ�������Cu0
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��(1)��һ�������£�28.80g��������A��1.20molCl2��ɷ�Ӧ������1.20molAClx����x=__________����Aԭ�Ӻ�����������������������Aԭ�Ӻ���������Ϊ__________ ����ԭ�ӽṹʾ��ͼΪ____________��
(2)���а���3.4g���ڱ�״���������Ϊ____________�����е�ԭ�ӵ���ĿΪ_____ ��������ȫ������ˮ�����500mL��Һ������Һ�����ʵ���Ũ��Ϊ______________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ͭ��Ʒ�к���Zn��Ag��Au�����ʣ���ͼ��ʾ����CH3OH-����ȼ�ϵ�ص������ͭ��Һ���պϵ��K���е�⡣����˵���в���ȷ���ǣ� ��
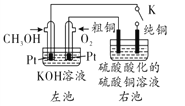
A. ��ظ�����ӦʽΪCH3OH -6e-+8OH-=CO32-+ 6H2O
B. ͨ��һ��ʱ���Ag��Au���ʽ��������ڵ��۵ײ�
C. ����ͭ�缫��������6.4g����ͭ�缫���ش���6.4g
D. ���������ҳش�ͭ�ʹ�ͭ�ֱ�Ϊ����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1�����������У�����ǿ����ʵ���___������������ʵ���__�����ڷǵ���ʵ���__��������ţ�
�ٰ��� �ڴ����� ������ �ܴ��� �����ᱵ ������� ���Ҵ�
��2��һ�������£�������Һ���ڵ���ƽ�⣺CH3COOH![]() CH3COO����H����H��0
CH3COO����H����H��0
�����з����У���ʹ0.10mol��L��1������Һ��CH3COOH����ƽ�������Ƶ���___��
a����������0.10mol��L��1��ϡ���� b������
c����ˮϡ����0.010mol��L��1 d����������������
����֪��25��ʱ�������������ĵ���ƽ�ⳣ���ֱ�Ϊ�����K��1.75��10��5�������K1��1.54��10��2 K2��1.02��10��7����25��ʱ����ͬŨ�ȴ������������Һ������ǿ����CH3COOH___H2SO3(�����������������)��
��25��ʱ����0.10mol��L��1CH3COOH��Һ�м����������ᣬʹ��Һ��[OH��]=5.0��10��13mol��L��1�������Һ��pH��__������֪��lg2=0.3��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������(��Ҫ�ɷ�ΪAl2O3��������������)����ȡ����ԭ�ϡ���ȡ���Ĺ����������£�
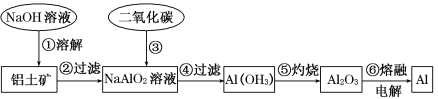
(1)�������ӷ���ʽ��ʾ���Ϲ��������еڢٲ���Ӧ��_____________________��
(2)д�����Ϲ��������еڢ۲���Ӧ�Ļ�ѧ����ʽ��___________________________��
(3)���ڢٲ�����������ᣬ������Ӧ�����ӷ���ʽΪ_________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��CuSO4��һ����Ҫ����ԭ�ϣ����Ʊ����й�������ͼ��ʾ��
��1����Ҫ����ͼ��ʾ��Ũ���������Ʋ����������Ҫ��1mol/L��ϡ����480ml����Ҫ������Ũ��������Ϊ______ml��
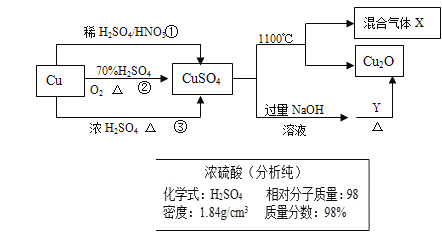
��2�����Ƹ�ϡ�������õ��IJ�������������������Ͳ���ձ����_______��__________��
��3�����в�����ʹ������ҺŨ��ƫ�͵��� _________��
A. ����ת��������ƿ��û��ϴ���ձ�
B. δ��ȴ�����¾�ת��������ƿ
C. ����ƿ�д�����������ˮ
D. ����ʱ���ӿ̶� E.��ȡŨ����ʱ��Ͳ������������ˮ
��4����ȡ����ͭ��;���٢ڢ��У�;��_________�ܸ��õ�������ɫ��ѧ��˼�롣
��5������1000ml 0.1mol/L������ͭ��Һ������������ƽ��ȡ________g������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ȤС����̽��һ����ʧ��˵���������θ�����Ŀ���ҩƬ����Ч�ɷ֡����ȣ��������ϵ�֪������ҩͨ��������������ɣ�������Ч�ɷ�Ϊ̼�����ơ�������þ������������̼����е�һ�ֻ��֡�Ȼ�����������ʵ�飺
��.����Ƭ����ҩƬ��ĥ��װ��һ֧�Թ��С�
��.����Թ��м���������ᣬ������ɫ���壮���˺�õ���ɫ��Һ��
��.�ò�˿պȡ��������������Һ���ھƾ������������գ���ɫ���档
��.�����������Һ�еμ�NaOH��Һ��������ɫ������
��ش�
(1)���в�����ɫ��������ӷ���ʽ��____________��
(2)��ͬѧ��ʵ����жϸÿ���ҩƬ��һ������������������ͬѧ��Ϊ����������ͬѧ�жϵ�������________�����ǣ���ͬѧ���ʵ��V����̽����ȡʵ����еİ�ɫ��������һ֧�Թ��У��μ�������NaOH��Һ�����������ܽ⣬��Ӧ�����ӷ���ʽ��__________��
(3)ͨ������ʵ�飬�ó��Ľ����ǣ��ÿ���ҩƬ����Ч�ɷ�Ϊ__________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ߴ��ȵ������ǵ��͵����ǽ������ϣ��ֳ����뵼�������ϣ����ķ��ֺ�ʹ��������������һ���������������ֲ��Ͽ������з����Ʊ���
SiO2![]() Si(��)
Si(��)![]() SiHCl3
SiHCl3![]() Si(��)������˵����ȷ����(����)
Si(��)������˵����ȷ����(����)
A.����ٵĻ�ѧ����ʽΪSiO2��C![]() Si��CO2��
Si��CO2��
B.����١��ڡ�����ÿ���ɻ�Ӧ1 mol Si��ת��4 mol����
C.����������������ᷴӦ�����費��������ᷴӦ
D.SiHCl3(�е�33.0 ��)�к���������SiCl4(�е�67.6 ��)��ͨ������(�����)���ᴿSiHCl3
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com