
 某课外小组利用如右图装置进行相关实验,请回答下列问题:
某课外小组利用如右图装置进行相关实验,请回答下列问题:| 10 |
| 16 |
| ||


 一课四练系列答案
一课四练系列答案 黄冈小状元满分冲刺微测验系列答案
黄冈小状元满分冲刺微测验系列答案 新辅教导学系列答案
新辅教导学系列答案 阳光同学一线名师全优好卷系列答案
阳光同学一线名师全优好卷系列答案科目:高中化学 来源: 题型:
| A、将二氧化碳通人硅酸钠溶液以证明碳酸的酸性比硅酸强 |
B、如图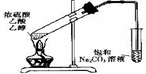 装置中,导管不能伸人液面的原因是产物易溶于水 装置中,导管不能伸人液面的原因是产物易溶于水 |
| C、用碱石灰可干燥氯气 |
| D、用普通玻璃棒蘸取溶液做焰色反应以证明溶液含有Na十 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 元素 | 信息 |
| B | 其单质在常温下为双原子分子,与A可形成分子X,X的水溶液呈碱性 |
| D | 其氧化物具有两性 |
| E | 元素原子最外层比次外层少2个电子 |
| C、F | 两种元素的原子最外层共有13个电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 某无色溶液中可能含有Mg2+、NH4+、K+、Al3+、SO42-、CO32-、Cl-等离子.现进行如下实验:①取10mL该溶液于试管中,滴加Ba(NO3)2溶液,加稀硝酸酸化后过滤得到6.99g白色沉淀;②另取10mL该溶液于试管中,滴加NaOH溶液产生白色沉淀,当沉淀增加到一定量后开始产生气体(必要时可加热),最后沉淀完全溶解,并且随NaOH溶液的加入,沉淀和气体物质的量变化如图所示.下列说法不符合事实的是( )
某无色溶液中可能含有Mg2+、NH4+、K+、Al3+、SO42-、CO32-、Cl-等离子.现进行如下实验:①取10mL该溶液于试管中,滴加Ba(NO3)2溶液,加稀硝酸酸化后过滤得到6.99g白色沉淀;②另取10mL该溶液于试管中,滴加NaOH溶液产生白色沉淀,当沉淀增加到一定量后开始产生气体(必要时可加热),最后沉淀完全溶解,并且随NaOH溶液的加入,沉淀和气体物质的量变化如图所示.下列说法不符合事实的是( )| A、根据图中数据计算实验中使用的NaOH溶液的浓度为1 mol?L-1 |
| B、根据信息分析该溶液中焰色反应呈紫色的离子的物质的量浓度为1 mol?L-1 |
| C、该溶液中NH4+、Al3+、SO42-三种离子的物质的量之比为2:1:3 |
| D、另取一定量该溶液滴加一定量Ba(OH)2溶液,不可能Al3+和SO42-同时完全沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、配制前,用研钵把重铬酸钾研磨得越细越好 |
| B、把重铬酸钾粉末加到热水中,充分搅拌,使其溶解 |
| C、配制时,选用大容器的玻璃仪器(如 干燥器等) |
| D、在充分搅拌下把浓硫酸慢慢加入重铬酸钾溶液中 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CH4 |
| B、C2H4 |
| C、C4H4 |
| D、C3H6 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在紫外线、饱和(NH4)2SO4溶液、CuSO4溶液、福尔马林等作用下,蛋白质均会发生变性 |
| B、在一定条件下,氨基酸之间能发生反应,合成更复杂的化合物(多肽) |
| C、为检验皂化反应进行程度,取几滴反应液,滴入装有热水的试管中,震荡,若有油滴浮在液面上,说明油脂已完全反应 |
| D、检验淀粉在稀硫酸催化条件下水解产物的方法是:取适量水解液于试管中,加入少量新制Cu(OH)2悬浊液,加热煮沸,观察是否出现红色沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①②③④⑤ | B、①②③④ |
| C、①③⑤ | D、②④⑤ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com