
【题目】实验室要配制100mL、10molL-1的NaCl溶液,试回答下列各题:
(1)经计算,应该用托盘天平称取NaCl固体___g。
(2)配制溶液时一般可分为以下几个步骤:①称量②计算③定容④移液⑤洗涤⑥溶解其正确的操作顺序为(填编号)___。
(3)容量瓶上需标有以下5项中的___
①温度 ②浓度 ③容量 ④压强 ⑤刻度线
A.①②④ B.③⑤⑥ C.①③⑤ D.②④⑥
(4)若用NaCl固体配制溶液,下列仪器中,不需要用到的是___。(填序号)
A.蒸发皿 B.100mL容量瓶 C.烧杯 D.胶头滴管 E.药匙 F.托盘天平 G.玻璃棒
(5)下列错误操作会导致所得溶液偏低的是___(多项,填序号)。
A.定容时仰视容量瓶刻度线区
B.容量瓶中原有少量蒸馏水
C.定容后,把容量瓶倒置摇匀后发现液面低于刻度线,便补充几滴水至刻度处
D.配制好溶液后,容量瓶未塞好,酒出一些溶液
【答案】58.5 ②①⑥④⑤③ C A AC
【解析】
(1)根据m=nM=cVM计算;
(2)配制一定物质的量浓度溶液的步骤为:计算、称量、溶解、转移、洗涤、定容,据此排序;
(3)容量瓶上标有刻度线、温度、容量,据此分析判断;
(4)若用NaCl固体配制溶液,需用药匙取药品、托盘天平称量药品、烧杯溶解药品、玻璃棒搅拌和引流、胶头滴管定容、100mL容量瓶配制溶液,据此判断不需要的仪器;
(5)根据c=![]() 知,如果n偏小或V偏大都导致配制溶液浓度偏低,据此分析判断。
知,如果n偏小或V偏大都导致配制溶液浓度偏低,据此分析判断。
(1)应该用托盘天平称取NaCl固体的质量m=cVM=10mol/L×0.1L×58.5g/mol=58.5g,故答案为:58.5;
(2)配制一定物质的量浓度溶液的步骤为:计算、称量、溶解、转移、洗涤、定容,所以配制溶液时步骤②①⑥④⑤③,故答案为:②①⑥④⑤③;
(3)容量瓶上标有温度、容量和刻度线,故选C;
(4)若用NaCl固体配制溶液,需用药匙取药品、托盘天平称量药品、烧杯溶解药品、玻璃棒搅拌和引流、胶头滴管定容、100mL容量瓶配制溶液,所以不需要的仪器是蒸发皿,故选A;
(5)A.定容时仰视容量瓶刻度线,会导致溶液的体积偏大,配制溶液的浓度偏低,故A正确;B.容量瓶中原有少量蒸馏水,不影响溶液的体积和溶质的物质的量,配制的溶液浓度无影响,故B错误;C.定容后,把容量瓶倒置摇匀后发现液面低于刻度线,便补充几滴水至刻度处,导致溶液的体积偏大,配制溶液的浓度偏低,故C正确;D.配制好溶液后,容量瓶未塞好,洒出一些溶液,溶液的浓度不变,故D错误;故选AC。


 教材全解字词句篇系列答案
教材全解字词句篇系列答案科目:高中化学 来源: 题型:
【题目】三效催化剂是最为常见的汽车尾气催化剂,其催化剂表面物质转化的关系如图所示,下列说法正确的 ( )
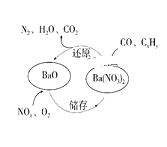
A.在转化过程中,氮元素均被还原
B.依据图示判断催化剂不参与储存和还原过程
C.还原过程中生成0.1mol N2,转移电子数为0.5 NA
D.三效催化剂能有效实现汽车尾气中CO、CxHy、NOx三种成分的净化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关化学反应速率、化学反应限度的说法中,正确的是( )
A.反应C(s)+H2O(g)![]() CO(g)+H2(g),增加碳的用量可加快反应速率
CO(g)+H2(g),增加碳的用量可加快反应速率
B.用铁片与稀硫酸反应制H2,改用 98%的浓硫酸可加快生成H2的速率
C.反应2SO2(g)+O2(g)![]() 2SO3(g)在密闭容器中进行,压缩容器体积,反应速率增大
2SO3(g)在密闭容器中进行,压缩容器体积,反应速率增大
D.可逆反应达到化学平衡状态时,正、逆反应的速率相等且都为0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫代硫酸钠(Na2S2O3)可用作分析试剂、基准试剂、还原剂、除氯剂等。
Ⅰ、实验室制备硫代硫酸钠装置图如下。

(1)仪器B的名称是________。
(2)写出装置B制备Na2S2O3的化学反应方程式____________________________。
(3)NaOH溶液的作用是____________________________________。
Ⅱ、测硫代硫酸钠样品纯度步骤如下
①称取Ⅰ中制得硫代硫酸钠样品8.0g配成250mL溶液
②从①中量取20.00mL溶液于锥形瓶中
③用0.lmol·L-1标准碘液滴定,实验测得数据如下
滴定前读数(mL) | 滴定后读数(mL) | 待测液体积(mL) | |
实验一 | 1.20 | 21.00 | 20.00 |
实验二 | 0.40 | 19.20 | 20.00 |
实验三 | 0.50 | x | 20.00 |
(4)该滴定时,向锥形瓶中加入1至2滴淀粉液作指示剂,则达到滴定终点的判断标准是______________。
(5)x读数如图所示,则x=________,根据所测的数据计算该硫代硫酸钠样品纯度为_______________。(已知I2+2Na2S2O3=2NaI+Na2S4O6)
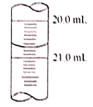
(6)若步骤①中量取20.00mL硫代硫酸钠溶液时,未用硫代硫酸钠溶液润洗滴定管,则测得样品的纯度将______________(填“偏大”或“偏小”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素X、Y在周期表中的相对位置如图所示,且已知X基态原子的价电子排布为nsnnpn+1,下列说法不正确的是( )
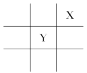
A. X元素的电负性大于YB. X元素的第一电离能大于Y
C. X在周期表中位于第二周期第ⅢA族D. 原子半径Mg>Y
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】自然界中铝元素主要存在于铝土矿(主要成分为Al2O3、FeO、Fe2O3、SiO2)中,铝的单质及其化合物在生产、生活、科研等领域应用广泛。工业上用铝土矿制备铝的某种化合物的工艺流程如下:
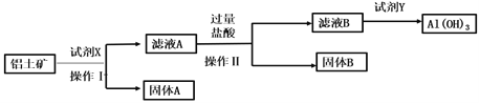
下列说法错误的是( )
A.在实验室实施操作Ⅰ需要的玻璃仪器是漏斗、烧杯、玻璃棒
B.为使铝元素全部转化为Al(OH)3,每一步操作的试剂均需过量
C.将试剂X与操作Ⅱ的试剂过量盐酸互换,也可制得Al(OH)3
D.固体A的主要成分是FeO和Fe2O3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】依据图中氮元素及其化合物的转化关系,回答问题:
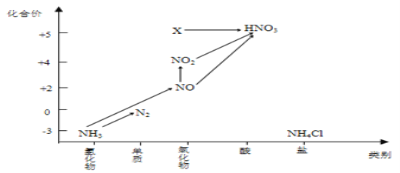
(1)该图利用“______和核心元素的_____是研究物质性质的两个重要角度”建立。
(2)实验室常用NH4Cl与Ca(OH)2制取氨气,该反应的化学方程式为________。
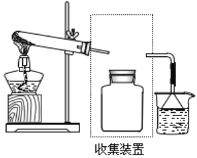
(3)若要收集一瓶氨气,请在横线上把图虚框内连接装置图不全的部分画出。_____
![]()
(4)工业上以NH3、空气、水为原料生产硝酸的工艺流程简图如图所示:
![]()
写出NH3→NO的化学方程式__________________________________。
(5)图中,X的化学式为_______,将X转化为HNO3属于______________反应(填“氧化还原”或“非氧化还原”)反应。
(6)若要将NH3→N2,从原理上看,下列试剂可行的是________(填序号)。
A.O2 B.Na C.NH4Cl D.NO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】汽车尾气无害化处理反应为2NO(g)+2CO(g)![]() N2(g)+2CO2(g) ΔH<0。下列说法正确的是
N2(g)+2CO2(g) ΔH<0。下列说法正确的是
A. 升高温度可使该反应的正反应速率增大,逆反应速率减小
B. 增大压强,可以使NO和CO完全转为为无污染的N2和CO2,而消除污染
C. 该反应反应物总能量小于生成物总能量
D. 使用高效催化剂可降低反应的活化能,增大活化分子百分数,反应速率增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com