
【题目】从元素化合价和物质类别两个角度研究物质的性质,是一种行之有效的方法。以下是铁元素组成物质的二维图的部分信息。
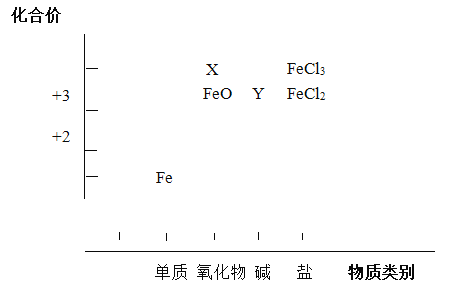
(1)分别写出X、Y的化学式______、______。
(2)写出FeO与稀硫酸反应的化学方程式____________。
(3)FeCl2既具有氧化性也具有还原性,分别写出体现其氧化性、还原性的反应的离子方程式。
| 离子方程式 |
氧化性 | ____________________ (一个即可) |
还原性 | ____________________ (一个即可) |
(4)某同学预测Fe3+可以与S2-发生反应,为验证预测,他结合资料信息,选择了两种试剂进行实验,确认了反应的发生。
资料:部分硫化物的溶解性表(室温)
阴离子 阳离子 | S2- |
Na+ | 溶 |
Fe3+ | 不 |
Fe2+ | 不 |
选取的试剂是______和______;可能发生的两种不同原理的反应的离子方程式是:_________、__________。
【答案】Fe2O3 Fe(OH)2 FeO+H2SO4=FeSO4+H2O Zn+ Fe2+= Zn2++ Fe 2Fe2++Cl2= 2Fe3++2Cl- FeCl3 Na2S 2Fe3++3S2-=Fe2S3↓ 2Fe3++S2-= 2Fe2++S↓或者2Fe3++3S2-= 2FeS+S↓
【解析】
由图可知Fe的化合价为+2、+3价,则 X的化学式Fe2O3;Y的化学式 Fe(OH)2。答案:Fe2O3;Fe(OH)2。
(2) FeO与稀硫酸反应的化学方程式为:FeO+H2SO4=FeSO4+H2O。答案:FeO+H2SO4=FeSO4+H2O。
(2)FeCl2既具有氧化性也具有还原性,在Zn+ Fe2+= Zn2++ Fe 这个反应中,Fe2+ 表现氧化性; 在2Fe2++Cl2= 2Fe3++2Cl-反应中Fe2+ 表现还原性; 所以FeCl2既有氧化性又有还原性。答案: Zn+ Fe2+= Zn2++ Fe ;2Fe2++Cl2= 2Fe3++2Cl-。
(3)预测Fe3+可以与S2-发生反应,可以通过FeCl3 和Na2S反应,可能发生的反应方程式为:2Fe3++3S2-=Fe2S3↓;2Fe3++S2-= 2Fe2++S↓或者2Fe3++3S2-= 2FeS+S↓ 。答案: FeCl3;Na2S 2Fe3++3S2-=Fe2S3↓ ;2Fe3++S2-= 2Fe2++S↓或者2Fe3++3S2-= 2FeS+S↓。


科目:高中化学 来源: 题型:
【题目】(1)0.5molCH4的质量是_______________g,在标准状况下的体积为_______________L;含有约______________个氢原子。
(2)将标准状况下22.4 L的HCl溶于水配成200 mL的溶液,所得溶液的物质的量浓度为_____
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯气是一种重要的工业原料,某研究性学习小组查阅资料得知,漂白粉与硫酸反应可制取氯气,化学方程式为:Ca(ClO)2+CaCl2+2H2SO4![]() 2CaSO4+2Cl2↑+2H2O。他们利用该反应设计如图所示装置制取氯气并验证其性质的实验。(B中装淀粉KI溶液,C中装Na2SO3溶液,D中装FeCl2溶液)
2CaSO4+2Cl2↑+2H2O。他们利用该反应设计如图所示装置制取氯气并验证其性质的实验。(B中装淀粉KI溶液,C中装Na2SO3溶液,D中装FeCl2溶液)

回答下列问题:
(1)该实验中A部分的装置是______(填标号)。

(2)装置B中产生的现象为______。
(3)请设计实验验证装置C中的Na2SO3已被氧化______。
(4)写出D装置中发生反应的离子方程式______。
(5)该实验存在明显的缺陷,请你提出改进的方法______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海洋植物,如海带、海藻中含有丰富的碘元素,碘元素以碘离子的形式存在。实验室里从海带中提取碘的流程如下:
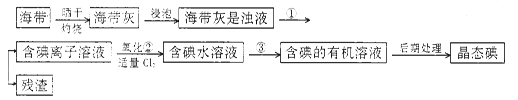
(1)指出提取碘的过程中有关的实验操作名称:①____________________;③______________。
若实验②中采用酸性条件下加入双氧水,则有关反应的离子方程式_________________________________。
(2)提取碘的过程中,可供选择的有关试剂是___________。
A.甲苯,酒精B.四氯化碳,苯C.汽油,乙酸D.汽油,甘油
(3)含碘的有机溶液后期处理得到晶态碘需要进行的操作为___________;
最后,晶态碘在___________里聚集。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】咖啡酸苯乙酯![]() 是一种天然抗癌药物。在一定条件下能发生如下转化。
是一种天然抗癌药物。在一定条件下能发生如下转化。
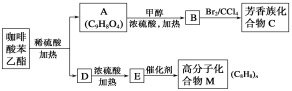
请回答下列问题:
(1)A分子中的官能团是_______________________________。
(2)高分子化合物M的结构简式是_______________________________。
(3)写出A→B反应的化学方程式:_________________________。A→B的反应类型为__________。
(4)E→M的反应方程式为_____________________;B→C的反应类型为__________。
(5)A的同分异构体有很多种,其中同时符合下列条件的同分异构体有________种。
①苯环上只有两个取代基 ②能发生银镜反应③能与碳酸氢钠溶液反应 ④能与氯化铁溶液发生显色反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应mA(g)+nB(g)![]() pC(g)+qD(g)的v-t图象如下右图,如若其它条件不变,只是在反应前加入合适的催化剂,则其v-t图象如图:①a1>a2 ②a1<a2 ③b1>b2 ④b1<b2 ⑤t1>t2 ⑥t1=t2 ⑦两图中阴影部分面积相等 ⑧右图中阴影部分面积更大,以上说法中正确的是
pC(g)+qD(g)的v-t图象如下右图,如若其它条件不变,只是在反应前加入合适的催化剂,则其v-t图象如图:①a1>a2 ②a1<a2 ③b1>b2 ④b1<b2 ⑤t1>t2 ⑥t1=t2 ⑦两图中阴影部分面积相等 ⑧右图中阴影部分面积更大,以上说法中正确的是
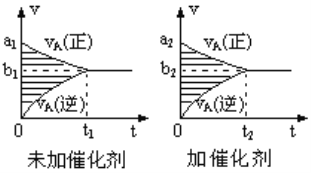
A. ②③⑤⑧ B. ①④⑥⑧ C. ②④⑤⑦ D. ①③⑥⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】核磁共振氢谱是研究有机物结构的有力手段之一,例如乙醛的结构简式为CH3-CHO,在核磁共振氢谱中有两个峰,其峰面积之比为3:1。
(1)结构式为![]() 的有机物,在核磁共振氢谱上吸收峰的面积之比为 __________;
的有机物,在核磁共振氢谱上吸收峰的面积之比为 __________;
(2)某含氧有机物,其质谱图中最大质荷比为46.0,碳的质量分数为52.2%,氢的质量分数为13.0%,核磁共振氢谱中只有一个吸收峰,则该有机物的相对分子质量为___________,其结构简式是 _________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室中可用如图装置来制取干燥的氨气。

(1)写出A处发生反应的化学方程式_____________________________________。
(2)U形管B中所放的药品是__________________。
(3)实验室制取下列气体时,与实验室制取氨气的气体发生装置相同的是______________(填字母)。
A. 氢气 B.氧气C.氯气 D.二氧化碳
(4)试管C的管口处要放置一小团棉花,放置棉花的作用是___________________________。
(5)资料显示:“氨气可在纯氧中点燃,反应生成氮气和水”。为验证此事实,某同学设计了一个实验方案,装置见D。请写出该反应的化学方程式__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上常用硫铁矿(FeS2)焙烧去硫后的烧渣(主要成分为Fe2O3、FeO、SiO2,不考虑其他杂质)制取七水合硫酸亚铁(FeSO4·7H2O),流程如下:
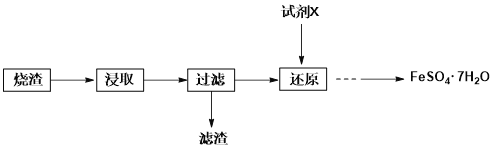
(1)试剂X可能为______________。
A.双氧水 B.酸性高锰酸钾 C.浓硫酸 D.SO2
(2)从还原后溶液中得到产品,应进行的操作是___________、____________、过滤、洗涤、干燥。
(3)七水合硫酸亚铁(FeSO4·7H2O)在医学上常用作补血剂。某课外小组通过以下实验方法测定某补血剂中亚铁离子的含量。
步骤a:取10片补血剂样品除去糖衣、研磨、溶解、过滤,将滤液配成500 mL溶液;
步骤b:取上述溶液25mL于锥形瓶中,逐渐滴加0.0500 mol/L的酸性KMnO4溶液,至恰好完全反应,记录消耗的酸性KMnO4溶液的体积(假定药品中其他成分不与酸性KMnO4反应);
步骤c:重复步骤b2~3次,平均消耗酸性KMnO4溶液20.00mL。
已知:5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O,则该补血剂中亚铁离子的含量为_____mg/片。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com