
【题目】为证明铜丝与稀硝酸反应生成的确实是NO,某同学设计了一套装置(如图1所示),有关该实验叙述不正确的是

A. 为保证实验效果,反应开始前,稀硝酸可加到与两侧胶塞相平的位置。
B. 利用该装置可控制反应随时停止或继续反应
C. 生成的气体可利用图2装置来收集
D. 长玻璃管的作用可防止稀硝酸溢出
科目:高中化学 来源: 题型:
【题目】下列保存试剂的方法中,错误的是( )
A.漂粉精保存在烧杯中B.新制的氯水保存在棕色瓶中,避光
C.氢氧化钠溶液保存在带木塞的试剂瓶D.碘单质保存在棕色瓶中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A.物质在溶解时,若达到饱和状态,则该物质不再溶解
B.晶体失去结晶水,一定是风化的结果
C.从饱和溶液中结晶析出的晶体都含有结晶水
D.某饱和溶液冷却而析出晶体后,该溶液仍为饱和溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用如图所示装置进行下列四组实验,不能得到相应实验结论的是
选项 | ① | ② | ③ | 实验结论 |
|
A | 浓硫酸 | Na2SO3 | 酸性KMnO4溶液变浅 | SO2有还原性 | |
B | 浓盐酸 | KMnO4 | FeBr2溶液变为黄色 | 氧化性:Cl2 >Br2 | |
C | 稀硫酸 | 碳酸钠 | CaCl2溶液无明显变化 | CO2不与CaCl2反应 | |
D | 浓硫酸 | 蔗糖 | 溴水褪色 | 浓硫酸具有脱水性、强氧化性 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了除去MgCl2酸性溶液中的Fe3+ , 可在加热搅拌的条件下加入一种试剂过滤后,再加入适量的盐酸,这种试剂是( )
A.NH3H2O
B.NaOH
C.Na2CO3
D.MgCO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】聚酰亚胺是重要的特种工程材料,已广泛应用在航空、航天、纳米、液晶、激光等领域.某聚酰亚胺的合成路线如图(部分反应条件略去). 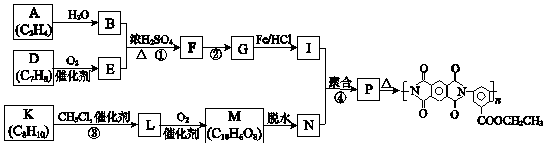
已知: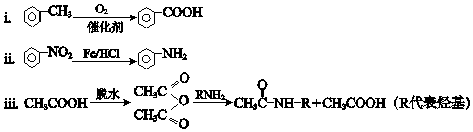
(1)A所含官能团的名称是 .
(2)①反应的化学方程式是 .
(3)②反应的反应类型是 .
(4)I的分子式为C9H12O2N2 , I的结构简式是 .
(5)K是D的同系物,核磁共振氢谱显示其有4组峰,③的化学方程式是 .
(6)1mol M与足量的NaHCO3溶液反应生成4mol CO2 , M的结构简式是 .
(7)P的结构简式是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各元素的原子或离子,各电子层都达到稳定结构的是( )
A.He、Ne、Ar、CaB.Be、B、C、Si
C.F、Cl、S、OD.Na+、F-、Cl-、Al3+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高炉炼铁过程中发生的主要反应为 ![]() Fe2O3(s)+CO(g)=
Fe2O3(s)+CO(g)= ![]() Fe(s)+CO2(g)已知该反应在不同温度下的平衡常数如下:
Fe(s)+CO2(g)已知该反应在不同温度下的平衡常数如下:
温度/℃ | 1000 | 1150 | 1300 |
平衡常数 | 4.0 | 3.7 | 3.5 |
请回答下列问题:
(1)该反应的平衡常数表达式K= , △H0(填“>”、“<”或“=”);
(2)在一个容积为10L的密闭容器中,1000℃时加入Fe、Fe2O3、CO、CO2各1.0mol,反应经过10min后达到平衡.求该时间范围内反应的平均反应速率v(CO2)=、CO的平衡转化率=:
(3)欲提高(2)中CO的平衡转化率,可采取的措施是 .
A.减少Fe的量
B.增加Fe203的量
C.移出部分CO2
D.提高反应温度
E.减小容器的容积
F.加入合适的催化剂.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com