
【题目】根据题目要求填空:
(1)有SO2、CH3COOH、BaSO4、CH3CH2OH四种物质,属于非电解质的是_________、__________;属于强电解质的是________________;属于弱电解质的是_______________。
(2)写出下列物质在水溶液中电离的方程式
①NaHCO3:__________________________________________;
②HClO:_______________________________________________。
(3) 写出MgCl2的电子式 ___________________________
【答案】SO2 CH3CH2OH BaSO4 CH3COOH NaHCO3=Na+ + HCO3- HClO![]() H++ClO-
H++ClO- ![]()
【解析】
(1)电解质是在水溶液或熔化状态下能够导电的化合物,非电解质是指在水溶液里和熔化状态下都不能导电的化合物,SO2 和CH3CH2OH属于非电解质,强电解质首先属于电解质,强电解质在水溶液里能够完全电离成离子,BaSO4属于强电解质;而弱电解质不能完全电离成离子,CH3COOH属于弱电解质,故答案为:SO2、CH3CH2OH;BaSO4;CH3COOH。
(2)①NaHCO3是强电解质,能够完全电离,电离方程式为:NaHCO3=Na+ + HCO3-,故答案为:NaHCO3=Na+ + HCO3-;
②HClO是弱电解质,部分发生电离,电离方程式为:HClO![]() H++ClO-,故答案为:HClO
H++ClO-,故答案为:HClO![]() H++ClO-。
H++ClO-。
(3)MgCl2由离子键构成,电子式为:![]() ,故答案为:
,故答案为:![]() 。
。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】从如图所示的两种微粒结构示意图中,不正确的是( )

A. 它们的核外电子数相同
B. 甲表示阴离子,乙表示原子
C. 它们属于同种元素
D. 它们的核外电子层数相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在某温度下可逆反应:Fe2(SO4)3+6KSCN![]() 2Fe(SCN)3+3K2SO4达到平衡状态后加入少量下列何种固体物质,该平衡几乎不发生移动( )
2Fe(SCN)3+3K2SO4达到平衡状态后加入少量下列何种固体物质,该平衡几乎不发生移动( )
A. NH4SCN B. K2SO4 C. NaOH D. FeCl3·6H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】298K时,在FeCl3酸性溶液中加少量锌粒后,Fe3+立即被还原成Fe2+。据此某学习小组设计如图所示的原电池装置。下列有关说法正确的是
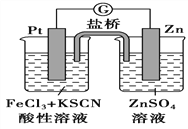
A. 正极反应为Zn-2e-=Zn2+
B. 该电池总反应为3Zn+2Fe3+=2Fe+3Zn2+
C. Pt电极上有气泡出现
D. 左烧杯中溶液的红色变浅
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学反应N2+3H2 ![]() 2NH3的能量变化下图所示,该反应的热化学方程式是
2NH3的能量变化下图所示,该反应的热化学方程式是
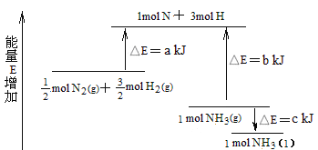
A.N2(g)+3H2(g) ![]() 2NH3(l) △H = 2(a-b+c) kJ/mol
2NH3(l) △H = 2(a-b+c) kJ/mol
B.N2(g)+3H2(g) ![]() 2NH3(l) △H = 2(a-b-c) kJ/mol
2NH3(l) △H = 2(a-b-c) kJ/mol
C.![]() N2(g)+
N2(g)+![]() H2(g)
H2(g) ![]() NH3(l) △H = (b+c-a) kJ/mol
NH3(l) △H = (b+c-a) kJ/mol
D.![]() N2(g)+
N2(g)+![]() H2(g)
H2(g) ![]() NH3(g) △H = (a+b) kJ/mol
NH3(g) △H = (a+b) kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z为短周期元素,X原子的质子数等于Z与Y的质子数之和;Z与Y位于同一周期,Y元素形成气态氢化物水溶液呈碱性,非金属Z的一种固体单质可导电。回答下列问题:
(1)Y在周期表中的位置是第_____周期、第____族,其原子结构示意图为_______.Y与Z之间形成的化学键属于___________(填离子键或共价键)。
(2) X、Y、Z三种元素中原子半径最大的是_______(填元素符号);X单质既可与盐酸反应,又可溶于氢氧化钠溶液,产生的气体为________(填分子式),该气体与Y单质反应的化学方程式______。
(3)Z的最价氧化物的电子式为_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定量的Cl2通入一定浓度的苛性钾溶液中,两者恰好完全反应(已知反应过程放热),生成物中有三种含氯元素的离子,其中ClO-和ClO3-两种离子的物质的量(n)与反应时间(t)的变化示意图如右图所示。下列说法正确的是( )
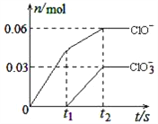
A. 苛性钾溶液中KOH的物质的量是0.09mol
B. ClO3-的生成是由于氯气的量的多少引起的
C. 在酸性条件下ClO-和ClO3-可生成Cl2
D. 反应中转移电子的物质的量是0.21mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com