
【题目】下列叙述正确的是( )
A. 聚乙烯不能使酸性KMnO4溶液褪色
B. ![]() 和
和 ![]() 均是芳香烃,
均是芳香烃,![]() 既是芳香烃又是芳香化合物
既是芳香烃又是芳香化合物
C. ![]() 和
和![]() 分子组成相差一个—CH2—,因此是同系物关系
分子组成相差一个—CH2—,因此是同系物关系
D. 分子式为C2H6O的红外光谱图上发现有C-H键和C-O键的振动吸收,由此可以初步推测有机物结构简式为C2H5-OH
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】“西气东输”是西部开发的重点工程,这里的“气”是指天然气,其主要成分是甲烷。
(1)甲烷分子具有________________结构,其结构式是_________________。
(2)通常情况下,甲烷比较稳定,但在特定条件下,甲烷也会发生某些反应,请写出甲烷在光照条件下与氯气反应生成一氯甲烷的化学方程式________________________,该反应属于____________(填反应类型)。
(3)在一定条件下甲烷也可用于燃料电池。如图是甲烷燃料电池的原理示意图:
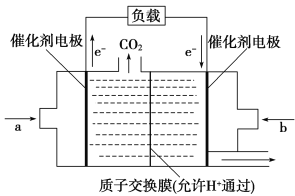
若正极的反应式为O2+4H++4e-=2H2O,则负极反应式为________________________________;该电池工作过程中,H+的移动方向为从________到________(填“左”或“右”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2007年诺贝尔化学奖授予善于做“表面文章”的德国科学家格哈德·埃特尔。他的成就之一是证实了气体在固体催化剂表面进行的反应,开创了表面化学的方法论。在汽车尾气净化装置里,气体在催化剂表面吸附与解吸作用的过程如图所示。下列说法正确的是
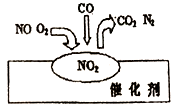
A.NO2是该过程的最终产物
B.NO 和O2必须在催化剂表面才能反应
C.汽车尾气的主要污染成分是CO2和NO
D.该催化转化的总反应方程式为:2NO+O2+4CO![]() 4CO2+N2
4CO2+N2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫和氮及其化合物在生产生活中应用广泛。请回答:
(1)蔗糖炭化的过程中,会发生反应:C+2H2SO4(浓) ![]() CO2↑+2SO2↑+2H2O,若生成0.5 mol CO2,则转移电子的物质的量是______mol,蔗糖炭化过程体现了浓H2SO4的____(选填:脱水性、吸水性、氧化性、酸性)。
CO2↑+2SO2↑+2H2O,若生成0.5 mol CO2,则转移电子的物质的量是______mol,蔗糖炭化过程体现了浓H2SO4的____(选填:脱水性、吸水性、氧化性、酸性)。
(2)实验室有一瓶放置很久的Na2SO3固体药品,小明同学想设计一个实验验证这瓶药品有没有变质?请你帮助他设计一个实验______________________________________。
(3)Cl2和SO2均可以使品红溶液褪色,将二者等体积混合通入品红,发现红色不褪去,用化学方程式解释其原因__________________________________________________。
(4)工业上可以通过氮气和氢气在一定条件下合成氨气。下列关于氨气的性质和用途描述正确的是____________。
A.氨气易液化,液氨可作制冷剂 B.可用排水法收集氨气
C.氨气是一种无色无味的气体 D.向氨水中滴加酚酞,溶液变红
(5)氨气在一定条件下还可以被氧气所氧化,请写出化学方程式_____________________
(6)实验室检验试管里氨气是否收集满的方法是___________________(写出一种即可)。
(7)25.6 g Cu与含2 mol/L的HNO3和1mol/LH2SO4的200mL混合酸充分反应,反应后收集到的气体在标准状况下的体积为___________________(假设HNO3还原产物为NO)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应不属于加成反应的是
A.CH2=CH2+HCl![]() CH3CH2ClB.2CH3CH3+5O2
CH3CH2ClB.2CH3CH3+5O2![]() 2CO2+6H2O
2CO2+6H2O
C.CH2=CH2+H2![]() CH3CH3D.CH2=CH2+Br2―→CH2BrCH2Br
CH3CH3D.CH2=CH2+Br2―→CH2BrCH2Br
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】体育竞技中服用兴奋剂既有失公平,也败坏了体育道德。某种兴奋剂的结构简式如图所示。有关该物质的说法中正确的是 ( )

A. 该物质与苯酚属于同系物,遇FeCl3溶液呈紫色
B. 能使酸性KMnO4溶液褪色,证明其结构中存在碳碳双键
C. 1mol该物质分别与浓溴水和H2反应时最多消耗Br2和H2分别为10mol和7mol
D. 该分子中的所有碳原子可能共平面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把1molCH4和一定量Cl2组成的混合气体通入量筒中,将此量筒倒立在盛有饱和食盐水的水槽中,放在光亮处,回答下列问题:

(1)片刻后量筒中的现象:①量筒内气体的黄绿色变浅,②量筒内壁上出现_______________,③量筒内________________________________________。
(2)在反应结束后,量筒内的产物最多的是________,空间构型呈正四面体的产物为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“84消毒液”广泛应用于杀菌消毒,其有效成分是NaClO。实验小组制备消毒液,并利用其性质探索制备碘水的方法。
资料:i.HClO的电离常数为Ka=4.7×10-8;
H2CO3的电离常数为K1=4.3×10-7、K2=5.6×10-11。
ii.碘的化合物主要以I-和IO3-的形式存在,IO3-+5I-+6H+=3I2+3H2O。
iii.碘单质能与I-反应:I2+I-![]() I3-(I3-低浓度时显黄色,高浓度时为棕色)。
I3-(I3-低浓度时显黄色,高浓度时为棕色)。
Ⅰ.制备消毒液(夹持装置略)
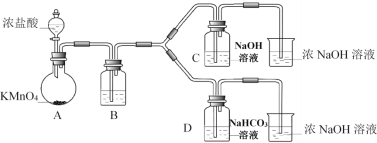
(1)制备NaClO消毒液的装置是__________(填C或D)。
(2)制备完成后,向C装置的溶液中添加NaOH、Na2SiO3等物质,得到与某品牌成份相同的消毒液,用平衡移动原理解释NaOH的作用___________________。
(3)结合资料i,写出D中反应的化学方程式______________________。
Ⅱ.利用消毒液的性质探究碘水的制备方法
将某品牌“84消毒液”稀释10倍,各取100mL于三个烧杯中,设计如下实验方案制备碘水:
方案 | 操作 | 现象 | 反应后加淀粉溶液 |
1 | 烧杯1溶液中加入9gKI固体 | 溶液为橙黄色 | …… |
2 | 烧杯2溶液中加入9gKI固体再加入1mo/L盐酸10mL | 溶液颜色快速加深,呈紫红色 | 变蓝 |
3 | 烧杯3溶液中加入少量KI固体(小于0.5g) | 振荡后溶液保持无色 | 不变蓝 |
(4)对比不同方案的实验现象,得出制取碘水的最佳方法要关注的因素是________。
(5)针对烧杯3“滴加淀粉溶液不变蓝”的原因,提出两种假设:
假设1:过量的NaClO将反应生成的I2氧化为IO3-。
设计实验证实了假设1成立。NaClO氧化I2生成IO3-的离子方程式是_____________。
假设2:生成的I2在碱性溶液中不能存在。
设计实验a证实了假设2成立,实验a的操作及现象是______________________。
(6)某小组检验烧杯3所得溶液中含IO3-:取烧杯3所得无色溶液少许,加入稀硫酸酸化的KI溶液,反应后再滴加淀粉溶液,发现溶液变蓝。该实验方案能否证明烧杯3所得溶液中存在IO3-,说明理由______________________。
(7)预测烧杯1反应后加淀粉溶液的实验现象,结合方程式说明预测依据________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应![]() ,在容积固定的密闭容器中达到平衡状态的标志是( )
,在容积固定的密闭容器中达到平衡状态的标志是( )
①单位时间内生成![]() 的同时生成
的同时生成![]()
②单位时间内生成![]() 的同时生成
的同时生成![]()
③用![]() 表示的反应速率之比为
表示的反应速率之比为![]() 的状态
的状态
④混合气体的颜色不再改变的状态
⑤混合气体的密度不再改变的状态
⑥混合气体的压强不再改变的状态
⑦混合气体的物质的量不再改变的状态
A.①④⑥⑦B.②③⑤⑦C.①③④⑤D.全部
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com