
【题目】碳族元素包括碳、硅、锗![]() 、锡
、锡![]() 、铅等,它们的单质及化合物广泛应用于我们生活的各个领域。锗和锡曾被用于半导体材料,铅被用来制造蓄电池。碳族元素在化合物中只有铅以低价形式存在时较稳定,其他元素在化合物中都是以高价形式存在比较稳定。
、铅等,它们的单质及化合物广泛应用于我们生活的各个领域。锗和锡曾被用于半导体材料,铅被用来制造蓄电池。碳族元素在化合物中只有铅以低价形式存在时较稳定,其他元素在化合物中都是以高价形式存在比较稳定。
请回答下列问题:
(1)实验室用单质锡粉制取少量二氯化锡溶液,制取和保存的方法是![]() 用文字叙述
用文字叙述![]() ________。
________。
(2)铅有多种氧化物,写出四氧化三铅与浓盐酸反应的离子方程式:________。
(3)二氧化铅在空气中加强热会得到一系列铅的其他氧化物。若把![]() 二氧化铅加强热,当固体的质量变为
二氧化铅加强热,当固体的质量变为![]() 时,写出反应的化学方程式:________。
时,写出反应的化学方程式:________。
 教材全解字词句篇系列答案
教材全解字词句篇系列答案科目:高中化学 来源: 题型:
【题目】某甲烷燃料电池构造示意图如图所示,关于该电池的说法不正确的是
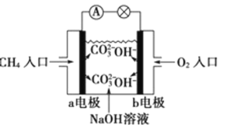
A.应该甲烷燃料电池的总反应:CH4+2O2=CO2+2H2O
B.正极的电极反应是:O2+2H2O+4e-=4OH-
C.a极是负极,发生氧化反应
D.甲烷燃料电池是环保电池
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在NH3和NH4Cl存在条件下,以活性炭为催化剂,用H2O2氧化CoCl2溶液来制备化工产品[Co(NH3)6]Cl3,下列表述正确的是
A. [Co(NH3)6]Cl3中Co的化合价是+3B. H2O2 的电子式:![]()
C. NH3和NH4Cl化学键类型相同D. 中子数为32,质子数为27的钴原子:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A和B均为钠盐的水溶液,A呈中性,B呈碱性并具有氧化性。下述为相关实验步骤和实验现象。请回答:
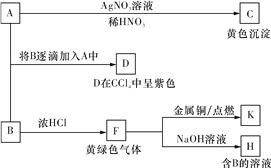
(1)写出C、D的化学式或分子式:__________、____________。
(2)指出D中所含元素在周期表中的位置________________,指出K的水溶液由稀到浓的颜色变化________________。
(3)将SO2气体通入D溶液,D溶液变为无色,生成两种强酸。写出该反应的化学方程式:________________________________________________________________________。
(4)F与粗硅加热生成__________(填分子式),该物质经蒸馏提纯后在1 100 ℃下与氢气反应生成高纯硅,写出后一步骤反应的化学方程式:_____________________________。
(5)0.25 mol F缓慢通入含有0.1 mol FeBr2、0.1 mol FeI2的混合溶液中,充分反应,试用一个离子方程式表示总反应:__________________________________________。
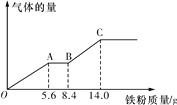
(6)某稀硫酸和稀硝酸的混合溶液100 mL,将其平均分成两份。向其中一份中逐渐加入铜粉,最多能溶解9.6 g铜粉;向另一份中逐渐加入铁粉,产生气体的量随铁粉质量的变化关系如图所示(假设硝酸的还原产物为NO气体)。则原混合溶液中NO3-的物质的量为__________,硫酸的物质的量浓度为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关①100mL 0.1 mol/L![]() 、②100mL 0.1 mol/L
、②100mL 0.1 mol/L![]() 两种溶液的叙述不正确的是
两种溶液的叙述不正确的是
A.溶液中水电离出的![]() 个数:②>①B.溶液中阴离子的物质的量浓度之和:②>①
个数:②>①B.溶液中阴离子的物质的量浓度之和:②>①
C.①溶液中:![]() D.②溶液中:
D.②溶液中:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知高能锂离子电池的总反应式为2Li+FeS===Fe+Li2S,LiPF6·SO( CH3)2为电解质,用该电池为电源电解含镍酸性废水并得到单质Ni的实验装置如图所示。下列说法不正确的是( )
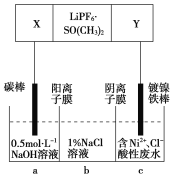
A.电极Y应为Li
B.电解过程中,b中NaCl溶液的物质的量浓度将不断减小
C.X极反应式为FeS+2Li++2e-===Fe+Li2S
D.若将图中阳离子膜去掉,将a、b两室合并,则电解反应总方程式发生改变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组模拟光合作用,采用电解CO2和H2O的方法制备CH3CH2OH和O2装置如图所示。下列说法不正确的是

A. 铂极为阳极,发生氧化反应
B. 电解过程中,H+由交换膜左侧向右侧迁移
C. 阴极的电极反应式为2CO2+12H++12e-====CH3CH2OH+3H2O
D. 电路上转移2mol电子时铂极产生11.2LO2(标准状况)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、X均为中学化学常见的物质。它们之间存在如下图所示转化关系(图中反应条件略去)填写下列空白:
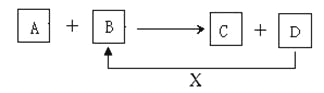
(1)若A为金属铝,B为氧化铁,写出反应A+B→C+D的一种用途______
(2)若A为两性氢氧化物, B为NaOH溶液,写出反应A+B→C+D的离子方程式________________。
(3)若A为金属单质,B、C、D都是化合物,A与B发生的反应常用于刻制印刷电路板,该反应的离子方程式________________________________________。
(4)若A、B、C为化合物,D、X为单质,A、B、C中肯定含有X元素的是________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在实验室中常用二氧化锰和浓盐酸反应来制备氯气,实验装置如图所示。
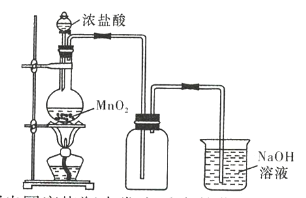
(1)写出圆底烧瓶中发生反应的化学方程式:___________________。
(2)若将过量的二氧化锰与20mL 12mol/L的盐酸混合加热,充分反应后生成的氯气明显少于0.06mol,请写出两个可能的原因:①______________________________;②______________________________。
(3)为了提高浓盐酸的利用率,请写出两条改进措施:①______________________________;②______________________________。
(4)实验结束清洗仪器时,为了减小烧瓶中残留氯气对环境的污染,可以向烧瓶中加入 _____________ ,所发生反应的离子方程式 _________________________________ 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com