
 ,
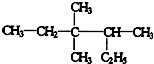
, .的分子式为
.的分子式为 含有2种不同的氢原子.
含有2种不同的氢原子. 最长碳连为6个碳,3号位有2个甲基,4号位有1个甲基,故名称为3,3,4-三甲基已烷;4号位的碳原子连有四个不同基团,为手性碳原子,
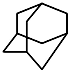
最长碳连为6个碳,3号位有2个甲基,4号位有1个甲基,故名称为3,3,4-三甲基已烷;4号位的碳原子连有四个不同基团,为手性碳原子, 的分子式为C10H16;1molC10H16完全燃烧,需要氧气的物质的量为:10+
的分子式为C10H16;1molC10H16完全燃烧,需要氧气的物质的量为:10+| 16 |
| 4 |
 含有2种不同的氢原子,故它的一溴取代物有2种;
含有2种不同的氢原子,故它的一溴取代物有2种;

科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
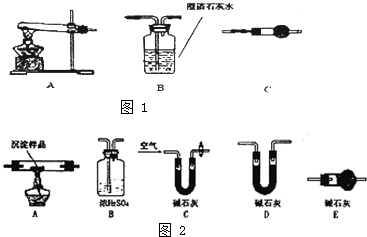 某研究性学习小组将一定浓度Na2CO3溶液滴入CuSO4溶液中得到蓝色沉淀.
某研究性学习小组将一定浓度Na2CO3溶液滴入CuSO4溶液中得到蓝色沉淀.查看答案和解析>>
科目:高中化学 来源: 题型:
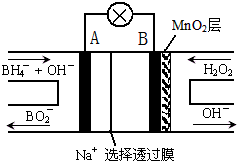
| A、电极B为正极 |
| B、放电过程中,Na+从正极区向负极区迁移 |
| C、电池负极的电极反应为:BH4-+8OH--8e-═BO2-+6H2O |
| D、在电池反应中,每消耗1L 6mol/L H2O2溶液,理论上流过电路中的电子为12NA |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
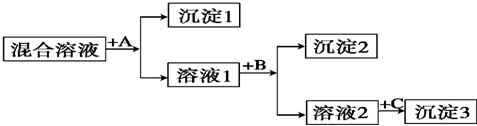
| Ba2+ | Cu2+ | Ag+ | |
| Cl- | 溶 | 溶 | 不 |
| CO | 不 | 不 | 不 |
| SO | 不 | 溶 | 微 |
| S2- | 溶 | 不 | 不 |
查看答案和解析>>
科目:高中化学 来源: 题型:
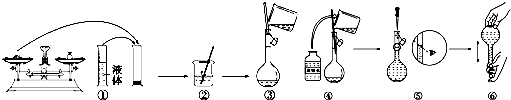
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com