
【题目】常温下,向20mL0.2mol·L-1H2A溶液中滴加0.2mol.L-1NaOH溶液,溶液中微粒H2A、HA-、A2-的物质的量的变化曲线如图所示。下列说法错误的是
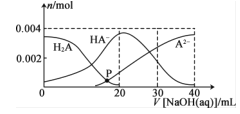
A.当V[NaOH(aq)]=20 mL时.c(OH- )=c(H+ )+c(HA- )+2c(H2A)
B.在P点时,c(Na+ )+c(H+ )=c(OH- )+c(HA- ) +c(A2- )+c(H2A)
C.当V[NaOH(aq)]=30 mL时,2c(Na+ )=3[c(HA- )+c(A2- )+c(H2A)]
D.当V[NaOH(aq)]=40 mL.时.c(Na+ )>c(A2- )>c(OH- )>c(HA- )>c(H2A)>c(H+)
【答案】A
【解析】
A. 当V(NaOH)=20mL时,二者恰好完全反应生成NaHA,根据电荷守恒得:c(OH-)+2c(A2-)+c(HA-)=c(H+)+c(Na+),根据物料守恒得c(Na+)=c(HA-)+c(H2A)+c(A2-),二者结合可得:c(OH-)+c(A2-)=c(H+)+c(H2A),则c(OH-)<c(H+)+c(H2A)<c(H+)+c(HA-)+2c(H2A),故A错误;
B. P点满足电荷守恒:c(HA-)+2c(A2-)+c(OH-)=c(Na+)+c(H+),根据图象可知,P点c(A2-)=c(H2A),则c(H2A)+c(HA-)+c(A2-)+c(OH-)=c(Na+)+c(H+),,故B正确;
C.当V(NaOH)=30mL时,混合溶液中溶质为等物质的量浓度的NaHA、Na2A,根据物料守恒可得:2c(Na+)=3[c(HA-)+c(A2-)+c(H2A)],故C正确;
D.当V(NaOH)=40mL时,反应后溶质为Na2A,A2-部分水解生成等浓度的OH-、HA-,溶液中还存在水电离的氢氧根离子,则c(OH-)>c(HA-),正确的离子浓度大小为:c(Na+)>c(A2-)>c(OH-)>c(HA-)>c(H2A)>c(H+),故D正确;
故选B。


科目:高中化学 来源: 题型:
【题目】锂空气充电电池有望成为电动汽车的实用储能设备。工作原理示意图如下,下列叙述正确的是
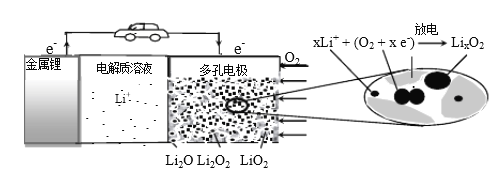
A. 该电池工作时Li+向负极移动
B. Li2SO4溶液可作该电池电解质溶液
C. 电池充电时间越长,电池中Li2O 含量越多
D. 电池工作时,正极可发生: 2Li+ +O2+ 2e-=Li2O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】人们对苯及芳香烃的认识有一个不断深化的过程。
(1)已知分子式为C6H6的结构有多种,其中的两种为:
Ⅰ![]() Ⅱ
Ⅱ![]()
①这两种结构的区别表现在定性方面(即化学性质方面):Ⅱ能_______,而Ⅰ不能。
a.被酸性高锰酸钾溶液氧化 b.与溴水发生加成反应
c.与溴发生取代反应 d.与氢气发生加成反应
②C6H6还可能有另一种立体结构(如图所示),该结构的二氯代物有____种。
![]()
(2)萘也是一种芳香烃,它的分子式是C10H8,请你判断它的结构简式可能是下列中的____。
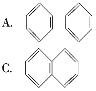
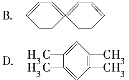
(3)根据第(2)小题中判断得到的萘的结构简式,它不能解释萘的下列事实中的____。
A.萘不能使酸性高锰酸钾溶液褪色 B.萘能与H2发生加成反应
C.萘分子中所有原子在同一平面内 D.一溴代萘(C10H7Br)只有两种同分异构体
(4)现代化学认为萘分子碳碳之间的键是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中可以证明反应H2(g)+I2(g)![]() 2HI(g)已达平衡状态的是
2HI(g)已达平衡状态的是
①单位时间内生成nmol H2的同时生成nmol HI;②一个H-H键断裂的同时有两个H-I键断裂;③百分含量w(HI)=w(I2);④反应速率v(H2)=v(I2)=v(HI);⑤c(HI)∶c(H2)∶c(I2)=2∶1∶1;⑥温度和体积一定时,生成物浓度不再变化;⑦温度和体积一定时,容器内的压强不再变化;⑧条件一定时,混合气体的平均相对分子质量不再变化;⑨温度和体积一定时,混合气体颜色不再变化;⑩温度和压强一定时,混合气体的密度不再变化
A.①②③④B.②⑥⑨C.②⑥⑨⑩D.③⑤⑥⑦⑧
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】重铬酸钾常用作有机合成的氧化剂和催化剂等。由含铬废液(主要含Cr3+、Fe3+、K+、SO42-等)制备K2Cr2O7的流程如图所示。

已知:i.在酸性条件下,H2O2能将Cr2O72-还原为Cr3+。
ii.相关金属离子形成氢氧化物沉淀的pH范围如下:
金属离子 | Fe3+ | Cr3+ |
开始沉淀的pH | 1.5 | 4.9 |
沉淀完全的pH | 2.8 | 6.8 |
回答下列问题:
(1)滤渣①的主要成分为_________(填化学式)。
(2)"氧化”步骤中发生反应的离子方程式为____________。
(3)“加热"操作的目的是_________。
(4)“酸化"过程中发生的反应为2CrO42- +2H+![]() Cr2O72-+ H2O (K=4.0×1014L3·mol -3)。已知“酸化”后溶液(pH=1)中c(Cr2O72- )=6. 4×10-3 mol·L-1,则溶液中c(CrO42-)=_______。
Cr2O72-+ H2O (K=4.0×1014L3·mol -3)。已知“酸化”后溶液(pH=1)中c(Cr2O72- )=6. 4×10-3 mol·L-1,则溶液中c(CrO42-)=_______。
(5)可利用微生物电池将镀铬废水中的Cr2O72-催化还原,其工作原理如图所示:
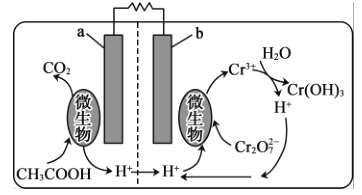
在该电池中,b作______极,a极的电极反应为__________
(6)K2 Cr2O7标准溶液还可用于测定市售硫代硫酸钠晶体(Na2S2O3·5H2O,M=248 g·mol -1)的纯度。测定步骤如下:
i.溶液配制:称取1.2400g市售硫代硫酸钠晶体样品,用新煮沸并冷却的蒸馏水在烧杯中溶解,完全溶解后.全部转移至100mL容量瓶中.加蒸馏水至刻度线。
ii.滴定:取0.01000 mol. L-1的K2Cr2 O7标准溶液20. 00 mL,稀硫酸酸化后加入过量KI溶液,发生反应(Cr2O72-被还原成Cr3+ ,I-被氧化成I2)。然后用硫代硫酸钠样品溶液滴定至淡黄绿色,发生反应:I2+2S2O32 - =S4O62-+2I-。加入淀粉溶液作为指示剂,继续滴定,当溶液蓝色褪去.即为终点。平行滴定3次,样品溶液的平均用量为25.00mL。
①稀硫酸酸化的K2Cr2O7标准溶液与KI溶液反应的离子方程式为_________
②该市售硫代硫酸钠晶体样品的纯度为_______%(保留1位小数)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:25 ℃时,CH3COOH和NH3·H2O的电离常数相等。
(1)25 ℃时,取10 mL 0.1 mol·L-1醋酸溶液测得其pH=3。
①将上述(1)溶液加水稀释至1 000 mL,溶液pH数值范围为___________,溶液中c(CH3COO-)/[c(CH3COOH)·c(OH-)]___________(填“增大”“减小”“不变”或“不能确定”)。
②25 ℃时,0.1 mol·L-1氨水(NH3·H2O溶液)的pH=___________。用pH试纸测定该氨水pH的操作方法为_______________________________________________________。
③氨水(NH3·H2O溶液)电离平衡常数表达式Kb=_______________________________,25 ℃时,氨水电离平衡常数约为___________。
(2)25 ℃时,现向10 mL 0.1 mol·L-1氨水中滴加相同浓度的CH3COOH溶液,在滴加过程中c(NH4+)/c(NH3.H2O)___________(填序号)。
a.始终减小 b.始终增大 c.先减小再增大 d.先增大后减小
(3)某温度下,向V1mL 0.1 mol·L-1NaOH溶液中逐滴加入等浓度的醋酸溶液,溶液中pOH与pH的变化关系如图。已知:pOH=- lgc(OH-)。

图中M、Q、N三点所示溶液呈中性的点是___________(填字母,下同)。
图中M、Q、N三点所示溶液中水的电离程度最大的点可能是___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按官能团的不同,可以对有机物进行分类,请指出下列有机物的种类(填写字母),填在横线上。
(1)CH3CH2CH2COOH____;(2)![]() ____;(3)
____;(3)![]() ____;(4)
____;(4)![]() ____;(5)
____;(5)![]() ____;(6)
____;(6)![]() ____。
____。
A.烷烃 B.烯烃 C.炔烃 D.醚 E.酚 F.醛 G.羧酸 H.芳香烃 I.酯 J.卤代烃 K.醇
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】新能源汽车的大力推广,带动锂电池材料的发展。我国科学家研发出利用钛铁矿(主要成分为![]() ,还含有少量
,还含有少量![]() 、
、![]() 、
、![]() 等杂质)制备锂离子电极材料—
等杂质)制备锂离子电极材料—![]() 和
和![]() 的工艺流程如下:
的工艺流程如下:
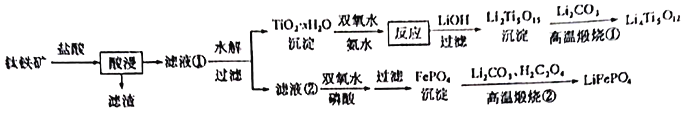
回答下列问题:
(1)![]() 中,Fe元素的化合价为____________。
中,Fe元素的化合价为____________。
(2)“酸浸”后,钛主要以![]() 形式存在,写出
形式存在,写出![]() 水解的的离子方程式_________________。
水解的的离子方程式_________________。
(3)![]() 沉淀与双氧水、氨水反应40min所得实验结果如下表所示:
沉淀与双氧水、氨水反应40min所得实验结果如下表所示:
温度/℃ | 30 | 35 | 40 | 45 | 50 |
| 92 | 95 | 97 | 93 | 88 |
分析高于40℃时![]() 转化率下降的原因_______________。
转化率下降的原因_______________。
(4)![]() 中Ti的化合价为
中Ti的化合价为![]() ,其中过氧键的数目为_____________。
,其中过氧键的数目为_____________。
(5)滤液②中加入双氧水和磷酸,反应生成![]() 的离子方程式为____________;若测得Fe3+沉淀完全后,溶液中
的离子方程式为____________;若测得Fe3+沉淀完全后,溶液中![]() 为
为![]() ,则常温下溶液的pH=______________。(已知
,则常温下溶液的pH=______________。(已知![]() 的
的![]() )
)
(6)从滤液②中得到![]() 沉淀之后,要对其进行洗涤、干燥,检验沉淀已经洗涤干净的方法_________________________________________。
沉淀之后,要对其进行洗涤、干燥,检验沉淀已经洗涤干净的方法_________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中进行反应:X(g)+3Y(g)![]() 2Z(g),有关下列图像的说法错误的是
2Z(g),有关下列图像的说法错误的是
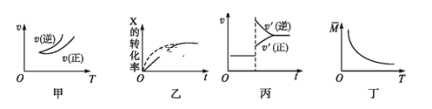
A.依据图甲可判断正反应为放热反应
B.在图乙中,虚线可表示使用了催化剂
C.若正反应的ΔH<0,图丙可表示升高温度使平衡向逆反应方向移动
D.由图丁中气体平均相对分子质量随温度的变化情况,可推知正反应的ΔH>0
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com