
【题目】人们对苯及芳香烃的认识有一个不断深化的过程。
(1)已知分子式为C6H6的结构有多种,其中的两种为:
Ⅰ![]() Ⅱ
Ⅱ![]()
①这两种结构的区别表现在定性方面(即化学性质方面):Ⅱ能_______,而Ⅰ不能。
a.被酸性高锰酸钾溶液氧化 b.与溴水发生加成反应
c.与溴发生取代反应 d.与氢气发生加成反应
②C6H6还可能有另一种立体结构(如图所示),该结构的二氯代物有____种。
![]()
(2)萘也是一种芳香烃,它的分子式是C10H8,请你判断它的结构简式可能是下列中的____。
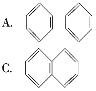
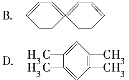
(3)根据第(2)小题中判断得到的萘的结构简式,它不能解释萘的下列事实中的____。
A.萘不能使酸性高锰酸钾溶液褪色 B.萘能与H2发生加成反应
C.萘分子中所有原子在同一平面内 D.一溴代萘(C10H7Br)只有两种同分异构体
(4)现代化学认为萘分子碳碳之间的键是__________。
【答案】ab 3 c a 介于单键与双键之间的独特的键
【解析】
(1)①I为苯不含双键,II中含2个碳碳双键,结合苯及烯烃的性质来解答;
②结构对称,只有一种H,二氯代物有三角形面上相邻、四边形面上相邻和相对位置;
(2)萘是一种芳香烃,含有苯环,不饱和度为![]() =8,含有两个苯环;
=8,含有两个苯环;
(3)根据萘分子碳碳之间的键是介于C-C单键与C=C双键之间的一种特殊的键,及苯的平面结构,等效氢解答;
(4)萘是一种芳香烃,含有苯环,不饱和度为![]() =8,含有两个苯环,萘分子碳碳之间的键是介于C-C单键与C=C双键之间的一种特殊的键。
=8,含有两个苯环,萘分子碳碳之间的键是介于C-C单键与C=C双键之间的一种特殊的键。
(1)①I(![]() )中碳碳之间的键是介于C-C单键与C=C双键之间的一种特殊键,不能被被酸性高锰酸钾溶液氧化,不能能与溴水发生加成反应,而II(
)中碳碳之间的键是介于C-C单键与C=C双键之间的一种特殊键,不能被被酸性高锰酸钾溶液氧化,不能能与溴水发生加成反应,而II(![]() )含有碳碳双键,能被被酸性高锰酸钾溶液氧化,能与溴水发生加成反应。结构都能与溴发生取代反应,都能与氢气发生加成反应,故答案为ab;
)含有碳碳双键,能被被酸性高锰酸钾溶液氧化,能与溴水发生加成反应。结构都能与溴发生取代反应,都能与氢气发生加成反应,故答案为ab;
②![]() 的一氯代物只有1种,二氯代物中的另一个氯原子的位置有三角形面上相邻、四边形面上相邻和相对位置,共3种,即
的一氯代物只有1种,二氯代物中的另一个氯原子的位置有三角形面上相邻、四边形面上相邻和相对位置,共3种,即![]() 的二氯代物有3种;
的二氯代物有3种;
(2)萘是一种芳香烃,含有苯环,不饱和度为![]() =8,含有两个苯环,结构简式为
=8,含有两个苯环,结构简式为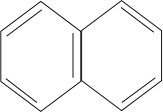 ,故答案为:c;
,故答案为:c;
(3)萘分子碳碳之间的键是介于C-C单键与C=C双键之间的一种特殊的键;
a.由萘的结构简式,萘分子能使溴水褪色,故a错误;
b.萘是一种芳香烃,含有两个苯环,具有苯的一些性质,可以与氢气加成,故b正确;
c.如图所示的6个碳原子处于同一平面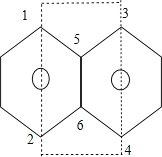 ,1、2碳原子处于右边苯环氢原子位置,3、4碳原子处于左边苯环氢原子位置,5、6碳原子共用,苯为平面结构,所以萘是平面结构,所有原子处于同一平面,故c正确;
,1、2碳原子处于右边苯环氢原子位置,3、4碳原子处于左边苯环氢原子位置,5、6碳原子共用,苯为平面结构,所以萘是平面结构,所有原子处于同一平面,故c正确;
d.萘是对称结构,只有两种氢原子,故一溴代物有两种结构,故d正确;
故答案为:a;
(4)萘是一种芳香烃,含有苯环,不饱和度为![]() =8,含有两个苯环,结构简式为
=8,含有两个苯环,结构简式为![]() ,萘分子碳碳之间的键是介于C-C单键与C=C双键之间的一种特殊的键。
,萘分子碳碳之间的键是介于C-C单键与C=C双键之间的一种特殊的键。


 新思维假期作业寒假吉林大学出版社系列答案
新思维假期作业寒假吉林大学出版社系列答案科目:高中化学 来源: 题型:
【题目】25 ℃时,下列各组离子在指定溶液中一定能大量共存的是( )
A.0.1 mol·L-1 AlCl3溶液中:H+、Na+、Cl-、![]()
B.能使紫色石蕊溶液变蓝的溶液:Ag+、Fe3+、Br-、![]()
C.能使淀粉碘化钾试纸显蓝色的溶液:K+、![]() 、S2-、
、S2-、![]()
D.由水电离产生的c(H+)=10-12 mol·L-1的溶液中:![]() 、
、![]() 、
、![]() 、Cl-
、Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯气、氨气和二氧化硫三种气体均是重要的化工原料且都会对环境造成污染,某课外活动小组拟探究三者的部分性质。
Ⅰ.利用如图装置探究干燥的氯气与氨气之间的反应。
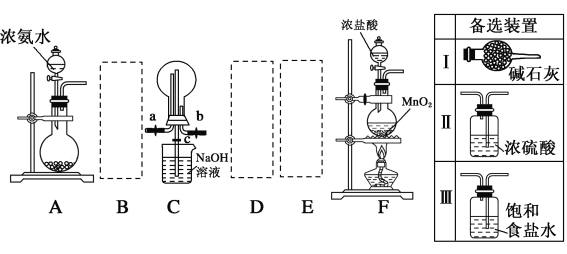
(1)请从备选装置中选择适当的装置连入虚线框中,组成一套完整的探究干燥的氯气与氨气之间的反应的装置,用备选装置序号填空:B___、D__、E__。
(2)装置A中的烧瓶内固体宜选用__(选填以下选项的字母)。
A 烧碱 B 生石灰
C 二氧化硅 D 五氧化二磷
(3)实验时先打开a、c活塞,关闭b活塞,向烧瓶中先通入氨气,然后关闭c活塞,打开b活塞,再向烧瓶中通入氯气,实验中装置C的烧瓶内出现浓厚的白烟并在容器内壁凝结,试推测发生反应的化学方程式为8NH3+3Cl2=6NH4Cl+N2。实验完毕后观察到C烧瓶内还有黄绿色气体,简述如何处理才能不污染环境____________________。
Ⅱ.探究干燥的氯气和SO2的反应:SO2(g)+Cl2(g) SO2Cl2(l) ΔH=-97.3 kJ·mol-1。硫酰氯(SO2Cl2)通常条件下为无色液体,熔点为-54.1 ℃,沸点为69.1 ℃,在潮湿空气中“发烟”,100 ℃以上开始分解,生成二氧化硫和氯气,长期放置也会发生分解。该小组同学用A装置制取SO2,分液漏斗中加入浓硫酸,圆底烧瓶中加入Na2SO3固体,B选择备选装置Ⅱ,将C装置用如图所示的装置甲替换,其余的装置不变来完成探究实验。
SO2Cl2(l) ΔH=-97.3 kJ·mol-1。硫酰氯(SO2Cl2)通常条件下为无色液体,熔点为-54.1 ℃,沸点为69.1 ℃,在潮湿空气中“发烟”,100 ℃以上开始分解,生成二氧化硫和氯气,长期放置也会发生分解。该小组同学用A装置制取SO2,分液漏斗中加入浓硫酸,圆底烧瓶中加入Na2SO3固体,B选择备选装置Ⅱ,将C装置用如图所示的装置甲替换,其余的装置不变来完成探究实验。
(4)装置甲中仪器G的名称为____________,甲中活性炭的作用是____。
(5)如果去掉装置B、D,则在甲的三颈烧瓶中可能发生反应的化学方程式为__________。

(6)为提高本实验中硫酰氯的产率,在实验操作中需要注意的事项有____(填序号)。
A 先通冷凝水,再通气
B 控制气流速率,宜慢不宜快
C 若三颈烧瓶发烫,可适当降温
D 加热三颈烧瓶
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】周期表中前四周期的元素A、B、C、D,原子序数依次增大,且A、B、C同周期。A共有两个原子轨道上有电子,且电子数目相同。B、C相邻,且C中的未成对电子数为3个,D是人类最早使用的元素,并以这种元素命名了一个时代。请回答下面的问题:
(1)A、B、C第一电离能从小到大的顺序为:__________________(填元素符号),D的价层电子排布图为:_______________________。
(2)在不同的温度下,A以ACl2和二聚体 A2Cl4两种形式存在,二聚体的结构式如下图所示:
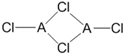
①ACl2中A的杂化方式为_____________。
②1mol A2Cl4中含配位键的数目为_____________。
(3)B元素能形成多种同素异形体,其中一种同素异形体X的晶体结构和晶胞结构如图所示。已知X的密度是a g/cm3,B-B键的键长为r cm,阿伏加德罗常数的值为NA。
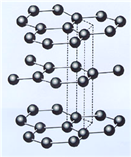
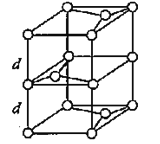
X的晶体结构(左)和晶胞(右)
①X中含有的化学键为____________________。
②X晶体的层间距离为___________________。
(4)C元素可以形成两种含氧酸HCO2和HCO3,酸性是HCO3___HCO2(填“强于”或者“弱于”),原因为__________________________。
(5)将二维密置层在三维空间内堆积,可以得到两种金属晶体的最密堆积方式。一种是按照XYXYXYXY……方式堆积,我们称这种堆积方式为“甲”方式。另外一种是按照XYZXYZXYZXYZ……方式堆积,我们称这种堆积方式为“乙”方式。则金属D的堆积方式为_______。(填“甲”或“乙”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】SPC(2Na2CO33H2O2具有Na2CO3和H2O2的双重性质,广泛应用于印染、医药卫生等领域。以芒硝(Na2SO410H2O)、H2O2等为原料制备SPC的工艺流程如下:
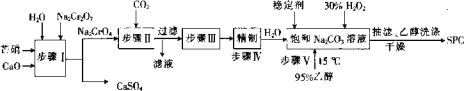
回答下列问题:
(1)步骤I中_____(填“有”或“没有”)发生氧化还原反应。
(2)步骤II中会生成一种可以循环使用的物质,该物质的化学式为_____。
(3)步骤Ⅲ中需要加热,发生反应的化学方程式为______。
(4)步骤Ⅳ中,合成时需选择温度为15℃,其目的是_____,从环境保护的角度看,诙流程中存在的缺点是_______。
(5)SPC的保存方法是________。
(6)过氧化氢用催化剂催化分解时生成水和氧原子,该氧原子非常活泼,称为活性氧。称量0.1600 g样品, 置于250 mL锥形瓶中,并用100 mL 0. 5 molL-1硫酸溶解完全,立即用0.02000molL-1KMnO4标准溶液滴定,滴定至终点时溶液颜色为_____,且半分钟内不恢复为原来的颜色,进行三次平行实验,消耗KMnO4溶液的平均体积为26.56 mL。另外,在不加样品的情况下按照上述过程进行空白实验,消耗KMnO4溶液的平均体积为2.24 mL。该样品的活性氧含量为______%。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】思维辨析:
(1)苯的分子式是C6H6,它不能使酸性KMnO4溶液褪色,属于饱和烃。(_____)
(2)从苯的凯库勒式![]() 看,苯分子中含有三个碳碳双键,应属于烯烃。(______)
看,苯分子中含有三个碳碳双键,应属于烯烃。(______)
(3)苯不能使溴的四氯化碳溶液褪色,但苯可以萃取溴水中的Br2。(______)
(4)烷烃与苯都能与卤素发生取代反应,反应条件相同。(_______)
(5)甲苯和苯互为同系物,都不能与溴水发生加成反应,不能使酸性KMnO4溶液褪色。(________)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向溴水中加入足量的乙醛溶液,可以看到溴水褪色,对产生该现象的原因有如下三种猜想:①溴水与乙醛发生取代反应;②由于乙醛分子中有不饱和键,溴水与乙醛发生加成反应;③由于乙醛具有还原性,溴水将乙醛氧化为乙酸。为探究哪种猜想正确,一研究性学习小组提出了如下两种实验方案:
方案一:检验褪色后溶液的酸碱性;
方案二:测定反应前溴水中 Br2 的物质的量和反应后溶液中 Br—离子的物质的量。
(1)方案一是否可行__________填(“是”或“否”),理由是____________________。
(2)假设测得反应前溴水中 Br2 的物质的量为 amol,
若测得反应后 n(Br-)=__________mol,则说明溴水与乙醛发生取代反应;
若测得反应后 n(Br-)=__________mol,则说明溴水与乙醛发生加成反应;
若测得反应后 n(Br-)=__________mol,则说明溴水将乙醛氧化为乙酸。
(3)按物质的量之比为 1︰5 配制 1000mLKBrO3-KBr 溶液,该溶液在酸性条件下完全反应可生成 0.5molBr2。取该溶液 10mL 加入足量乙醛溶液,使其褪色,然后将所得溶液稀释为 100mL,准确量取其中 10mL,加入过量的 AgNO3 溶液,过滤、洗涤、干燥后称量得到固体 0.188g。若已知 CH3COOAg 易溶于水,试通过计算判断溴水与乙醛发生反应的类型为__________(选填猜想序号)。
(4)写出上述测定过程中的三个反应的离子方程式:
①KBrO3 和KBr 在酸性条件下的反应:______________________________;
②溴水与乙醛的反应:______________________________;
③测定 Br-离子含量的反应:______________________________;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向20mL0.2mol·L-1H2A溶液中滴加0.2mol.L-1NaOH溶液,溶液中微粒H2A、HA-、A2-的物质的量的变化曲线如图所示。下列说法错误的是
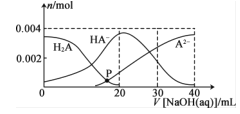
A.当V[NaOH(aq)]=20 mL时.c(OH- )=c(H+ )+c(HA- )+2c(H2A)
B.在P点时,c(Na+ )+c(H+ )=c(OH- )+c(HA- ) +c(A2- )+c(H2A)
C.当V[NaOH(aq)]=30 mL时,2c(Na+ )=3[c(HA- )+c(A2- )+c(H2A)]
D.当V[NaOH(aq)]=40 mL.时.c(Na+ )>c(A2- )>c(OH- )>c(HA- )>c(H2A)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】煤和石油等化石燃料对促进经济社会发展起到了重要的作用,这些燃料合理的综合利用是当前节能减排的要求。请回答下列问题:
(1)石油分馏是石油炼制的重要环节,这种操作是在_______(填设备名称)内完成的。工业上通常使用的分馏石油的方法有常压分馏和_____,分馏的目的是___________。
(2)石油不仅是重要的燃料,还是重要的化工原料的来源,如利用石油生产乙烯。为了使石油分馏产物进一步生成更多的乙烯、丙烯等短链烃而采取______措施。
(3)目前石油资源逐渐匮乏,人们把目光聚集到储量相对丰富的煤上。目前煤综合利用的主要方法是________________、________和煤的气化,煤气化涉及的化学方程式有:C+O2![]() CO2 2C+O2
CO2 2C+O2![]() 2CO _____________(写出第三个化学方程式)。
2CO _____________(写出第三个化学方程式)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com