
【题目】钒的化合物常用于制作催化剂和新型电池。回答下列问题:
(1)金属钒可由铝热反应制得。已知25℃、101 kPa时,
4A1(s)+3O2(g)=2Al2O3 (s) △H1=a kJ·mol-1
4V(s) +5O2 (g)=2V2O5(s) △H2=b kJ·mol-1
则用铝热反应冶炼金属V(s)的热化学方程式为_____________________。
⑵V2O5为橙黄至砖红色固体,无味、有毒,微溶于水,是许多有机和无机反应的催化剂。下图表示的是25℃时,部分含钒微粒的存在形式、浓度和存在的pH范围(其余可溶性微粒均未标出),图中“[V]”表示含钒微粒的浓度,虚线表示[V]或pH的范围尚未准确确定。
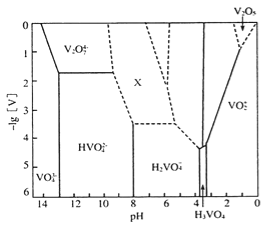
①V2O5溶于足量2mol L-1NaOH溶液中,发生反应的离子方程式为_________________,向反应后的溶液中,滴加硫酸溶液至过量(pH<1)的过程中,开始溶液保持澄淸,滴加一段时间后,观察到有橙黄色沉淀产生,继续滴加硫酸溶液,沉淀又消失。则沉淀消失过程中发生反应的化学方程式为_______________。
②上述滴加硫酸溶液的过程中,先后发生如下反应:

则“X所示区域溶液中的离子”不可能是___________(填序号);
a.V3O93- b.V4O103- c. V4O124-
(3)V2O5是反应2SO2+O2![]() 2SO3的催化剂。其他条件不变,加入V2O5后,该反应的速率加快的原因是_______________;恒温恒压下,加人V2O5,该反应的平衡常数________________ (填“增大”、 “减小”或“不变”);
2SO3的催化剂。其他条件不变,加入V2O5后,该反应的速率加快的原因是_______________;恒温恒压下,加人V2O5,该反应的平衡常数________________ (填“增大”、 “减小”或“不变”);
(4)下图所示为可充电的全钒液流电池构造示意图,该电池中的隔膜只允许H+通过。电池放电时,负极区溶液的pH将_____________(填“增大”、“减小”或“不变”),电池充电时,阳极的电极反应式为_____________________。

【答案】 10Al(s)+3V2O5(s)═5Al2O3(s)+6V(s) ΔH=(2.5a-l.5b)kJ·mol-1 V2O5+6OH-═2VO43-+3H2O V2O5+H2SO4═(VO2)2SO4+H2O b 加入V2O5后,反应路径发生改变,反应的活化能降低,反应速率加快 不变 增大 VO2+-e-+H2O═VO2++2H+
【解析】(1)金属钒可由铝热反应制得。已知25℃、101 kPa时,
①4A1(s)+3O2(g)=2Al2O3 (s) △H1=a kJ·mol-1
②4V(s) +5O2 (g)=2V2O5(s) △H2=b kJ·mol-1
根据盖斯定律,(①×5-②×3)/2,则用铝热反应冶炼金属V(s)的热化学方程式为10Al(s)+3V2O5(s)═5Al2O3(s)+6V(s) ΔH=(2.5a-l.5b)kJ·mol-1
⑵①由图可知,在碱性条件下,以VO43-形式存在,V2O5溶于足量2mol L-1NaOH溶液中,发生反应的离子方程式为V2O5+6OH-═2VO43-+3H2O;沉淀消失过程中发生反应的化学方程式为V2O5+H2SO4═(VO2)2SO4+H2O;②H2VO4―缩水后,V的化合价不变,所以不可能的是V4O102― ;(3)加入V2O5后,该反应的速率加快的原因是反应路径发生改变,反应的活化能降低,反应速率加快。反应温度不变,平衡常数不变;(4)原电池中H+ 带正电,移向正极,故负极区溶液的pH将增大;电池充电时,阳极发生氧化反应,电极反应式为VO2+-e-+H2O═VO2++2H+。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】根据如表提供的数据可知,在溶液中能大量共存的微粒组是

A. H2CO3 、HCO3-、CH3COO-、CN-
B. CO32-、 HCO3-、CH3COOH、CN-
C. HCO3-、CH3COO-、CN-、HCN
D. HCN 、HCO3-、CN-、CO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 常温下醋酸分子不可能存在于pH>7的碱性溶液中
B. 常温下pH=2的H2SO4与pH=13的NaOH溶液混和,所得混和液的pH=11,则H2SO4溶液与NaOH溶液的体积比是9:1
C. 0.1mol/L硫化钠溶液中,c(S2-)+c(HS-)+2c(H2S)=0.1mol/L
D. 常温下向氯化铵溶液中加入少量氨水使溶液的pH=7,则混合溶液中c(NH4+)>c(Cl-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】微量元素在生物体内含量虽然很少,却是维持正常生命活动不可缺少的。这可通过下面的哪一实例得到证实( )
A.缺Mg时叶片变黄
B.油菜缺B时只开花不结果
C.动物血液中钙盐的含量太低会抽搐
D.缺P会导致作物植株矮小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作中都正确的选项是 ( )
①用剩的药品为避免浪费应放回原瓶
②蒸发氯化钠溶液时要用玻璃棒不断搅拌
③称取易潮解的药品必须放在玻璃器皿中称量
④浓硫酸的稀释时,将水沿烧杯内壁缓缓倒入,并不断搅拌
A.②③B.②③④C.②④D.①②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图表示一个化学反应过程,图中的黑球表示两个相同的单糖或其单元。
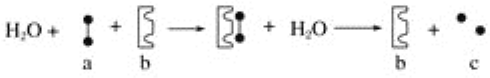
则图中的a、b、c分别表示( )
A. 麦芽糖 麦芽糖酶 葡萄糖
B. 蔗糖 蔗糖酶 果糖
C. 乳糖 乳糖酶 葡萄糖
D. 淀粉 淀粉酶 葡萄糖
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:将Cl2通入适量NaOH溶液,产物中可能有NaCl、NaClO、NaClO3,且![]() 的值与温度高低有关。当n(NaOH)=a mol时,下列有关说法错误的是
的值与温度高低有关。当n(NaOH)=a mol时,下列有关说法错误的是
A. 参加反应的氯气的物质的量等于a/2 mol
B. 改变温度,产物中NaClO3的最大理论产量为a/7 mol
C. 改变温度,反应中转移电子的物质的量ne的范围:a/2 mol≤ne≤5a/6 mol
D. 若某温度下,反应后![]() =11,则溶液中
=11,则溶液中![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应属于氧化还原反应的是
A. H2O+SO3=H2SO4 B. CH4+2O2![]() CO2+2H2O
CO2+2H2O
C. 2Fe(OH)3![]() Fe2O3+3H2O↑ D. NaHCO3+NaOH=Na2CO3+H2O
Fe2O3+3H2O↑ D. NaHCO3+NaOH=Na2CO3+H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com