
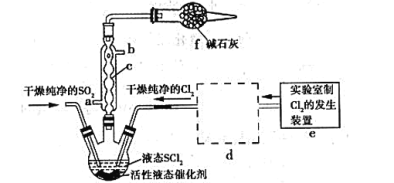
【题目】亚硫酰氯(俗称氯化亚砜,SOCl2)是一种液态化合物,沸点77℃,在农药、制药行业、有机合成等领域用途广泛。SOCl2遇水剧烈反应,液面上产生白雾,并常有刺激性气味的气体产生,实验室合成原理:SO2+Cl2+SCl2=2SOCl2,部分装置如图所示:
请回答下列问题:
(1)装置f的作用是_____。
(2)实验室用二氧化锰制备Cl2的离子方程式为_____。
(3)SOCl2遇水剧烈反应,液面上产生白雾,并伴有刺激性气味的气体,写出有关反应的化学方程式_____。
(4)下列制备SO2的原理中最佳选择是____。
A.Cu与浓硫酸混合共热
B.Na2S2O3溶液与稀硫酸混合反应
C.Na2SO3固体与70%的H2SO4混合反应
D.Na2SO3固体与4mol·L﹣1的HNO3混合反应
(5)装置e中产生的Cl2经过装置d后进入三颈烧瓶,d中所用的试剂为___。(按气流方向)
(6)若反应中消耗Cl2的体积为672mL(己转化为标准状况,SO2足量),最后得到纯净的SOCl2 4.76g,则SOCl2的产率为____(保留三位有效数字)。
(7)实验结束后,将三颈烧瓶中混合物分离开的实验操作是____(己知SCl2的沸点为50℃)。分离产物后,向获得的SOCl2中加入足量NaOH溶液,振荡、静置得到无色溶液W,检验溶液W中存在Cl-的方法是____。
【答案】吸收逸出有毒的Cl2、SO2,防止空气中的水蒸气进入反应装置,防止SOCl2水解 MnO2+4H++2Cl-![]() Mn2++Cl2↑+2H2O SOCl2+H2O=SO2↑+2HCl↑ C 饱和食盐水,浓硫酸 66.7% 蒸馏 取少量W溶液于试管中,加入过量 Ba(NO3)2溶液,静置,取上层清液,滴加HNO3酸化,再加入AgNO3溶液,产生白色沉淀,则说明溶液中有Clˉ
Mn2++Cl2↑+2H2O SOCl2+H2O=SO2↑+2HCl↑ C 饱和食盐水,浓硫酸 66.7% 蒸馏 取少量W溶液于试管中,加入过量 Ba(NO3)2溶液,静置,取上层清液,滴加HNO3酸化,再加入AgNO3溶液,产生白色沉淀,则说明溶液中有Clˉ
【解析】
(1)SOCl2遇水会发生水解反应,Cl2、SO2有毒,会污染空气;
(2)二氧化锰与浓盐酸再加热条件下反应生成MnCl2、氯气与水;
(3)SOCl2遇水剧烈反应,液面上产生白雾,并伴有刺激性气味的气体,说明反应生成HCl和SO2;
(4)从反应原理、原料的利用率及能源消耗等角度分析;
(5)装置d干燥氯气,且除去HCl;
(6)消耗氯气![]() =0.03mol,由方程式得到氯化亚砜的理论值为0.06mol,进而计算产率;
=0.03mol,由方程式得到氯化亚砜的理论值为0.06mol,进而计算产率;
(7)氯化亚砜沸点为77℃,Cl2的沸点为50℃,所以采用分馏的方法即可将之分离;SOCl2中加入足量NaOH溶液会生成亚硫酸钠、氯化钠,亚硫酸根会影响氯离子的检验,用硝酸钡除去亚硫酸根离子,用硝酸酸化除去过量的氢氧化钠及可能存在的碳酸根等,再用硝酸银溶液检验氯离子。
(1)SOCl2遇水会发生水解反应,Cl2、SO2有毒,会污染空气,装置f的作用是:吸收逸出有毒的Cl2、SO2,防止空气中的水蒸气进入反应装置,防止SOCl2水解;
(2)二氧化锰与浓盐酸再加热条件下反应生成MnCl2、氯气与水,反应离子方程式为:MnO2+4H++2Cl-![]() Mn2++Cl2↑+2H2O;
Mn2++Cl2↑+2H2O;
(3)SOCl2遇水剧烈反应,液面上产生白雾,并伴有刺激性气味的气体,说明反应生成HCl和SO2,发生反应的化学方程式为SOCl2+H2O=SO2↑+2HCl↑;
(4)A.Cu与浓硫酸混合共热有SO2生成,但硫酸的消耗量大,且反应需要加热,耗能,故A错误;
B.Na2S2O3溶液与稀硫酸混合反应,除生成SO2,还有S生成,S元素利用率不高,故B错误;
C.Na2SO3固体与70%的H2SO4混合反应生成硫酸钾与二氧化硫还有水,操作简单,比较合理,故C正确;
D.Na2SO3固体与4mol·L﹣1的HNO3混合反应,硝酸具有很强的氧化性,将亚硫酸钠中的正4价的硫氧化为正6价的硫酸根离子而无法得到二氧化硫,故D错误;
故答案为C;
(5)装置e中产生的Cl2混有水、HCl,则d框内包含一个盛装饱和食盐水的气瓶除去HCl,一个盛装浓硫酸的干燥装置;
(6)消耗氯气![]() =0.03mol,由SO2+Cl2+SCl2═2SOCl2,生成SOCl2为0.04mol×2=0.08mol,则SOCl2的产率为
=0.03mol,由SO2+Cl2+SCl2═2SOCl2,生成SOCl2为0.04mol×2=0.08mol,则SOCl2的产率为![]() =66.7%;
=66.7%;
(7)已知氯化亚砜沸点为77℃,已知SCl2的沸点为50℃,所以采用分馏的方法即可将之分离;SOCl2中加入足量NaOH溶液会生成亚硫酸钠、氯化钠,亚硫酸根会影响氯离子的检验,用硝酸钡除去亚硫酸根离子,用硝酸酸化除去过量的氢氧化钠及可能存在的碳酸根等,再用硝酸银溶液检验氯离子,即检验溶液W中存在Cl-的方法是:取少量W溶液于试管中,加入过量Ba(NO3)2溶液,静置,取上层清液,滴加HNO3酸化,再加入AgNO3溶液,产生白色沉淀,则说明溶液中有Clˉ。


科目:高中化学 来源: 题型:
【题目】请回答下列问题:
(1)(NH4)2SO4中含有化学键的类型为_________________________。
(2)KNO3中NO3-的立体构型为____________________,其中N原子的杂化方式为________,写出与NO![]() 互为等电子体的另一种阴离子的化学式:_______________。
互为等电子体的另一种阴离子的化学式:_______________。
(3)已知配合物CrCl3·6H2O中心原子Cr3+的配位数为6,向含0.1 mol CrCl3·6H2O的溶液中滴加2 mol·L-1 AgNO3溶液,反应完全后共消耗AgNO3溶液50 mL,则该配合物的化学式为________________,Cr在基态时,价电子排布式为_____________________。
(4)LiBH4由Li+和BH4-构成,BH4-的立体构型是____________,根据化合物LiBH4判断,Li、B、H的电负性由大到小的顺序为____________。
(5)丙酮(![]() )分子中C原子轨道杂化类型为_____________;含有的π键与σ键数目之比为___________。
)分子中C原子轨道杂化类型为_____________;含有的π键与σ键数目之比为___________。
(6)第一电离能I 1(Zn)______I 1(Cu)(填“大于”或“小于”),原因是_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】食品香精菠萝酯的生产路线(反应条件略去)如下:

下列叙述错误的是( )
A.步骤(1)产物中残留的苯酚可用FeCl3溶液检验
B.苯酚和菠萝酯均可与酸性KMnO4溶液发生反应
C.苯氧乙酸和菠萝酯均可与NaOH溶液发生反应
D.步骤(2)产物中残留的丙烯醇可用溴水检验
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关说法正确的是( )
A.将![]() 通入酸性高锰酸钾溶液,溶液褪色,体现
通入酸性高锰酸钾溶液,溶液褪色,体现![]() 的还原性
的还原性
B.浓硫酸滴在白纸上,白纸变黑,体现了浓硫酸的吸水性
C.硅晶体具有半导体性能,可用于制造光导纤维
D.将![]() 为5.4的雨水样品在空气中放置一段时间后,测得
为5.4的雨水样品在空气中放置一段时间后,测得![]() 变小,是因为样品吸收了空气中的
变小,是因为样品吸收了空气中的![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Li/Li2O体系的能量循环图如图所示。已知,△H4>0。下列说法正确的是
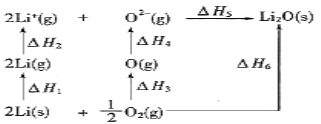
A. △H3<0
B. △H3+△H4+△H5=△H6
C. △H6>△H5
D. △H1+△H2+△H3+△H4+△H5+△H6=0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知常温下二氯化二硫(S2 Cl2)为红棕色液体,其结构式为Cl-S-S-Cl。其制备反应及与水反应的化学方程式如下:①CS2+3Cl2 ![]() CCl4+S2Cl2 ②2S2Cl2 +2H2O=4HCl+SO2↑+3S↓则下列说法正确的是 ( )
CCl4+S2Cl2 ②2S2Cl2 +2H2O=4HCl+SO2↑+3S↓则下列说法正确的是 ( )
A. 反应①中CS2作氧化剂
B. 反应②中S2Cl2既作氧化剂又作还原剂
C. 反应①中每生成1mol S2Cl2转移4mol电子
D. 反应②中氧化产物与还原产物的物质的量之比为3:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上利用CO和水蒸气在一定条件下发生反应制取氢气:
CO(g)+H2O(g)![]() CO2(g)+H2(g) △H=-41 kJ/mol
CO2(g)+H2(g) △H=-41 kJ/mol
某小组研究在相同温度下该反应过程中的能量变化。他们分别在体积均为VL的两个恒温恒容密闭容器中加入一定量的反应物,使其在相同温度下发生反应。相关数据如下:
容器编号 | 起始时各物质物质的量/mol | 达到平衡的时间/min | 达平衡时体系能量的变化/kJ | |||
CO | H2O | CO2 | H2 | |||
① | 1 | 4 | 0 | 0 | t1 | 放出热量:32.8 kJ |
② | 2 | 8 | 0 | 0 | t2 | 放出热量:Q |
(1)该反应过程中,反应物分子化学键断裂时所吸收的总能量_____________(填“大于”、“小于”或“等于”)生成物分子化学键形成时所释放的总能量。
(2)容器①中反应达平衡时,CO的转化率为_____________。
(3)计算容器①中反应的平衡常数K=_____________。某时刻测得②中氢气的物质的量为1.8mol,请问此刻V正 V逆(填大于,小于或等于)
(4)下列叙述正确的是_____________(填字母序号)。
a.平衡时,两容器中H2的体积分数相等
b.容器②中反应达平衡状态时,Q > 65.6 kJ
c.反应开始时,两容器中反应的化学反应速率相等
d.平衡时,两容器中CO的转化率相同
(5)已知:2H2(g)+O2(g)=2H2O(g)ΔH=-484kJ/mol,请写出CO完全燃烧生成CO2的热化学方程式: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】掌握仪器名称、组装及使用方法是中学化学实验的基础,如图为两套实验装置。
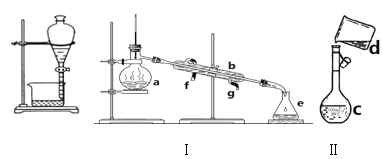
(1)写出下列仪器的名称:a.___,b.___,c.___,d.___。
(2)若利用装置I分离四氯化碳和酒精的混合物,还缺少的仪器是___,冷凝水由___(填f或g)口通入。
(3)现需配制0.25mol/LNaOH溶液450mL,装置II是某同学转移溶液的示意图。
①图中的错误是___。
②根据计算得知,需称量NaOH的质量为___g。
③下列操作使配制的NaOH溶液浓度偏低的有____。
A.将砝码放在左盘上,NaOH放在右盘上进行称量(使用游码)
B.选用的容量瓶内有少量蒸馏水
C.定容摇匀后,液面下降,又加水至刻度线
D.整个配制过程中,容量瓶不振荡
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知有机物A、B、C、D、E、F有以下转化关系.A的产量是衡量一个国家石油化工生产水平的标志;D能使石蕊试液变红;E是不溶于水且具有水果香味的无色液体,相对分子质量是C的2倍;F是塑料的主要成分之一,常用于制食品包装袋。结合如图关系回答问题:

(1)按要求回答下列问题:
①写出A、E的结构简式:A___、E___;
②写出B、C、D中官能团的名称:B___、C___、D___;
③写出反应②的反应方程式:___。
(2)A与苯都是石油化工的重要产品,在一定条件下A可以转化生成苯,按要求回答下列问题:
①苯可以发生取代反应,写出由苯制备溴苯的化学反应方程式:___。
②纯净的溴苯是无色油状液体,实验室制得的粗溴苯通常因溶解了Br2呈褐色,可以加入试剂___除去,该除杂操作所必须的主要玻璃仪器是___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com