
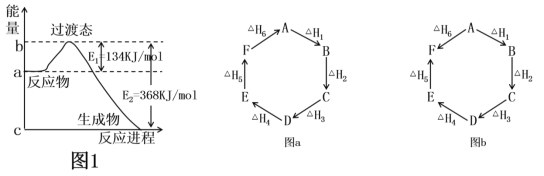
【题目】(1)如图1是1molNO2(g)和1molCO(g)反应生成CO2和NO过程中的能量变化示意图,若在反应体系中加入催化剂,则E1________(填“增大”、“减小”或“不变”,下同),ΔH________。请写出NO2和CO反应的热化学方程式:________________。
(2)观察图a和图b,根据盖斯定律,写出△H1、△H2、△H3、△H4、△H5和△H6的关系。图a:________________________;图b:_________________________。
(3)用CH4催化还原氮氧化物可以消除氮氧化物的污染。
已知:① H2O(l)=H2O(g) △H=+44 kJ/mol
② 2N2(g)+CO2(g)+2H2O(g)=CH4(g)+4NO(g) △H= +1160 kJ/mol
③ CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) △H= -574 kJ/mol
请写出CH4(g)与NO2(g)反应生成参与大气循环的气体和液态水的热化学方程式________。
【答案】减小 不变 NO2(g)+CO(g)=NO(g)+CO2(g)△H=-234 kJ/mol △H1+△H2+△H3+△H4+△H5+△H6=0 △H1+△H2+△H3+△H4+△H5=△H6 CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(l) ΔH=-955kJ/mol
【解析】
(1)若在反应体系中加入催化剂,活化能降低,则E1减小;由图可以知道,ΔH =E1-E2=134kJ/mol-368kJ/mol=-234kJ/mol;1molNO2(g)和1molCO(g)反应生成CO2和NO,则NO2和CO反应的热化学方程式为NO2(g)+CO(g)=NO(g)+CO2(g)△H=-234 kJ/mol;
(2)图a:以A为起点,最终回到A,整个过程没有能量变化,所以△H1+△H2+△H3+△H4+△H5+△H6=0;图b:变化有两个途径A→F,A→B→C→D→E→F,两个途径的热效应相同,所以△H1+△H2+△H3+△H4+△H5=△H6;
(3)① H2O(l)=H2O(g) △H=+44 kJ/mol
② 2N2(g)+CO2(g)+2H2O(g)=CH4(g)+4NO(g) △H= +1160 kJ/mol
③ CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) △H= -574 kJ/mol
则-2×①-![]() ×②+
×②+![]() ×③,得:CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(l),且△H=-2×(+44 kJ/mol)-
×③,得:CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(l),且△H=-2×(+44 kJ/mol)-![]() ×(+1160 kJ/mol)+
×(+1160 kJ/mol)+![]() ×(-574 kJ/mol)= -955kJ/mol,则CH4(g)与NO2(g)反应生成参与大气循环的气体和液态水的热化学方程式为CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(l) ΔH=-955kJ/mol。
×(-574 kJ/mol)= -955kJ/mol,则CH4(g)与NO2(g)反应生成参与大气循环的气体和液态水的热化学方程式为CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(l) ΔH=-955kJ/mol。


科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分,回答下列问题:

(1)在这些元素中,_____(用元素符号填写,下同)是最活泼的金属元素;_____是最活泼的非金属元素,它们组成的化合物含有的化学键类型为_____。
(2)这些元素的最高价氧化物的对应水化物中_____酸性最强;_____碱性最强;能形成两性氢氧化物的元素是_____。
(3)写出①的最高价氧化物的化学式_____,电子式_____。
(4)③和氢元素组成的化合物中,既含有极性共价键又含有非极性共价键的化合物是_____。
(5)比较⑤与⑥的化学性质,_____更活泼,试用实验证明此现象_____(简述操作、现象和结论)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机化合物J是治疗心脏病药物的一种中间体,分子结构中含有3个六元环。其中一种合成路线如下:

已知:①有关A的信息如下:
能发生银镜反应 |
与FeCl3溶液发生显色反应 |
核磁共振氢谱显示有4组峰,峰面积之比为1∶2∶2∶1 |
②R1—CHO+R2—CH2—CHO![]()
![]()
回答以下问题:
(1)A中含有的含氧官能团名称是__________和_________。
(2)写出反应类型:G→H:_________,I→J:____________。
(3)写出下列过程化学方程式。
F→G_____________。B→C__________________。
(4)写出J的结构简式______________。
(5)结合题给信息,以D为原料经过三步反应制备1,3—丁二烯,设计合成路线(其他试剂任选)__________________________________________。
合成路线流程图示例:

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A.强酸、强碱、重金属盐等可使蛋白质变性
B.用新制氢氧化铜悬浊液(必要时可加热)能鉴别甲酸、乙醇、乙醛
C.乙酸乙酯中混有的乙酸,可加入足量的饱和![]() 溶液,经分液除去
溶液,经分液除去
D.向苯和苯酚的混合液中加入浓溴水,充分反应后过滤,可除去苯中少量的苯酚
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生活密切相关,下列说法不正确的是![]()
A.“酸雨”、“臭氧层受损”、“光化学烟雾”都与氮氧化物有关
B.PM2.5作为空气质量预报的一项重要指标,它是指空气中直径小于或等于2.5m的颗粒物,该值越高,代表空气污染程度越严重
C.静电除尘治理悬浮颗粒污染,其依据是胶体的电泳原理
D.为消除碘缺乏症,卫生部规定食盐中必须加含碘物质,食盐中所加含碘物质是KI
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知碳碳单键可以绕键轴自由旋转,结构简式为如图所示的烃,下列说法中正确的是( )

A. 分子中处于同一直线上的碳原子最多有6个
B. 该烃苯环上的二氯代物共有13种
C. 该烃的一氯代物共有8种
D. 分子中至少有12个碳原子处于同一平面上
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为一种广泛使用的高分子材料助剂的结构简式,下列说法正确的是( )(CH3CH2CH2CH3可表示为![]()
![]()

A.该有机物的分子式为C24H40O4
B.1mol该有机物与氢气发生加成反应,最多消耗5mol氢气
C.该有机物在氢氧化钠作用下发生水解反应得到三种有机物
D.该有机物在FeBr3存在下与液溴发生取代反应生成两种一溴代物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知![]() 为
为![]() 和
和![]() 的混合物,且知氧化性顺序:
的混合物,且知氧化性顺序:![]() ,取
,取![]() 样品进行如下图所示的实验:
样品进行如下图所示的实验:

(1)写出③步可能发生反应的3个离子方程式为________________________、________________________、________________________。
(2)若溶液E中只有一种金属离子,则一定是______;若D固体是纯净物,该固体是______。(填化学式)
(3)向溶液A中加入![]() 粉,若会反应,则写出反应的离子方程式,若不会反应,则填“不能”在横线上__________________________________________。
粉,若会反应,则写出反应的离子方程式,若不会反应,则填“不能”在横线上__________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图甲为一种新型污水处理装置,该装置可利用一种微生物将有机废水的化学能直接转化为电能。图乙为电解氯化铜溶液的实验装置的一部分。下列说法中正确的是

A. a极要与Y极连接
B. N电极发生还原反应,当N电极消耗5.6L(标准状况下)气体时,则a电极增重64g
C. 不论b为何种电极材料,b极的电极反应式一定为2C1--2e-=Cl2↑
D. 若有机废水中主要含有乙醛,则图甲中M极发生的电极应为:CH3CHO+3H2O-l0e-=2CO2↑+l0H+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com