
【题目】设NA为阿伏加德罗常数的值。下列说法正确的是
A.足量Zn与一定量的浓硫酸反应产生22.4L气体时,转移的电子数为2NA
B.5NH4NO3![]() 2HNO3+4N2↑+9H2O反应中,生成28gN2时,转移的电子数目为4NA
2HNO3+4N2↑+9H2O反应中,生成28gN2时,转移的电子数目为4NA
C.过量的铁在1mol Cl2中然烧,最终转移电子数为2NA
D.由2H和18O所组成的水11 g,其中所含的中子数为4NA
【答案】C
【解析】
A.未注明是在标准状况下生成的22.4L气体,故无法计算转移的电子数,A选项错误;
B.5NH4NO3![]() 2HNO3+4N2↑+9H2O反应中,铵根离子中被氧化的N元素化合价由-3价升高为N2中的0价,共失去15个电子,被还原的氮元素由硝酸根中+5价降低为氮气中的0价,共得到15个电子,则生成28g(即1mol)氮气,转移电子的物质的量为
2HNO3+4N2↑+9H2O反应中,铵根离子中被氧化的N元素化合价由-3价升高为N2中的0价,共失去15个电子,被还原的氮元素由硝酸根中+5价降低为氮气中的0价,共得到15个电子,则生成28g(即1mol)氮气,转移电子的物质的量为![]() =3.75mol,个数为3.75NA,B选项错误;
=3.75mol,个数为3.75NA,B选项错误;
C.过量的铁在1mol Cl2中然烧,Cl2被还原为Cl-,共转移2mol电子,数目为2NA,C选项正确;
D.由2H和18O所组成的水化学式为2H218O,一个2H218O含有1×2+10=12个中子,11g2H218O的物质的量为0.5mol,则含有的中子数为6NA,D选项错误;
答案选C。


科目:高中化学 来源: 题型:
【题目】以含1个碳原子物质(如CO、CO2、CH4、CH3OH等)为原料的“碳一化学”处于未来化学产业的核心,成为科学家研究的重要课题。请回答下列问题:
(1)已知CO、H2、CH3OH(g)的燃烧热分别为-283.0kJ·mol-1、-285.8kJ·mol-l、-764.5kJ·mol-l。则反应I:CO(g)+2H2(g)=CH3OH(g)△H=___
(2)在温度T时,向体积为2L恒容容器中充入3molCO和H2的混合气体,发生反应I,反应达到平衡时,CH3OH(g)的体积分数(φ)与n(H2)/n(CO)的关系如下图所示。
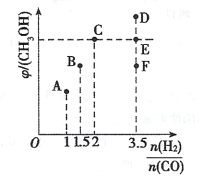
①当起始n(H2)/n(CO)=1时,从反应开始到平衡前,CO的体积分数将___(填“增大”、“减小”或“不变”)。
②当起始n(H2)/n(CO)=2时,反应经过l0min达到平衡,CO转化率为0.5,则0~l0min内平均反应速率v(H2)=___。
③当起始n(H2)/n(CO)=3.5时,达到平衡后,CH3OH的体积分数可能是图像中的__。(填“D”、“E”或“E”点)。
(3)在一容积可变的密闭容器中充有10molCO和20molH2,发生反应I。CO的平衡转化率(α)与温度(T)、压强(P)的关系如下图所示。
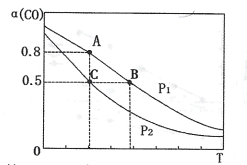
①压强P1=___(填“<”、“=”或“>”)P2;A、B、C三点的平衡常数KA、KB、KC的大小关系为___(用“<”、“=”或“>”表示)。
②若达到平衡状态C时,容器体积为10L,则在平衡状态A时容器体积为____L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于有机化合物的说法错误的是( )
A. 甘氨酸和氯乙烯都能通过聚合反应生成高分子化合物
B. 检测淀粉是否完全水解,向水解液中滴加碘水
C. 等质量的苯和苯乙烯(![]() )完全燃烧,消耗氧气的物质的量不相同
)完全燃烧,消耗氧气的物质的量不相同
D. 乙酸和葡萄糖都能与新制的氢氧化铜反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分枝酸可用于生化研究。其结构简式如图。下列关于分枝酸的叙述正确的是

A. 分子中含有2种官能团
B. 可与乙醇、乙酸反应,且反应类型相同
C. 1mol分枝酸最多可与3molNaOH发生中和反应
D. 可使溴的四氯化碳溶液、酸性高锰酸钾溶液褪色,且原理相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫化氢的转化是资源利用和环境保护的重要研究课题。将H2S和空气的混合气体通入FeCl2、CuCl2的混合溶液中反应回收S,其物质转化如图所示。下列说法错误的是( )

A.在图示的转化中,Fe3+和CuS是中间产物
B.在图示的转化中,化合价不变的元素只有铜
C.图示转化的总反应是2H2S+O2![]() 2S+2H2O
2S+2H2O
D.当有1molH2S转化为硫单质时,需要消耗O2的物质的量为0.5mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为解决“温室效应”日趋严重的问题,科学家们不断探索CO2的捕获与资源化处理方案,利用CH4捕获CO2并转化为CO和H2混合燃料的研究成果已经“浮出水面”。
已知:①CH4(g)十H2O(g)==CO(g)+3H2(g) △H1=+206.4kJ/mol
②CO(g)+H2O(g)==CO2(g)+H2(g) △H2=-41.2kJ/mol
T1°C时,在2L恒容密闭容器中加入2molCH4和1molCO2,并测得该研究成果实验数据如下:
请回答下列问题:
时间/s | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
CO2/mol | 1 | 0.7 | 0.6 | 0.54 | 0.5 | 0.5 | 0.5 |
H2/mol | 0 | 0.6 | 0.8 | 0.92 | 1 | 1 | 1 |
(1)该研究成果的热化学方程式③CH4(g)+CO2(g)==2CO(g)+2H2(g) △H=_____
(2)30s时CH4的转化率为_______,20~40s,v(H2)=_______.
(3)T2°C时,该反应的化学平衡常数为1.5,则T2___T1(填“>”“=”或 “<”。)
(4)T1°C时反应③达到平衡的标志为______________。
A.容器内气体密度不变 B.体系压强恒定
C.CO和H2的体积分数相等且保持不变 D.2v(CO)逆=v(CH4)正
(5)上述反应③达到平衡后/span>,其他条件不变,在70 s时再加入2 molCH4和1molCO2,此刻平衡的移动方向为________(填“不移动”“正向”或“逆向"),重新达到平衡后,CO2的总转化率比原平衡____________(填“大”“小”或“相等”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外活动小组设计了下列装置,验证二氧化碳跟过氧化钠反应时需要与水接触。
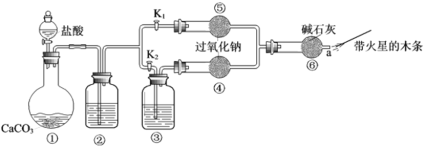
(装置分析)
(1)装置①中反应的化学方程式是___________。
(2)装置②中的试剂是___________(填序号)。装置③中的试剂是___________.
a.饱和![]() 溶液 b.饱和
溶液 b.饱和![]() 溶液 c.浓
溶液 c.浓![]()
(进行实验)
步骤1:打开弹簧夹![]() ,关闭
,关闭![]() ,打开分液漏斗活塞加入盐酸,将带火星的木条放在a处。
,打开分液漏斗活塞加入盐酸,将带火星的木条放在a处。
步骤2:打开弹簧夹![]() ,关闭
,关闭![]() ,打开分液漏斗活塞加入盐酸,将带火星的木条放在a处。
,打开分液漏斗活塞加入盐酸,将带火星的木条放在a处。
(3)步骤1和步骤2中,a处带火星的木条产生的实验现象分别是__________;__________。
(4)过氧化钠跟二氧化碳反应的化学方程式是________
(实验反思)
(5)有同学提出质疑:“上述实验不足以证明有水存在时过氧化钠跟二氧化碳发生了化学反应。”其理由是_______。
(6)需要补充的实验操作是:取⑤中反应后的少量固体,_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现将下列物质分别装入有水的锥形瓶里(见下图),立即塞紧带 U 形管的塞子, 发现 U 形管内滴有红墨水的水面如图所示状态,判断加入的物质不可能是( )
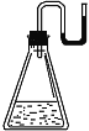
A.NaOH 固体B.浓硫酸C.![]() 晶体D.CaO固体
晶体D.CaO固体
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com