
| 25 |
| 2 |
| 25 |
| 2 |
| 1311.7kJ |
| 2 |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
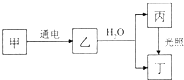 �ס��ҡ�������4�����ʾ���AԪ�أ����м���ɫ��Ӧ�ʻ�ɫ����Ϊ����ɫ���嵥�ʣ�����֮������ͼ��ʾ��ת����ϵ��ת�������в��ֲ���δ�������
�ס��ҡ�������4�����ʾ���AԪ�أ����м���ɫ��Ӧ�ʻ�ɫ����Ϊ����ɫ���嵥�ʣ�����֮������ͼ��ʾ��ת����ϵ��ת�������в��ֲ���δ��������鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A������ķ�ɢ����ͨ����ֽ��϶������Һ�ķ�ɢ�ʲ��� |
| B�������ܲ��������ЧӦ |
| C�������ɢ������ֱ����1nm��100nm֮�� |
| D��������һ�����������ȶ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
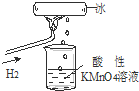 ��У��ѧ��ȤС������һ����ͼ��ʾ��ʵ�飬�����ձ�������KMnO4��Һ��ɫ�������ձ��е���Һ���ɺ�������KSCN��FeCl2��Һ����Һ�Ժ�ɫ����������£�������
��У��ѧ��ȤС������һ����ͼ��ʾ��ʵ�飬�����ձ�������KMnO4��Һ��ɫ�������ձ��е���Һ���ɺ�������KSCN��FeCl2��Һ����Һ�Ժ�ɫ����������£�������| A�����ɵ�ˮ���ӻ�ѧ���ʱȽϻ��� |
| B��H2ȼ�������˾��������Ե����� |
| C��H2����ȴΪҺ̬�⣬Һ���ˮ��Һ���л�ԭ�� |
| D��H2ȼ�յIJ����п��ܺ���һ������H2O2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
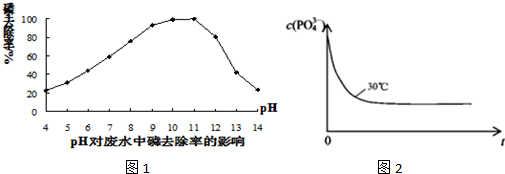
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ѡ�� | ���ᴿ������ | ѡ�õ��Լ� | �������� |
| A | I2��H2O�� | CCl4 | ��ȡ����Һ |
| B | CO2��CO�� | O2 | ��ȼ |
| C | Zn ��Cu�� | ϡ���� | ���� |
| D | �Ҵ���ˮ�� | ��ʯ�� | ���� |
| A��A | B��B | C��C | D��D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��Na+ |
| B��SO42-��Na+ |
| C��S2-��SO42-��Na+ |
| D��Al3+ |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com