
【题目】碳和硫是高中化学学习的两种重要非金属元素
(1)下列C原子的电子排布式表达的状态中能量最高的是_____。
A 1s22s22p2 B.1s22s22px12py1 C.1s22s22px12pz1 D.1s22s12px12py12pz1
(2)硫有一种结构为![]() 的分子(灰球代表硫原子)。其中硫原子杂化方式为_____。
的分子(灰球代表硫原子)。其中硫原子杂化方式为_____。
(3)Fe(CO)5可用作催化剂、汽油抗爆剂等,其分子中σ键和π键的数目之比为_____。
(4)已知CS2晶体结构类似于干冰。CS2晶体中与每个CS2分子距离最近且等距的CS2分予有_____个。推测CS2晶体密度与冰的晶体密度较大的为_____。可能的原因是_____。又知CS2晶体中晶胞参数是apm,NA表示阿佛加德罗常数的值,晶体密度为_____g/cm3(用含a、NA等符号的表达式表示)。
(5)Na2S是高子晶体,其晶格能可通过图的Born﹣Haber循环计算得到。
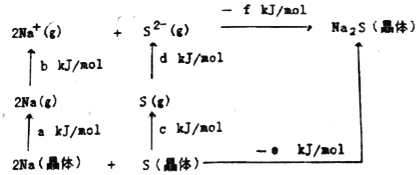
由此可知,Na原子的第一电离能为_____kJ/mol,Na2S的晶格能为_____kJ/mol。(用图中给出的符号作答)
【答案】D sp3 1:1 12 CS2晶体 冰晶体中水分子之间形成的氢键具有方向性与饱和性,空间利用率低,密度下,而CS2晶体中分子之间为范德华力,没有方向性,分子密堆积,密度大 ![]()
![]() f
f
【解析】
(1)基态原子核外电子排布式符合能量最低原理、泡利原理、洪特规则,选项中A、B、C为基态原子电子排布式。D中2s能级1个电子跃迁到2p能级,为激发态,D表示的原子的能量更高,故答案为:D;
(2)结构中S原子形成2个S﹣S键,有2对孤对电子,杂化轨道数目为4,S原子杂化方式为sp3杂化,故答案为:sp3;
(3)Fe(CO)5中Fe与5个CO分子形成5个配位键,属于σ键,CO与氮气分子互为等电子体,CO结构式为C≡O,CO分子中含有1个σ键、2个π键,Fe(CO)5分子含有10个σ键、10个π键,含有的σ键、π键数目之比为1:1,故答案为:1:1;
(4)CS2晶体结构类似于干冰,则CS2晶体中CS2位于立方晶胞的顶点与面心位置,以顶点CS2分子研究,与之紧邻的CS2分子处于晶胞面心,每个顶点为8个晶胞共用,每个面心为2个晶胞共用,故晶体中与1个CS2分子距离最近且等距的CS2分子数为![]() ;冰晶体中水分子之间形成的氢键具有方向性与饱和性,空间利用率低,密度下,而CS2晶体中分子之间为范德华力,没有方向性,分子密堆积,密度大;
;冰晶体中水分子之间形成的氢键具有方向性与饱和性,空间利用率低,密度下,而CS2晶体中分子之间为范德华力,没有方向性,分子密堆积,密度大;
晶胞中CS2分子数目=![]() =4,晶胞质量=
=4,晶胞质量=![]() g,晶体密度=
g,晶体密度=
![]() gcm﹣3,故答案为:12;CS2晶体;冰晶体中水分子之间形成的氢键具有方向性与饱和性,空间利用率低,密度下,而CS2晶体中分子之间为范德华力,没有方向性,分子密堆积,密度大;
gcm﹣3,故答案为:12;CS2晶体;冰晶体中水分子之间形成的氢键具有方向性与饱和性,空间利用率低,密度下,而CS2晶体中分子之间为范德华力,没有方向性,分子密堆积,密度大;![]() ;
;
(5)气态基态Na原子失去1个电子转化为气态基态钠离子需要的最低能量为Na的第一电离能,故Na的第一电离能为![]() kJ/mol;Na2S晶格能是Na+、S2-气态离子形成1molNa2S晶体释放的能量,故Na2S的晶格能为 f kJ/mol,故答案为:
kJ/mol;Na2S晶格能是Na+、S2-气态离子形成1molNa2S晶体释放的能量,故Na2S的晶格能为 f kJ/mol,故答案为:![]() ;f。
;f。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】二茂铁可用作燃料的节能消烟剂、抗爆剂等。实验室制备二茂铁装置示意图如右下图(二茂铁熔点是173℃,在100℃时开始开华;沸点是249℃)。实验步骤为:
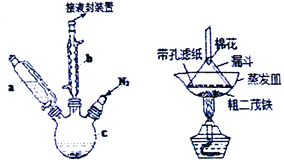
①在三颈烧瓶中加入25g粉末状的KOH,并从仪器a中加入60mL无水乙醚到烧瓶中,充分搅拌,同时通氮气约10min;
②再从仪器a滴入5.5mL新蒸馏的环戊二烯(密度0.95g/cm3),搅拌;
③将6.5g无水FeCl2与(CH3)2SO(二甲亚砜,作溶剂)配成的溶液25mL装入仪器a中,慢慢滴入仪器c中,45min滴完,继续搅拌45min;
④再从仪器a加入25mL无水乙醚搅拌;
⑤将c中的液体转入仪器d,依次用盐酸、水各洗涤两次,分液得橙黄色溶液;
⑥蒸发橙黄色溶液,得二茂铁粗产品。
回答下列问题:
(1)仪器b的名称是______________,作用是________________________。
(2)步骤①中通入氮气的目的是__________________________________。
(3)仪器c的适宜容积应为_________:①100mL、②250mL、③500mL;仪器a使用前应进行的操作是_______________________________________。
(4)KOH、FeCl2、C5H6反应生成二茂铁[Fe(C5H5)2]和KCl的化学方程式为_________________________;步骤⑦是二茂铁粗产品的提纯,该过程在右图中进行,其操作名称为 ____________________________。
(5)为了确证得到的是二茂铁,还需要进行的一项简单实验是_________________________。
(6)最终得到纯净的二茂铁3.7g,则该实验的产率为 __________________(保留两位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,向10mL0.1mol·L-1一元弱碱XOH溶液中逐滴滴加0.1mol·L-1的HCl溶液,溶液的AG![]() 变化如图所示(溶液混合时体积变化忽略不计)。下列说法不正确的是
变化如图所示(溶液混合时体积变化忽略不计)。下列说法不正确的是
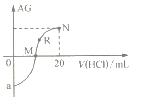
A. 若a=-8,则Kb(XOH)≈10-5
B. M点表示盐酸和XOH恰好完全反应
C. R点溶液中可能存在c(X+)+c(XOH)=c(Cl-)
D. M点到N点,水的电离程度先增大后减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,将浸透了石蜡油的石棉放置在硬质试管的底部,试管中加入碎瓷片,给碎瓷片加强热,关于该实验的分析正确的是( )

A.石棉的作用是催化剂
B.碎瓷片的作用是防暴沸
C.若小试管中的液体是酸性高锰酸钾,则其褪色的原因是石蜡油挥发
D.若小试管中的液体是溴水,一段时间后会观察到其褪色并分层
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某原电池装置如图所示,电池总反应为2Ag+Cl2═2AgCl(忽略溶液体积变化)下列关于该电池装置工作时的说法正确的是( )
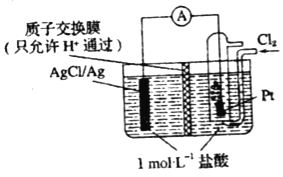
A.H+向左侧迁移
B.若有11.2L氯气(标准状况)参与反应,左侧电极质量增加71 g
C.左侧电极区反应为Ag﹣e﹣═Ag+
D.若把质子交换膜换成阴离子交换膜,一段时间右侧c(HCl)几乎不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硼及其化合物在工业、医药、农业等部门有许多用途。某工厂以铁硼精矿(主要成分为B2O3·2MgO,还有SiO2、CaO、FeO等杂质)制取制硼酸、金属镁的工艺流程图为:
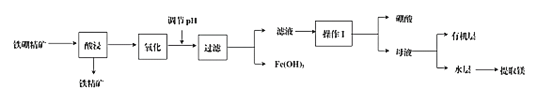
已知:硼酸在不同温度下的溶解度:
温度(℃) | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 |
溶解度(g/100g水) | 3 | 3 | 5 | 7 | 9 | 11 | 15 | 18 | 23 | 29 |
回答下列问题:
(1)使用盐酸酸浸,过程中主要反应的化学方程式为_________,为提高浸出速率,可采取的措施有_________(写出两条)。
(2)酸浸时,温度与硼浸出率的关系如图所示,则合适的酸浸温度为_________。

(3)浸出液“氧化”的是将溶液中的Fe2+用_______试剂氧化为Fe3+,反应的离子方程式为_________。
(4)从滤液中获得H3BO3晶体的“操作I”具体操作是_________。
(5)向滤液中加入有机萃取剂萃取分液,此时硼酸处于_________层中(填“有机”或“无机”)。实验室模拟萃取操作使用的玻璃仪器除烧杯外,另一主要玻璃仪器是_________。
(6)某工厂用 m1 kg的铁硼精矿制备硼酸,得到纯度为99.8%的硼酸m2 kg,则铁硼精矿中硼的质量分数是__________(列式表达)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表短周期的一部分:

请按要求用化学用语回答下列问题:
(1)元素④、⑥、⑨的离子半径由大到小的顺序为________________;
(2)元素②、③、④的简单氢化物的沸点由低到高的顺序: _____________________;
(3)用电子式表示元素④与元素⑥形成的化合物的形成过程____________;
(4)比元素⑦的原子序数多17的元素在周期表的位置为________________;
(5)写出由①④⑤三种元素组成的一种离子化合物的电子式_______________,若将其溶于水,破坏了其中的__________(填“离子键”、“共价键”或“离子键和共价键”);
(6)元素①和元素④形成的化合物及元素①和元素⑧形成的化合物均为18电子分子,请写出这两种化合物按物质的量之比4:1反应的离子方程式________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】决定物质性质的重要因素是物质结构,请回答下列问题。
(1)已知A和B为第三周期元素,其原子的第一至第四电离能如下表所示:
电离能/kJ·mol-1 | I1 | I2 | I3 | I4 |
A | 578 | 1 817 | 2 745 | 11 578 |
B | 738 | 1 451 | 7 733 | 10 540 |
A通常显 价,A的电负性 B的电负性(填“>”、“<”或“=”)。
(2)紫外光的光子所具有的能量约为399 kJ·mol-1。根据下表有关蛋白质分子中重要化学键的信息,说明人体长时间照射紫外光后皮肤易受伤害的原因 。
组成蛋白质的最简单的氨基酸中的碳原子杂化类型是 。
共价键 | C—C | C—N | C—S |
键能/kJ·mol-1 | 347 | 305 | 259 |
(3)实验证明:KCl、MgO、CaO、TiN这4种晶体的结构与NaCl晶体结构相似(如图所示),已知3种离子晶体的晶格能数据如下表:
离子晶体 | NaCl | KCl | CaO |
晶格能/kJ·mol-1 | 786 | 715 | 3 401 |

则该4种离子晶体(不包括NaCl)熔点从高到低的顺序是: 。其中MgO晶体中一个Mg2+周围和它最邻近且等距离的Mg2+有 个。
(4)金属阳离子含未成对电子越多,则磁性越大,磁记录性能越好。离子型氧化物V2O5和CrO2中,适合作录音带磁粉原料的是 。
(5)某配合物的分子结构如图所示,其分子内不含有 (填序号)。
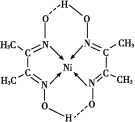
A离子键;B极性键;C金属键;D配位键;E氢键;F非极性键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由下列实验及现象不能推出相应结论的是
实验 | 现象 | 结论 | |
A | 向2mL0.1mol·L-1的FeCl3溶液中加足量铁粉,振荡,加1滴KSCN溶液 | 黄色逐期消失,加KSCN溶液颜色不变 | 还原性:Fe>Fe2+ |
B | 将金属钠在燃烧匙中点燃,迅速伸入集满CO2的集气瓶 | 集气瓶中产生大量白烟,瓶内有黑色颗粒产生 | CO2具有氧化性 |
C | 加热盛有少NH4HCO3固体的试管,并在试管口放置湿润的红色石蕊试纸 | 石蕊试纸变蓝 | NH4HCO3显碱性 |
D | 向2支盛有2mL相同浓度银氨溶液的试管中分别加入2滴相同浓度的NaCl和NaI溶液 | 一只试管中产生黄色沉淀,另一支中无明显现象 | Ksp(AgI)<Ksp(AgCl) |
A. A B. B C. C D. D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com