
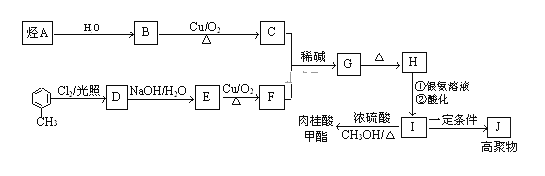
【题目】肉桂酸甲酯是调制具有草莓、葡萄、樱桃、香子兰等香味的食用香精,用于肥皂、洗涤剂、风味剂和糕点的调味,在医药工业中作为有机合成的中间体.合成肉桂酸甲酯的工业流程如图所示:
已知:I.醛与醛能发生反应,原理如下:![]() +CH3CHO
+CH3CHO RCH=CH2CHO
RCH=CH2CHO
Ⅱ.烃A在标准状况下的密度为1.25g/L。
请回答:
(1)化合物H中的官能团为__。
(2)A的结构简式为__,F的结构简式为__。
(3)G→H的反应类型为__。
(4)写出B→C的化学反应方程式___。
【答案】碳碳双键,醛基 CH2=CH2 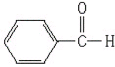 消去反应 2CH3CH2OH+O2
消去反应 2CH3CH2OH+O2![]() 2CH3CHO+2H2O
2CH3CHO+2H2O
【解析】
烃A在标准状况下的密度为1.25g/L,则Mr(A)=1.25×22.4=28,故A为乙烯,与水发生加成反应生成B为乙醇,B发生氧化反应生成C为CH3CHO.乙醛与F发生信息中反应得到G,故F中含有醛基,结合转化关系可知,甲苯与氯气发生甲基上的取代反应生成D为![]() ,D发生发生水解反应生成E为
,D发生发生水解反应生成E为![]() ,E发生氧化反应生成F为
,E发生氧化反应生成F为![]() ,结合信息可知,G为
,结合信息可知,G为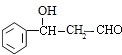 ,H为
,H为![]() ,I为
,I为![]() ,I发生加聚反应生成高聚物J为
,I发生加聚反应生成高聚物J为 ,I与甲醇反应生成肉桂酸甲酯为
,I与甲醇反应生成肉桂酸甲酯为![]() ,据此解答。
,据此解答。
烃A在标准状况下的密度为1.25g/L,则Mr(A)=1.25×22.4=28,故A为乙烯,与水发生加成反应生成B为乙醇,B发生氧化反应生成C为CH3CHO.乙醛与F发生信息中反应得到G,故F中含有醛基,结合转化关系可知,甲苯与氯气发生甲基上的取代反应生成D为![]() ,D发生发生水解反应生成E为
,D发生发生水解反应生成E为![]() ,E发生氧化反应生成F为
,E发生氧化反应生成F为![]() ,结合信息可知,G为
,结合信息可知,G为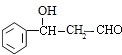 ,H为
,H为![]() ,I为
,I为![]() ,I发生加聚反应生成高聚物J为
,I发生加聚反应生成高聚物J为 ,I与甲醇反应生成肉桂酸甲酯为
,I与甲醇反应生成肉桂酸甲酯为![]() ;
;
(1)由上述分析可知,化合物H的结构简式为![]() ,含有官能团有:醛基、碳碳双键;
,含有官能团有:醛基、碳碳双键;
(2)由分析知:A的结构简式为CH2=CH2,F的结构简式为![]() ;
;
(3G→H为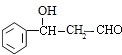 发生消去反应生成
发生消去反应生成![]() ;
;
(4)B→C为乙醇的催化氧化,反应方程式为2CH3CH2OH+O2![]() 2CH3CHO + 2H2O。
2CH3CHO + 2H2O。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】在一定条件下,将H2和N2置于一容积为2 L的密闭容器中发生反应。反应过程中H2、N2和NH3的物质的量变化如图所示。

(1)反应处于平衡状态的时间段是_________________。
(2)图中10~20 min内曲线发生变化的可能原因是_______________________________________。
(3)第25 min,平衡改变的条件是____________________________________,此时正反应速率_____(填“增大”“减小”或“不变”);重新达平衡后,NH3的体积分数比原平衡______(填“大”“小”或“不变”)。
(4)判断该反应达到平衡状态的标志是___________(填字母)。
a.N2和NH3的浓度相等
b.NH3的百分含量保持不变
c.容器中气体的压强不变
d.NH3的生成速率与H2的消耗速率相等
e.容器中混合气体的密度保持不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】螺环化合物具有抗菌活性,用其制成的药物不易产生抗药性,螺[3,4]辛烷的结构如图,下列有关螺[3,4]辛烷的说法正确的是( )

A. 分子式为C8H16B. 分子中所有碳原子共平面
C. 与2—甲基—3—庚烯互为同分异构体D. 一氯代物有4种结构
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】顺式乌头酸是一种重要的食用增味剂,其结构简式如图所示。下列有关说法错误的是( )
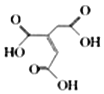
A.该有机物的分子式为:C6H6O6
B.该有机物分子中含有两种官能团
C.该有机物能使酸性KMnO4溶液、溴的四氯化碳溶液褪色,且原理相同
D.相同条件下,等量的顺式乌头酸分别与足量的NaHCO3、Na反应,产生气体的体积比为2:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在下列叙述的方法中,能将有机化合物 转变为
转变为 的有( )
的有( )
①跟足量NaOH溶液共热后,通入二氧化碳直至过量
②与稀硫酸共热后,加入足量Na2CO3溶液
③与稀硫酸共热后,加入足量NaOH溶液
④与稀硫酸共热后,加入足量NaHCO3溶液
⑤与足量的NaOH溶液共热后,再加入适量H2SO4
A.①②B.②③
C.③④D.①④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物A有如下的转化关系: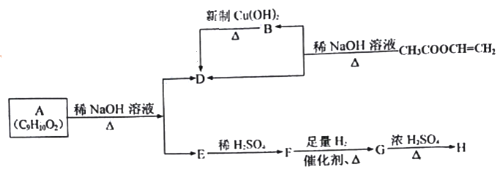
已知:![]() 当羟基与双键碳原子相连接时,易发生如下转化:
当羟基与双键碳原子相连接时,易发生如下转化:
![]()
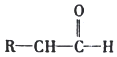
![]() 可与
可与![]() 溶液发生显色反应。
溶液发生显色反应。
![]() 的反应中,有机产物只有一种结构且能使溴水褪色。
的反应中,有机产物只有一种结构且能使溴水褪色。
请回答下列问题:
![]() 的结构简式为______。
的结构简式为______。![]() 中含有的官能团名称为______。
中含有的官能团名称为______。
![]() 的化学方程式为______,
的化学方程式为______,![]() 的化学方程式为______。
的化学方程式为______。
![]() 上述合成过程中没有涉及的反应类型有______
上述合成过程中没有涉及的反应类型有______![]() 填字母
填字母![]() 。
。
![]() 取代反应
取代反应 ![]() 酯化反应
酯化反应 ![]() 加成反应
加成反应 ![]() 消去反应
消去反应 ![]() 氧化反应
氧化反应 ![]() 还原反应
还原反应
![]() 的名称______,与F不同类且含苯环的同分异构体的结构简式为______。
的名称______,与F不同类且含苯环的同分异构体的结构简式为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,在含有PbI2固体的饱和溶液中存在着平衡PbI2(s)![]() Pb2+(aq)+2I(aq),加入KI固体,下列说法正确的是( )
Pb2+(aq)+2I(aq),加入KI固体,下列说法正确的是( )
A.溶液中Pb2+和I的浓度都增大B.溶度积常数Ksp增大
C.沉淀溶解平衡向右移动D.溶液中Pb2+的浓度减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】航天员呼吸产生的CO2用下列反应处理,可实现空间站中O2的循环利用。
Sabatier反应:CO2(g)+4H2(g)![]() CH4(g)+2H2O(g)
CH4(g)+2H2O(g)
水电解反应:2H2O(l)![]() 2H2(g)+O2(g)
2H2(g)+O2(g)
(1)将原料气按![]() ∶
∶![]() =1∶4置于密闭容器中发生Sabatier反应,测得H2O(g)的物质的量分数与温度的关系如图所示(虚线表示平衡曲线)。
=1∶4置于密闭容器中发生Sabatier反应,测得H2O(g)的物质的量分数与温度的关系如图所示(虚线表示平衡曲线)。
① 该反应的平衡常数K随温度升高而__________(填“增大”或“减小”)。

② 温度过高或过低均不利于该反应的进行,原因是________。
③ 200℃达到平衡时体系的总压强为p,该反应平衡常数Kp的计算式为________。(不必化简。用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)
(2)Sabatier反应在空间站运行时,下列措施能提高CO2转化效率的是______(填标号)。
A.适当减压
B.增大催化剂的比表面积
C.反应器前段加热,后段冷却
D.提高原料气中CO2所占比例
E.合理控制反应器中气体的流速
(3)一种新的循环利用方案是用Bosch反应CO2(g)+2H2(g)![]() C(s)+2H2O(g)代替Sabatier反应。
C(s)+2H2O(g)代替Sabatier反应。
① 已知CO2(g)、H2O(g)的生成焓分别为–394 kJmol-1、–242 kJmol-1,Bosch反应的ΔH =________kJmol-1。(生成焓指一定条件下由对应单质生成1mol化合物时的反应热)
② 一定条件下Bosch反应必须在高温下才能启动,原因是________。
③ 新方案的优点是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各选项中所述的2个量,前者一定大于后者的是( )
A.![]() 和
和![]() 的沸点
的沸点
B.纯水在![]() 和
和![]() 时的pH
时的pH
C.同温下,分别在100g水中最多能溶解的无水![]() 和
和![]() 的质量
的质量
D.![]() 时,等体积的、pH都等于3的盐酸与
时,等体积的、pH都等于3的盐酸与![]() 水溶液中,已电离的水分子数
水溶液中,已电离的水分子数
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com