
����Ŀ��I���м����������ǻ����Ȼ����ֻ��ţ���������������γɵĻ������У�д�������������ʵ����ʵĽṹ��ʽ��
��1����ʹʯ����Һ��ɫ����______�֣�
��2���������������������������ͭ����������ԭ��Ӧ����______
��3����ͬ��������������Ʒ�Ӧ�����������ε���______��
II���л���A���������Ƿ��͵õ���Ҳ�ɴ���ţ������ȡ��������AΪ��ɫ��Һ�壬������ˮ��Ϊ�о�A�������ṹ������������ʵ�飺
ʵ�鲽�� | ���ͻ�ʵ����� |
(1)��ȡA 9.0 g������ʹ�������������ܶ�����ͬ������H2��45���� | (1)A����Է�������Ϊ��________. |
(2)����9.0 g A��������O2�г��ȼ�գ���ʹ��������λ���ͨ��Ũ���ᡢ��ʯ�ң��������߷ֱ�����5.4 g��13.2 g | (2)A�ķ���ʽΪ��________. |
(3)��ȡA 9.0 g����������NaHCO3��ĩ��Ӧ������2.24 L CO2(��״��)���������������Ʒ�Ӧ������2.24 L H2(��״��)�� | (3)�ýṹ��ʽ��ʾA�к��еĹ����ţ�________��________. |
(4)A�ĺ˴Ź�����������ͼ��
| (4)A�к���________����ԭ�ӣ� |
(5)����������A�Ľṹ��ʽ________. | |
���𰸡� 3 CH3OH H2CO3 90 C3H6O3 ��COOH ��OH 4 ![]()
��������I�����ֻ���������϶�Ӧ���л�����![]() ��
��![]() ��
��![]() ��
��![]() ��CH3OH��,
��CH3OH��,
(1)��ʹʯ����Һ��ɫ�����ʾ�������,��Ӧ����![]() ��
��![]() ��
��![]() ���֡��𰸣�3��
���֡��𰸣�3��
(2)�ܷ���������Ӧ,˵������-CHO,ֻ��CH3OH����,��ˣ�������ȷ����: CH3OH
(3)��ͬ��������������Ʒ�Ӧ�����������ε���H2CO3,������Na2CO3��NaHCO3,��ˣ�������ȷ����: H2CO3
II��(1)�����ܶ�����ͬ������H2��45��,����֪��A����Է�������Ϊ45![]() =90,
=90,
��ˣ�������ȷ����:90;
(2)�����������֪:![]() mol,
mol,![]() moL
moL![]() mol,
mol,![]() mol,
mol,
����A�ķ���ʽΪ:![]() ,��ˣ�������ȷ����: C3H6O3��
,��ˣ�������ȷ����: C3H6O3��
(3)0.1molA��NaHCO3��Ӧ�ų�0.1molCO2,��˵A��Ӧ����һ���Ȼ�,�������������Ʒ�Ӧ������0.1molH2,˵��A�л�����һ���ǻ�,��ˣ�������ȷ����: ��COOH ��OH ;
(4)�˴Ź�����������4�����շ�,���֮��Ϊ1��1;1��3,����֪��A��Ӧ����4�ֲ�ͬ��������ԭ��,��ˣ�������ȷ����:4;
(5)��������,A�Ľṹ��ʽΪ: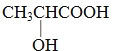 ����ˣ�������ȷ����:
����ˣ�������ȷ����: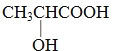 ��
��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����18 mol��L-1 Ũ��������90 mL 3.0 mol��L-1 ϡ�����ʵ�鲽�����£�
�ټ�������Ũ����������
����ȡһ�������Ũ����
���ܽ⡡
��
��ת�ơ�ϴ�ӡ�
���ݡ�ҡ��
��װƿ����ǩ
����������⣺
��1������Ũ����������_____________����ȡŨ�������õ���Ͳ�Ĺ���� _____________����������ѡ��A��10 mL��B��25 mL��C��50 mL��D��100 mL����Ũ����ϡ�͵IJ���______________��
��2���ڢܲ�ʵ��IJ�����_______________________________________________________
��3����������������Ƶ�ϡ����Ũ���к�Ӱ�죿���á�ƫ��ƫС������Ӱ�족��д��
A������Ͳ��ȡŨ�����ϴ����Ͳ����ϴ��Һע������ƿ��___________________��
B������ƿ������ˮϴ�Ӻ������������ˮ________________��
C�����ù����ձ���������δϴ��________________��
D������ʱ���ӿ̶���________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���� X��Y��Z ����Ԫ�أ�X ���л��������бغ���Ԫ�أ� Y �ǵؿ��ﺬ������Ԫ�أ�Z ���� �������Ԫ�ء�X��Y��Z ����Ԫ����ɵ��л��� M �ܱ����Ը�������������� N��Ϊ�˲ⶨ�л��� M �Ľṹ��������ʵ�飺
���� 4.6 g �л��� M ��ȫȼ�գ�������� 0.2mol CO2 �� 5.4 g ˮ�� ���������Ǽ���л��� M���õ���ͼ 1 ��ʾ������ͼ�� ���ú˴Ź����Ǵ����л��� M���õ���ͼ 2 ��ʾͼ�ס�

�Իش��������⣺
��1��M �Ľṹ��ʽ��___________________��N �к��еĹ����ŵĽṹ��ʽΪ_____________��
��2��д�� M ��ͭ�������Ҽ���������������������Ӧ�Ļ�ѧ����ʽ___________________��
��3��д�� M �� N ��Ũ H2SO4���������·�����Ӧ�Ļ�ѧ����ʽ___________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ϩ����������ȩ����Ƴ���ͼ��ʾ��ȼ�ϵ�أ������Ʊ���ȩ��ͬʱ��õ��ܣ����ܷ�ӦʽΪ2CH2===CH2��O2===2CH3CHO�������й�˵����ȷ����
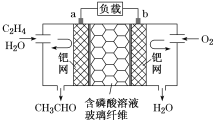
A. ÿ��0.1 mol O2��Ӧ����Ǩ��H��0.4 mol
B. ������ӦʽΪCH2===CH2��2e����H2O===CH3CHO��2H��
C. �����ƶ����缫a��������Һ���缫b
D. �õ��Ϊ���ε��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������һ�ֱ仯�ķ�Ӧ�������������ֱ仯��ͬ���ǣ� ��
A. CH3CH2OH + CH3COOH![]() CH3COOCH2CH3 + H2O
CH3COOCH2CH3 + H2O
B. CH3CH2OH![]() CH2=CH2��+H2O
CH2=CH2��+H2O
C. 2CH3CH2OH![]() CH3CH2OCH2CH3 + H2O
CH3CH2OCH2CH3 + H2O
D. CH3CH2OH + HBr=CH3CH2Br + H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ҩ����һ��ɫ��A�����Ľṹ��ʽΪ![]() �������Ƴɵ��Լ��Լ������ʵ�
�������Ƴɵ��Լ��Լ������ʵ�
����ԡ��ܹ���1molA��Ӧ��Br2(ˮ��Һ)��H2����������ֱ��� �� ��
A. 3 mol��5 mol B. 6 mol��8 mol C. 10 mol��8 mol D. 6 mol��10 mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾΪ��п�ɳ���طŵ�ʱ�缫��������ת����ʾ��ͼ�����ʹ��KOH��K2Zn(OH)4Ϊ�������Һ�����й��ڸõ��˵����ȷ����
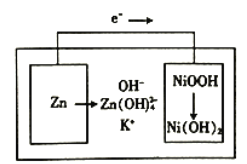
A. �ŵ�ʱ��Һ�е�K+���� B. ���ʱ������Ǩ��pH�ή��
C. �����ϸ�������ÿ����6.5g����Һ��������6.3g D. �ŵ�ʱ������ӦΪH++NiOOH+e-=Ni(OH)2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������л���a(![]() )��b(
)��b(![]() )��c(
)��c(![]() )��˵����ȷ����
)��˵����ȷ����
A. a��b��c�ķ���ʽ��ΪC8H8
B. a��b��c��������ˮ������Ӧ
C. a��b��c��ֻ��a������ԭ�ӻᴦ��ͬһƽ��
D. a��b��c��һ�ȴ����У�b��1�֣�a��c����5��(�����������칹)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NAΪ����٤��������ֵ������˵����ȷ���ǣ� ��
A.�ڳ��¡���ѹ�£�11.2 L N2���еķ�����Ϊ0.5 NA
B.��״���£�22.4 L H2��O2�Ļ��������������ΪNA
C.��״���£�18 g H2O�������22.4 L
D.1 mol SO2�������22.4 L
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com