
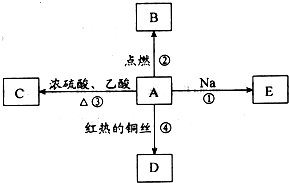
 ⅠA是化学实验室中最常见的有机物,它易溶于水并有特殊香味,并能进行如图所示的多种反应.
ⅠA是化学实验室中最常见的有机物,它易溶于水并有特殊香味,并能进行如图所示的多种反应.| 点燃 |
| 浓硫酸 |
| △ |
| Cu |
| △ |
| 点燃 |
| 浓硫酸 |
| Cu |
| △ |
| 催化剂 |
| 催化剂 |
| 3g |
| 0.5mol |
| 7.2g |
| 18g/mol |
| 8.96L |
| 22.4L/mol |
| 6.4g |
| 16g/mol |


 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案科目:高中化学 来源: 题型:
| 1 |
| 2 |
| A、原子半径:W>Z>Y>X>M |
| B、XZ2、M2Z2、W2Z2均为含非极性键的共价化合物 |
| C、由X元素形成的单质有的可以导电 |
| D、由X、Y、Z、M四种元素形成的化合物中不可能含有离子键 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、若X、Y处于同一周期,则化合物M不可能是正四面体型分子晶体 |
| B、若X的单质常温下是气体,则Y的单质常温下也是气体 |
| C、若X、Y两元素周期数差1,则属于离子化合物的M只有四种 |
| D、若M属于离子晶体,则其中可能含有非极性键 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、位于元素周期表中短周期 |
| B、原子最外层有1个电子 |
| C、属于金属元素,和Na同属于ⅠA族 |
| D、能和水反应,生成氢气 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 元 素 | 有关信息 |
| A | 最高价氧化物对应的水化物(甲)能与其气态氢化物(乙)反应生成盐 |
| B | 最外层电子数是次外层电子数的2倍 |
| C | M层上有3个电子 |
| D | 短周期原子半径最大的主族元素 |
| E | E的氧化物是生活中最常见的液体,D、E同族 |
| F | A与B、F相邻,且A、B、E、F四种元素组成一种离子化合物丙,1mol丙含有10mol原子 |
| G | G、D同周期,G是所在周期元素非金属性最强的 |

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
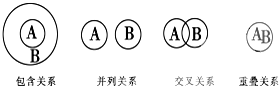
| A、化合物与电解质属于包含关系 |
| B、单质与非电解质属于包含关系 |
| C、溶液与分散系属于并列关系 |
| D、化合物与碱性氧化物属于交叉关系 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com