
【题目】一定温度下,在三个容积均为2.0 L的恒容密闭容器中发生反应:2NO(g)+2CO(g)![]() N2(g)+2CO2(g)。各容器中起始物质的量与反应温度如下表所示,反应过程中甲、丙容器中CO2的物质的量随时间变化关系如图所示:
N2(g)+2CO2(g)。各容器中起始物质的量与反应温度如下表所示,反应过程中甲、丙容器中CO2的物质的量随时间变化关系如图所示:

容器 | 温度/℃ | 起始物质的量/mol | |
NO (g) | CO (g) | ||
甲 | T1 | 0.20 | 0.20 |
乙 | T1 | 0.30 | 0.30 |
丙 | T2 | 0.20 | 0.20 |
下列说法正确的是
A. 该反应的正反应为吸热反应
B. 达到平衡时,乙中CO2的体积分数比甲中的小
C. T1℃时,若起始时向甲中充入0.40 mol NO、0.40mol CO、0.40mol N2和0.40mol CO2,则反应达到新平衡前v(正)<v(逆)
D. T2℃时,若起始时向丙中充入0.06molN2和0.12 molCO2,则达平衡时N2的转化率大于40%
【答案】D
【解析】
A.先拐先平温度高,甲平衡状态时二氧化碳物质的量小,说明温度越高平衡逆向进行;
B.乙中可以看做是甲起始量达到平衡状态,再加入0.1molNO和0.1molCO,相当于增大平衡压强,平衡正向进行;
C.甲状态下平衡时CO物质的量为0.10mol,结合三段式计算平衡常数,依据起始量计算浓度商和平衡常数比较判断反应进行方向;
D.T2℃时,依据图象可知平衡状态下CO物质的量为0.12mol,若起始时向丙中充入0.06mol N2和0.12 mol CO2,反应逆向进行得到平衡状态,和起始量为0.12molNO和0.12molCO达到的平衡相比较,和起始量0.2molCO、NO相比,相当于减少了NO、CO0.08mol的CO、NO,压强减小平衡逆向进行.
A.2NO(g)+2CO(g)![]() N2(g)+2CO2(g),先拐先平温度高,甲状态温度高于丙,T1>T2,此时甲平衡状态二氧化碳物质的量小,说明温度越高平衡逆向进行,逆反应为吸热反应,正反应为放热反应,故A错误;
N2(g)+2CO2(g),先拐先平温度高,甲状态温度高于丙,T1>T2,此时甲平衡状态二氧化碳物质的量小,说明温度越高平衡逆向进行,逆反应为吸热反应,正反应为放热反应,故A错误;
B.乙中可以看做是甲起始量达到平衡状态,再加入0.1molNO和0.1molCO,相当于增大平衡压强,平衡正向进行,达到平衡时,乙中CO2的体积分数比甲中的大,故B错误;
C.甲状态下平衡时CO物质的量为0.10mol,结合三段式计算平衡常数,
2NO(g)+2CO(g)![]() N2(g)+2CO2(g)
N2(g)+2CO2(g)
起始量(mol·L-1) 0.1 0.1 0 0
变化量(mol·L-1) 0.05 0.05 0.025 0.05
平衡量(mol·L-1) 0.05 0.05 0.025 0.05
K=![]() =10,T1℃时,若起始时向甲中充入0.40 mol NO、0.40mol CO、0.40mol N2和0.40mol CO2,Qc=
=10,T1℃时,若起始时向甲中充入0.40 mol NO、0.40mol CO、0.40mol N2和0.40mol CO2,Qc=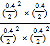 =5<K=10.则反应达到新平衡前v(正)>v(逆),故C错误;
=5<K=10.则反应达到新平衡前v(正)>v(逆),故C错误;
D.T2℃时,平衡状态CO物质的量为0.12mol,
2NO(g)+2CO(g)![]() N2(g)+2CO2(g)
N2(g)+2CO2(g)
起始量(mol) 0.2 0.2 0 0
转化量(mol) 0 0 0.1 0.2
变化量(mol) 0.08 0.08 0.04 0.08
平衡量(mol) 0.12 0.12 0.04 0.08
2NO(g)+2CO(g)![]() N2(g)+2CO2(g)
N2(g)+2CO2(g)
起始量(mol) 0 0 0.06 0.12
转化量(mol) 0.12 0.12 0 0
若起始时向丙中充入0.06mol N2和0.12 mol CO2,反应逆向进行得到平衡状态,和起始量为0.12molNO和0.12molCO达到的平衡相同,和起始量0.2molCO、NO相比,相当于减少了NO、CO 0.08mol的CO、NO,压强减小平衡逆向进行,所以氮气转化率大于40%,故D正确;
故选:D。


科目:高中化学 来源: 题型:
【题目】在120℃的条件下,将体积比为1:1总质量为7.2g的CO与H2的混合气体在足量的O2中充分燃烧,然后将产生的气体通过足量的Na2O2固体中充分反应,反应后固体增加的质量为( )
A.4.5 gB.7.2 gC.9.3 gD.无法计算
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】溴酸镉[Cd(BrO3)2]常用于生产颜料和荧光粉。以镉铁矿(成分为CdO2、Fe2O3、FeO及少量的Al2O3和SiO2)为原料制备[Cd(BrO3)2]的流程如下:
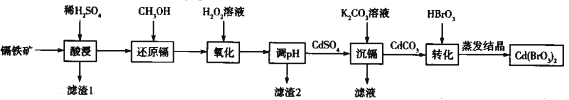
已知:Cd(SO4)2溶于水。
(1)Cd(BrO3)2中Cd的化合价为__________
(2)酸浸时,为了提高镉的浸取率可以采取的指施有__________(写出两种即可)。
(3)还原镉时,产生能使澄清石灰水变浑浊的气体,其发生反应的离于方程式为__________
(4)用H2O2溶液氧化时,氧化剂与还原剂的物质的量之比为__________
(5)已知几种金属离子的氢氧化物开始沉淀和完全沉淀的pH如下表,调pH时,应调整的pH范为____,滤渣2的主要成分为_____(填化学式)。
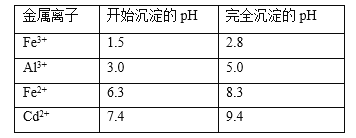
(6)实际工业生产中,有时还采用阳离子交换树脂法来测定沉镉后溶液中Cd2+的含量,其原理是: Cd2++2NaR=2Na++CdR2,其中NaR为阳离子交换树脂。常温下,将沉镉后的溶液(此时溶液pH=6)经过阳离子交换树脂后,测得溶液中的Na+比交换前增加了0.046g/L,则该条件下Cd(OH)2的Ksp值为____
(7)已知镉铁矿中CdO2的含量为72%,整个流程中镉元素的损耗率为8%,则2t该镉铁矿可制得Cd(BrO3)2(相对分子质量为368)_____Kg。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】FFC电解法可由金属氧化物直接电解制备金属单质,西北稀有金属材料研究院利用此法成功电解制备钽粉(Ta),其原理如图所示。下列说法正确的是
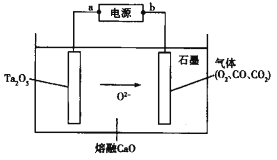
A. 该装置将化学能转化为电能
B. a极为电源的正极
C. Ta2O5极发生的电极反应为Ta2O5+10e—=2Ta+5O2—
D. 石墨电极上生成22.4 L O2,则电路中转移的电子数为4×6.02×1023
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知五种元素的原子序数的大小顺序为C>A>B>D>E,A、C同周期,B、C同主族;A与B形成离子化合物,A2B中所有离子的电子数相同,其电子总数为30;D和E可形成4核10电子的分子。试回答下列问题:
(1)写出下列物质的电子式:
D的单质:_________________;
A、B、E形成的化合物:________________;
D、E形成的化合物:___________________。
(2)A、B两元素组成的化合物A2B2存在的化学键是_______________。
(3)铝与A的最高价氧化物的水化物在水溶液中反应的离子方程式为:_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二碳化学的研究在工业生产中具有重要意义。
(1)在一定温度和压强下,已知:
化学键 | C—H | C—O | O—H | C===O | O===O | C—C |
键能/(kJ·mol-1) | 414 | 326 | 464 | 728 | 498 | 332 |
①CH3CH2OH(g)+1/2O2(g)![]() CH3CHO(g)+H2O(g) ΔH1=________。
CH3CHO(g)+H2O(g) ΔH1=________。
②若反应2CH3CHO(g)+O2(g)![]() 2CH3COOH(g)可自发进行,则CH3CH2OH(g)+O2(g)
2CH3COOH(g)可自发进行,则CH3CH2OH(g)+O2(g)![]() CH3COOH(g)+H2O(g) ΔH2________(填“>”“<”或“=”)0。
CH3COOH(g)+H2O(g) ΔH2________(填“>”“<”或“=”)0。
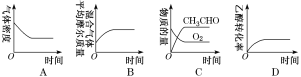
(2)将一定量的CH3CH2OH和O2充入恒温、恒压密闭容器中,发生反应2CH3CH2OH(g)+O2(g)![]() 2CH3CHO(g)+2H2O(g)至平衡状态。下列图象不合理的是________(填字母)。
2CH3CHO(g)+2H2O(g)至平衡状态。下列图象不合理的是________(填字母)。
(3)已知:25 ℃,Ka(CH3COOH)=1.75×10-5,Kb(NH3·H2O)=1.75×10-5,![]() ≈1.3,lg 1.3≈0.1。
≈1.3,lg 1.3≈0.1。
①25 ℃,0.1 mol·L-1CH3COOH溶液的pH=______;将0.1 mol·L-1CH3COOH溶液与0.1 mol·L-1的氨水等体积混合,所得溶液中离子浓度大小关系为_______________________________。
②25 ℃,0.2 mol·L-1NH4Cl溶液中NH4+水解反应的平衡常数Kh=________。(保留2位有效数字)
③25 ℃,向0.1 mol·L-1氨水中加入少量NH4Cl固体,NH3·H2O![]() NH4++OH-的电离平衡________(填“正向”“逆向”或“不”)移动;请用氨水和某种铵盐(其他试剂与用品自选),设计一个实验证明NH3·H2O是弱电解质____________________________________。
NH4++OH-的电离平衡________(填“正向”“逆向”或“不”)移动;请用氨水和某种铵盐(其他试剂与用品自选),设计一个实验证明NH3·H2O是弱电解质____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某种电镀污泥主要含有碲化亚铜(Cu2Te)、三氧化二铬(Cr2O3)以及少量的金(Au),可以用于制取Na2Cr2O7溶液、金属铜和粗碲等,以实现有害废料的资源化利用,工艺流程如下:
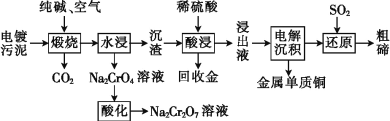
已知:煅烧时,Cu2Te发生的反应为Cu2Te+2O2![]() 2CuO+TeO2。
2CuO+TeO2。
(1)煅烧时,Cr2O3发生反应的化学方程式为__________________。
(2)浸出液中除了含有TeOSO4(在电解过程中不反应)外,还可能含有____(填化学式)。
(3)工业上用重铬酸钠(Na2Cr2O7)母液生产重铬酸钾(K2Cr2O7)的工艺流程如图所示:
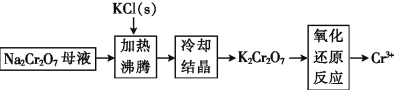
通过冷却结晶能析出大量K2Cr2O7的原因是__________________。
(4)测定产品中K2Cr2O7含量的方法如下:称取产品试样2.50 g配成250 mL溶液,用移液管取出25.00 mL于锥形瓶中,加入足量稀硫酸酸化后,再加入几滴指示剂,用0.1000 mol·L-1硫酸亚铁铵(NH4)2Fe(SO4)2标准液进行滴定,重复进行二次实验。(已知Cr2![]() 被还原为Cr3+)
被还原为Cr3+)
①氧化还原滴定过程中的离子方程式为________________。
②若三次实验消耗(NH4)2Fe(SO4)2标准液的平均体积为25.00 mL,则所得产品中K2Cr2O7的纯度为_____%。[已知M(K2Cr2O7)=294 g·mol-1,计算结果保留三位有效数字]。
(5)上述流程中K2Cr2O7发生氧化还原反应后所得溶液中除含有Cr3+外,还含有一定浓度的Fe3+杂质,可通过加碱调pH的方法使两者转化为沉淀。已知c(Cr3+)=3×10-5 mol·L-1,则当溶液中开始析出Cr(OH)3沉淀时Fe3+是否沉淀完全?____(填“是”或“否”)。{已知:Ksp[Fe(OH)3]=4.0×10-38, Ksp[Cr(OH)3]=6.0×10-31}
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钢是现代社会的物质基础,钢中除含有铁外还含有碳和少量不可避免的钴、硅、锰、磷、硫等元素。请回答下列有关问题:
(1)基态Mn原子的价电子排布式为___________。Mn2+与Fe2+中,第一电离能较大的是__________,判断的理由是_____________________________________。
(2)碳元素除可形成常见的氧化物CO、CO2外,还可形成C2O3(结构式为![]() )。C2O3中碳原子的杂化轨道类型为___________,CO2分子的立体构型为___________。
)。C2O3中碳原子的杂化轨道类型为___________,CO2分子的立体构型为___________。
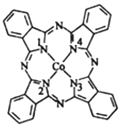
(3)酞菁钴分子的结构简式如图所示,分子中与钴原子通过配位键结合的氮原子的编号是______(填“1” “2” “3”或“4”)其中C、H、O元素电负性由大到小的顺序是_________________________
(4)碳酸盐的热分解是由于晶体中的阳离子结合碳酸根中的氧离子,是碳酸根分解为CO2分子的结果。MgCO3分解温度低于CaCO3,请解释原因_________________________。
(5)氧化亚铁晶胞与NaCl的相似,NaCl的晶胞如图所示。由于晶体缺陷,某氧化亚铁晶体的实际组成为Fe0.9O,其中包含有Fe2+和Fe3+,晶胞边长为apm,该晶体的密度为ρg·cm-3,则a=___________(列出计算式即可,用NA表示阿伏加德罗常数的值)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇(CH3OH)是重要的溶剂和替代燃料,工业上用CO和H2在一定条件下制备CH3OH的反应为CO(g)+2H2(g)![]() CH3OH(g); △H。
CH3OH(g); △H。
(1)在体积为1L的恒容密闭容器中,充入2molCO和4molH2,一定条件下发生上述反应,测得CO(g)和CH3OH(g)的浓度随时间的变化如图甲所示。
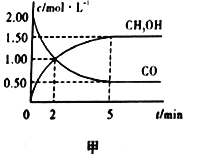
①从反应开始到5min,用氢气表示的平均反应速率v(H2)=________。
②下列说法正确的是________(填序号)。
A. 达到平衡时,H2的转化率为75%
B. 5min后容器中压强不再改变
C. 达到平衡后,再充入氩气,反应速率增大
D. 2min前v(正)>v(逆),2min后v(正)<v(逆)
(2)某温度下,在一恒压容器中分别充入1.2molCO和1molH2,达到平衡时容器体积为2L,且含有0.4molCH3OH(g),则该反应平衡常数的值为__________。
(3)甲醇是一种新型的汽车动力燃料。已知H2(g)、CO(g)、CH3OH(l)的燃烧热分别为285.8kJ/mol、283.0kJ/mol和726.5kJ/mol,则甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式为________。
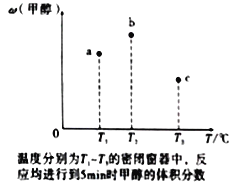
(4)现有容积均为1L的a、b、c三个密闭容器,往其中分别充入1molCO和2molH2的混合气体,控制温度,进行反应,测得相关数据的关系如图所示。b中甲醇体积分数大于a中的原因是____________。达到平衡时,a、b、c中CO的转化率大小关系为___________。
(5)甲醇作为一种燃料还可用于燃料电池。在温度为650℃的熔融盐燃料电池中用甲醇、空气与CO2的混合气体作反应物,镍作电极,用Li2CO3和Na2CO3混合物作电解质。该电池的负极反应式为___________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com