
【题目】已知五种元素的原子序数的大小顺序为C>A>B>D>E,A、C同周期,B、C同主族;A与B形成离子化合物,A2B中所有离子的电子数相同,其电子总数为30;D和E可形成4核10电子的分子。试回答下列问题:
(1)写出下列物质的电子式:
D的单质:_________________;
A、B、E形成的化合物:________________;
D、E形成的化合物:___________________。
(2)A、B两元素组成的化合物A2B2存在的化学键是_______________。
(3)铝与A的最高价氧化物的水化物在水溶液中反应的离子方程式为:_____________。
【答案】![]()
![]()
![]() 离子键、共价键 2Al+2OH-+6H2O===2[Al(OH)4]-+3H2↑
离子键、共价键 2Al+2OH-+6H2O===2[Al(OH)4]-+3H2↑
【解析】
五种元素的原子序数的大小顺序为C>A>B>D>E,A、C同周期,B、C同主族。A与与B形成离子化合物A2B,A2B中所有离子的电子数相同,且电子总数为30,所以每个离子都有10个电子,由化学式的结构可知,B带2个单位负电荷,A带1个单位正电荷,所以A是Na元素,B是O元素,因为A、C同周期,B与C同主族,所以C为S元素;D和E可形成4核10电子的分子,可知其中一定含有氢原子,分子中有4个原子核共10个电子,一定是NH3,结合原子序数D>E,可知D是N元素,E是H元素,以此来解答。
由上述分析可知,E为H、D为N、B为O、A为Na、C为S。
(1)D的单质是氮气,电子式为![]() ;A、B、E形成的化合物是氢氧化钠,电子式为
;A、B、E形成的化合物是氢氧化钠,电子式为![]() ;D、E形成的化合物是共价化合物氨气,电子式为
;D、E形成的化合物是共价化合物氨气,电子式为![]() 。
。
(2)A、B两元素组成的化合物A2B2是过氧化钠,存在的化学键是离子键和共价键。
(3)铝与A的最高价氧化物的水化物在水溶液中反应的离子方程式为2Al+2OH-+6H2O=2[Al(OH)4]-+3H2↑。


 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案科目:高中化学 来源: 题型:
【题目】有A、B、C、D四种元素,常温下A的单质是深红棕色的液体,B、C、D是短周期元素。D元素原子K层的电子数是B元素原子核外电子总数的2倍。C、D元素原子最外层电子数相同,D元素原子核内质子数是C元素原子核内质子数的2倍。
(1)由上述元素组成的一种单质和化合物相互作用生成沉淀的两个反应的化学方程式:①__________________;②____________________。
(2)写出各元素原子的电子排布式:A_____________,B______________,C____________,D____________。
(3)比较C、D两元素的性质:①第一电离能:C________D(填“<”或“>”,下同);②电负性:C________D;③非金属性:C________D;④原子半径:C________D。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用18.4 mol·L-1的浓H2SO4来配制500 mL 0.2 mol·L-1的稀H2SO4。可供选择的仪器有:①玻璃棒、②烧瓶、③烧杯、④胶头滴管、⑤量筒、⑥容量瓶、⑦托盘天平。请回答下列问题:
(1)上述仪器中,在配制稀H2SO4时用不到的有(填代号)________。
(2)经计算,需量取浓H2SO4 ________mL。现有①10 mL、②50 mL、③100 mL三种规格的量筒,你选用的量筒是________(写序号)。
(3)将浓H2SO4加入到适量蒸馏水中稀释后,冷却片刻,随后全部转移到______ mL的容量瓶中。
(4)在配制过程中,其他操作都准确,下列操作中能引起误差偏高的有________(填代号)。
①定容时,加蒸馏水超过刻度线,又用胶头滴管吸出
②转移前,容量瓶中含有少量蒸馏水
③定容摇匀后,发现液面低于刻度线,又用胶头滴管加蒸馏水至刻度线
④定容时,俯视刻度线
(5)在下图的配制过程示意图中,正确的是(填写序号)_______。
A.称量
B.溶解
C.转移
D.定容![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】鹅去氧胆酸和胆烷酸都可以降低肝脏中的胆固醇,二者的转化关系如图,下列说法中正确的是
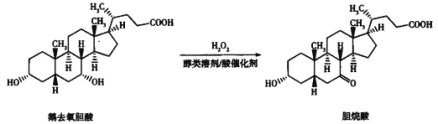
A. 二者互为同分异构体
B. 二者均能发生氧化反应和取代反应
C. 胆烷酸中所有碳原子可能处于同一平面内
D. 等物质的量的鹅去氧胆酸和胆烷酸与足量Na反应时,最多消耗Na的量相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素 W、X、Y、Z的原子序数依次递增,a、b、c、d、e、f 是由这些元素组成的化合物,d是淡黄色粉末,m为元素Y的单质,通常为无色无味的气体。上述物质的转化关系如图。下列说法错误的是 ( )

A.简单离子半径:Z<Y
B.简单气态氢化物的热稳定性:Y>X
C.a一定是烃
D.d中既含有离子键又含有共价键,其中阳离子和阴离子的数目之比为2∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在三个容积均为2.0 L的恒容密闭容器中发生反应:2NO(g)+2CO(g)![]() N2(g)+2CO2(g)。各容器中起始物质的量与反应温度如下表所示,反应过程中甲、丙容器中CO2的物质的量随时间变化关系如图所示:
N2(g)+2CO2(g)。各容器中起始物质的量与反应温度如下表所示,反应过程中甲、丙容器中CO2的物质的量随时间变化关系如图所示:

容器 | 温度/℃ | 起始物质的量/mol | |
NO (g) | CO (g) | ||
甲 | T1 | 0.20 | 0.20 |
乙 | T1 | 0.30 | 0.30 |
丙 | T2 | 0.20 | 0.20 |
下列说法正确的是
A. 该反应的正反应为吸热反应
B. 达到平衡时,乙中CO2的体积分数比甲中的小
C. T1℃时,若起始时向甲中充入0.40 mol NO、0.40mol CO、0.40mol N2和0.40mol CO2,则反应达到新平衡前v(正)<v(逆)
D. T2℃时,若起始时向丙中充入0.06molN2和0.12 molCO2,则达平衡时N2的转化率大于40%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1909年化学家哈伯在实验室首次合成了氨。2007年化学家格哈德·埃特尔在哈伯研究所证实了氢气与氮气在固体表面合成氨的反应过程,示意如下图:
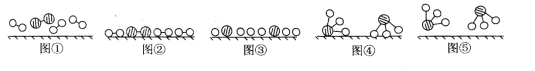
(1)图⑤表示生成的NH3离开催化剂表面,图②和图③的含义分别是______,_______。
(2)已知:4NH3(g)+3O2(g)=2N2(g)+6H2O(g);ΔH=-1266.8kJ/mol,N2(g)+O2(g)=2NO(g)ΔH=+180.5kJ/mol,氨催化氧化的热化学方程式为_________________________。
(3)500℃下,在A、B两个容器中均发生合成氨的反应。隔板Ⅰ固定不动,活塞Ⅱ可自由移动。
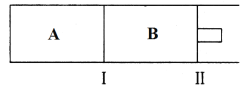
①当合成氨在容器B中达平衡时,测得其中含有1.0molN2,0.4molH2,0.4molNH3,此时容积为2.0L。则此条件下的平衡常数为________________;保持温度和压强不变,向此容器中通入0.36molN2,平衡将______________(填“正向”、“逆向”或“不”)移动。
②向A、B两容器中均通入xmolN2和ymolH2,初始A、B容积相同,并保持温度不变。若要平衡时保持N2在A、B两容器中的体积分数相同,则x与y之间必须满足的关系式为_____________。
(4)以CO和O2为电极燃料,以熔融K2CO3为电解质组成燃料电池,请写出该电池的负极反应方程式_____________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】胡妥油(D)用作香料的原料,它可由A合成得到:
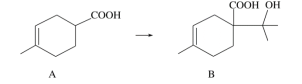
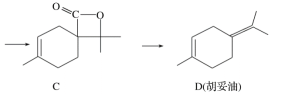
下列说法正确的是
A. 有机物B的分子式为C11H19O3
B. 有机物D分子中所有碳原子一定共面
C. 有机物C的所有同分异构体中可能有芳香族化合物存在
D. 1 mol有机物A中含有6.02×1023个双键.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下下列溶液中的指定离子与100 mL 3.9 mol/L Ba(NO3)2溶液所含NO3-物质的量浓度相同的是
A.390 mL 0.1 mol/L MgCl2溶液中的Cl-
B.200 g 浓度为26%,密度为1.2g/mLNaOH溶液中的OH-
C.50 mL 7.8 mol/L Al2(SO4)3溶液中的SO42-
D.200 mL 3.9 mol/L CaCl2溶液中的Ca2+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com