
【题目】工业上用铝土矿(主要成分为Al2O3,只含Fe2O3杂质)为原料冶炼铝的工艺流程如下:

回答下列问题:
(1)上述反应,其中是氧化还原反应的有___个;写出试剂X的化学式___。
(2)反应②的离子反应方程式______________。
(3)反应①后过滤的沉淀为_____,简述确定此物质中金属元素及其价态的操作过程____。
(4)反应①后过滤时必须用到的玻璃仪器有______________。
(5)请你写出检验试剂X中含有阳离子的实验操作: ______________。
【答案】 1 NaOH AlO2-+CO2+2H2O= Al(OH)3↓+HCO3- Fe2O3 取少量沉淀于一支洁净试管,加入适量稀硫酸(或盐酸)使其完全溶解,再滴加少量硫氰化钾(或硫氰化铵),若溶液呈(血)红色,说明此物之中含有正三价铁元素 玻璃棒、烧杯、漏斗 用洁净的铂丝(铁丝)蘸取试剂X于酒精灯外焰灼烧,看到黄色火焰,即验证试剂X中含有Na+
【解析】Fe2O3和氢氧化钠不反应而氧化铝能反应,向偏铝酸钠中通入过量的二氧化碳可以生成氢氧化铝沉淀,过滤得到氢氧化铝的沉淀,再加热分解得到氧化铝,最后电解得到铝单质,因此试剂X为氢氧化钠溶液,溶液乙为偏铝酸钠溶液,Y为二氧化碳气体。
(1)上述反应,其中属于氧化还原反应的只有电解熔融的氧化铝生成铝的反应;根据上述分析,试剂X为氢氧化钠溶液,故答案为:1;NaOH;
(2)向偏铝酸钠中通入过量的二氧化碳反应的实质是:AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-,
故答案为:AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-;
(3)根据上面的分析可知,反应 ①后过滤的沉淀为Fe2O3,要确定氧化铁中金属元素及其价态,可以用酸溶解,再用KSCN溶液检验铁离子的存在,操作过程为取少量沉淀于一支洁净试管,加入适量稀硫酸(或盐酸)使其完全溶解,再滴加少量硫氰化钾(或硫氰化铵),若溶液呈(血)红色,说明此物之中含有正三价铁元素,故答案为:Fe2O3;取少量沉淀于一支洁净试管,加入适量稀硫酸(或盐酸)使其完全溶解,再滴加少量硫氰化钾(或硫氰化铵),若溶液呈(血)红色,说明此物之中含有正三价铁元素;
(4)反应①后过滤时必须用到的玻璃仪器有玻璃棒、烧杯、漏斗,故答案为:玻璃棒、烧杯、漏斗;
(5)试剂X为氢氧化钠,检验其中含有的钠离子可以使用焰色反应,故答案为:用洁净的铂丝(铁丝)蘸取试剂X于酒精灯外焰灼烧,看到黄色火焰,即验证试剂X中含有Na+。


科目:高中化学 来源: 题型:
【题目】下列各组物质中,不能进行喷泉实验的是( )
A. Cl2和 NaOH 溶液 B. CO2 和 H2O C. CO2 和 NaOH 溶液 D. HCl 和 H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用如图所示装置制取溴化亚铁.D和d中均盛有液溴,E为外套电炉丝的瓷管,e是两只耐高温的瓷皿,其中共盛有56g细铁粉.实验开始时先将干燥、纯净的CO2气流通入D中,然后将铁粉加热至600℃~700℃,E管中反应开始.E中的反应为:
2Fe+3Br2═2FeBr3 , 2FeBr3 ![]() 2FeBr2+Br2↑,
2FeBr2+Br2↑,
最后将d中液溴滴入100℃~120℃的D中,经过几小时的连续反应,在铁管的一端沉积有黄绿色鳞片状溴化亚铁80g.
请回答:
(1)仪器d的名称 .
(2)导入的CO2不干燥,会在E中发生副反应,其含铁副产物为;若所得产物中含此副产物,用化学方法检验.下列方案合理的是 .
A.取少量产物于试管中加入稀盐酸,再加入KSCN溶液
B.取少量产物于硬质大试管中,通入氢气,排尽空气后加热,用CuSO4检验生成的水蒸气
C.用磁铁吸引,看产物能否被吸引
D.取少量产物于试管中加入蒸馏水,过滤看是否有黑色不溶物
(3)为防止污染空气,实验时应在F处连接盛有NaOH溶液的尾气吸收装置,反应的化学方程式: .
(4)取产品10g配制成250mL溶液,取出25.00mL用酸性KMnO4溶液滴定溶液中的Fe2+ , 用去0.03000mol/L酸性KMnO4溶液25.00mL,则产品的纯度为 .
(5)利用除去杂质后的FeBr2可以验证Cl2、Fe3+、Br2的氧化性强弱.将你设计的实验操作、预计的实验现象和实验结论(氧化性强弱)填写在下列表空格内:
实验操作 | 实验现象 | 氧化性强弱 |
① | 溶液呈血红色 | ② |
③ | ④ | Cl2>Br2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式中,正确的是( )
A.钠放入水中??? Na+H2O═Na++OH﹣+H2↑
B.电解饱和食盐水??? 2Cl﹣+2H2O ![]() 2OH﹣+H2↑+Cl2↑
2OH﹣+H2↑+Cl2↑
C.实验室用氯化铝溶液和氨水制氢氧化铝??? Al3++3OH﹣═Al(OH)3↓
D.向碳酸氢铵溶液中加入足量氢氧化钠溶液??? HCO3﹣+OH﹣═CO32﹣+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在体积为2L的密闭容器中进行下列反应:C(s)+CO2(g)═2CO(g);△H=+Q kJmol﹣1 . 如图为CO2、CO的物质的量随时间t的变化关系图.下列说法不正确的是( ) 
A.在0﹣1min内CO的物质的量增加了2mol
B.当固焦炭的质量不发生变化时,说明反应已达平衡状态
C.5min时再充入一定量的CO,n(CO)、n(CO2)的变化可分别由c、b曲线表示
D.3min时温度由T1升高到T2 , 重新平衡时K(T2)小于K(T1)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某温度下,四种一元弱酸的电离平衡常数为:物质的量浓度都为0.1molL﹣1的下列溶液中,pH最小的是( )
HCN | HF | CH3COOH | HNO2 | |
Ka | 6.2×10﹣10 | 6.8×10﹣4 | 1.8×10﹣5 | 6.4×10﹣6 |
A.HCN
B.CHSCOOH
C.HF
D.HNOp
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是 ( )
A. 摩尔是表示物质的量的单位,每摩尔物质含有6.02×1023个分子
B. 2H既可表示2个氢原子,又可表示2 mol氢原子
C. 相同物质的量的CO和CO2所含的原子总数目之比为2∶3
D. 相同质量的CO和CO2所含的原子总数目之比为1∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】强酸与强碱的稀溶液发生中和反应的热效应为H+(aq)+OH(aq)![]() H2O(l) ΔH=57.3 kJ/mol。稀醋酸、浓硫酸、稀硝酸分别与0.1 mol·L1的NaOH溶液恰好完全反应,放出的热量与消耗NaOH溶液的体积之间的关系如图所示(CH3COOH电离要吸热)。则下列描述正确的是
H2O(l) ΔH=57.3 kJ/mol。稀醋酸、浓硫酸、稀硝酸分别与0.1 mol·L1的NaOH溶液恰好完全反应,放出的热量与消耗NaOH溶液的体积之间的关系如图所示(CH3COOH电离要吸热)。则下列描述正确的是
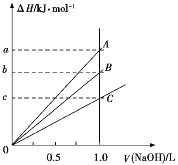
A.A表示稀硝酸与NaOH溶液的反应
B.B表示稀醋酸与NaOH溶液的反应
C.b=5.73
D.C表示浓硫酸与NaOH溶液的反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】依据事实,写出下列反应的热化学方程式。
(1)1 mol C2H4(g)与适量O2(g)反应生成CO2(g)和H2O(l),放出1411 kJ能量: 。
(2)1 mol C2H5OH(l)与适量O2(g)反应生成CO2(g)和H2O(l),放出1366.8 kJ热量: 。
(3)2 mol Al(s)与适量O2(g)发生反应生成Al2O3(s),放出1669.8 kJ热量: 。
(4)在200°C、101 kPa时,1 mol H2与碘蒸气作用生成HI气体,放出14.9 kJ热量: 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com