
����Ŀ�������£�������Һ�е�����Ũ�ȹ�ϵ��ȷ���ǣ� ��
A. һ�����ʵ���Ũ�ȵ�Na2S��Һ�У�c(OH��)��c(H��)��2c(H2S)��c(HS��)
B. ������ˮ�м������NaOH��c(Na��)��c(Cl��)��c(ClO��)��c(OH��)
C. pH��8.3��NaHCO3��Һ��c(Na��)>c(HCO3-)>c(CO32-)>c(H2CO3)
D. 25��ʱ��Ũ�Ⱦ�Ϊ0.1mol��L��1��CH3COOH��CH3COONa�����ҺpH��4.75��c(![]() )+c(
)+c(![]() )=c(CH3COOH)+c(H+)
)=c(CH3COOH)+c(H+)
���𰸡�A
��������A����Na2S��Һ�������������غ��c��OH����=c��H+��+2c��H2S��+c��HS��������A��ȷ��B��������ˮ�м������NaOH�����ݵ���غ��c��Na+��+c��H+��=c��Cl����+c��ClO����+c��OH����������c��Na+����c��Cl����+c��ClO����+c��OH��������B����C��pH=8.3��NaHCO3��Һ����Һ�ʼ��ԣ�˵��HCO3����ˮ��̶ȴ��ڵ���̶ȣ�����c��CO32������c��H2CO3������C����D��25��ʱ��Ũ�Ⱦ�Ϊ0.1mol��L��1��CH3COOH��CH3COONa�Ļ����Һ�д��ڵ���غ���c��CH3COO����+c��OH����=c��Na+��+c��H+����25��ʱ����ҺpH=4.75������Һ�д������̶ȴ��ڴ��������ˮ��̶ȣ�����c��Na+����c��CH3COOH������c��CH3COO����+c��OH������c��CH3COOH��+c��H+������D����ѡA��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���谢���ӵ�������ֵΪNA,�����й�������ȷ���ǣ� ��
A. ������,1LpH=13��Ba(OH)2��Һ�к���OH-����ĿΪ0.2NA
B. �ܱ�������0.2molNO��0.1molO2��ַ�Ӧ��,��������Ϊ0.2NA
C. 7.8gNa2S��7.8gNa2O2�к�������������������Ϊ0.3NA
D. 0.02molNa��0.1mol/L�������ַ�Ӧ��ת�Ƶĵ�����Ϊ0.01NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ߴ�������[Sr(NO3)2]������������ɫ�̻𡢹�ѧ���������ӹ��������ϵȡ��ɹ�ҵ��������(�������ᱵ������Ƶ�����)��ȡ�ߴ������ȵ���������:

��1����Һ1�е���Ҫ������___________(�ѧʽ)��
��2�������ˮϴ������1��Ũ����ϴ�ӵ��ŵ���________________________________��
��3����Һ2�й����ĸ���ϴҺ��N2H4��ԭ����Cr3+��һ�ֲ���Ⱦ���������塣�÷�Ӧ�����ӷ���ʽΪ______________________________________��
��4������3����Ҫ�ɷ���_____(�ѧʽ)����Һ3��c(Cr3+)=_____mol/L(������Ksp[Cr(OH)3]=6.3��10-31)��
��5������XΪ_____________��Sr(NO3)2��nH2Oת��Ϊ�ߴ������ȵĹ����¶�Ҫ������100�棬Ŀ����_________________��
��6��Ϊ�ⶨSr(NO3)2��nH2O����ֵn����7.44g Sr(NO3)2��nH2O������100������������Ϊ6.36g�ĸߴ������ȡ������n=______(M[Sr(NO3)2]=212g/mol)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֦������������о�����ṹ��ʽ��ͼ�����й��ڷ�֦���������ȷ����
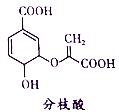
A. �����к���2�ֹ�����
B. �����Ҵ������ᷴӦ���ҷ�Ӧ������ͬ
C. 1mol��֦��������3molNaOH�����кͷ�Ӧ
D. ��ʹ������Ȼ�̼��Һ�����Ը��������Һ��ɫ����ԭ����ͬ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���л����CH2OH(CHOH)4CHO����CH3CH2CH2OH����CH2===CH��CH2OH����CH2===CH��COOCH3����CH2===CH��COOH�У����ܷ����ӳɷ�Ӧ��������Ӧ�����ܷ���������Ӧ����(����)
A. �ۢ� B. �ڢ�
C. �٢ۢ� D. �٢�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��25��ʱ��H2CO3��Ka1=4.2��10-7��Ka2=5.0��10-11����������20mL0.1mol/LNa2CO3��Һ����μ���40mL0.1mol/L'HCl��Һ����Һ�к�̼Ԫ�صĸ�����(CO2���ݳ�δ����)���ʵ�������(����)����ҺpH�仯�IJ��������ͼ��ʾ��
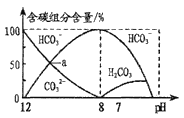
����˵����ȷ����
A. ��ͬһ��Һ�У�H2CO3��HCO3-��CO32-�ܴ�������
B. a��ʱ:c(Na+)+c(H+)=c(OH-)+3c(CO32-)
C. ��pH=7ʱ����Һ��c(Na+)=c(HCO3-)+2c(CO32-)
D. ����Һ��c(HCO3-):c(CO32-)=2:1ʱ����Һ��pH=10
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ӳɷ�Ӧ���л������������˫���ϵ�̼ԭ��������ԭ��(��ԭ����)ֱ�ӽ�������µĻ�������ӵķ�Ӧ�����й�����ӳɷ�Ӧ�ص���(����)
A. ������ˮ�����ˮ����ɫ��dz
B. �ѻ���������ˮ�����ˮ����ɫ��dz
C. ��ϩ��ˮ��һ�������·�Ӧ��ȡ�Ҵ�
D. ��ϩ���Ȼ�����һ�������·�Ӧ��ȡ������һ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ����ϵͳ�У���ʼ�¶�Ϊ25�棬��20.00mL0.1000mol/L�İ�ˮ��Һ����μ���0.1000mol/L��HCl��Һ����û����Һ���¶ȱ仯��ͼ���������˵����ȷ����
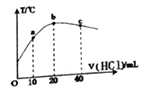
A. a��b��c���ˮ�ĵ���̶���������
B. �ж���Һ��pH:b��pH=7��c��pH<7
C. ��֪25��ʱ0.2mol/L��ˮ�����Ϊ1.33%����ʱ��ˮ��pH ԼΪ12
D. ��a����Һ�ʼ��ԣ���a����c(NH4+)>c(Cl-)>c(NH3��H2O)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з�Ӧ�����������������ڷ�Ӧ������������ �� ��
A. Ba(OH)2��8H2O��NH4Cl��Ӧ B. �Ҵ�ȼ��
C. ��������������ĩ��Ӧ D. NaOH��Һ�����ᷴӦ
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com