
【题目】资源化利用二氧化碳不仅可减少温室气体的排放,还可重新获得燃料或重要工业产品。
(1)以CO2与NH3为原料可合成化肥尿素[CO(NH2)2]。
已知:①2NH3(g)+CO2(g)=NH2CO2NH4(s)△H =-159.47 kJ·mol-1
②NH2CO2NH4(s)=CO(NH2)2(s)+H2O(g)△H =+116.49 kJ·mol-1
③H2O(l)=H2O(g)△H =+88.0 kJ·mol-1
试写出NH3和CO2合成尿素和液态水的热化学方程式______________。
(2)在一定条件下,二氧化碳转化为甲烷的反应如下:CO2(g)+4H2(g)![]() CH4(g)+2H2O(g) ΔH<0
CH4(g)+2H2O(g) ΔH<0
①向一容积为2L的恒容密闭容器中充入一定量的CO2和H2,在300℃时发生上述反应,达到平衡时各物质的浓度分别为CO2:0.2mol·L-1,H2:0.8mol·L-1,CH4:0.8mol·L-1,H2O:1.6mol·L-1,起始充入CO2和H2的物质的量分别为_____、_____,CO2的平衡转化率为______。
②现有两个相同的恒容绝热(与外界没有热量交换)密闭容器I、II,在I中充入1 molCO2,和4 molH2,在II中充入1 mol CH4和2 mol H2 O(g),300℃下开始反应。达到平衡时,下列说法正确的是_________(填字母)。
A.容器I、II中正反应速率相同 B.容器I、II中CH4的物质的量分数相同 C.容器I中CO2的物质的量比容器II中的多 D.容器I中CO2的转化率与容器II中CH4的转化率之和小于1
(3)华盛顿大学的研究人员研究出一种方法,可实现水泥生产时CO2零排放,其基本原理如图所示:
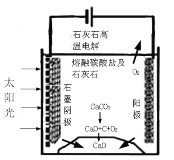
①上述生产过程的能量转化方式是_____。
②上述电解反应在温度小于900℃时进行碳酸钙先分解为CaO和CO2,电解质为熔融碳酸钠,则阳极的电极反应式为___,阴极的电极反应式为______。
【答案】2NH3(g) + CO2(g)=CO(NH2)2(s)+H2O(l) △H =-130.98 kJ·mol1 2mol 8mol 80% CD 太阳能和电能转化为化学能 2CO32--4e-=2CO2↑+O2↑ 3CO2+4e-=C+2CO32-
【解析】
(1)根据盖斯定律进行计算。
(2)①求出改变量,再求起始时浓度,再求起始的物质的量,再计算CO2的平衡转化率;②A.由于反应正向是放热反应,逆向吸热反应,容器I温度高于容器II中温度,因此正反应速率不相同;
B.两个容器是恒温恒容则两容器中CH4的物质的量分数相同,但容器I温度比容器II中温度高,容器I相对恒温恒容容器,平衡逆向移动,容器II相对恒温恒容容器,平衡正向移动,因此容器I中CH4的物质的量分数大;
C.根据B选项类似分析得出容器I中CO2的物质的量比容器II中的多;
D.若是恒温恒容,两个容器的中是等效平衡,转化率相加等于1,但对容器I中CO2的转化率比恒温时减小,对容器II中CH4的转化率比恒温时减小,因此两者转化率之和小于1。
(3)①根据图中信息,石灰石高温电解是吸热反应;②根据图中信息阳极是熔融盐中的碳酸根离子得到电子生成氧气和二氧化碳,阴极是二氧化碳得到电子变为碳和碳酸根。
(1)根据盖斯定律①+②-③得到NH3和CO2合成尿素和液态水的热化学方程式2NH3(g) + CO2(g)=CO(NH2)2(s)+H2O(l) △H =-130.98 kJ·mol1;故答案为:2NH3(g) + CO2(g)=CO(NH2)2(s)+H2O(l) △H =-130.98 kJ·mol1。
(2)①达到平衡时各物质的浓度分别为CO2:0.2mol·L1,H2:0.8mol·L1,CH4:0.8mol·L1,H2O:1.6mol·L1,则CO2改变量为0.8mol·L1,H2改变量为3.2 mol·L1,因此起始时CO2和H2的物质的量浓度分别为1mol·L1,4 mol·L1,容器体积为2L,因此充入CO2和H2的物质的量分别为2mol、8mol,CO2的平衡转化率为![]() ;故答案为:2mol;8mol;80%。
;故答案为:2mol;8mol;80%。
②A.由于反应正向是放热反应,逆向吸热反应,容器I温度高于容器II中温度,因此正反应速率不相同,故A错误;
B.两个容器是恒温恒容则两容器中CH4的物质的量分数相同,但容器I温度比容器II中温度高,容器I相对恒温恒容容器,平衡逆向移动,容器II相对恒温恒容容器,平衡正向移动,因此容器I中CH4的物质的量分数大,故B错误;
C.根据B选项类似分析得出容器I中CO2的物质的量比容器II中的多,故C正确;
D.若是恒温恒容,两个容器的中是等效平衡,转化率相加等于1,但对容器I中CO2的转化率比恒温时减小,对容器II中CH4的转化率比恒温时减小,因此两者转化率之和小于1,故D错误;
综上所述,答案为CD。
(3)①根据图中信息,石灰石高温电解,电能提供能量,太阳能在石墨阴极提供能量,因此上述生产过程的能量转化方式是太阳能和电能转化为化学能;故答案为:太阳能和电能转化为化学能。
②上述电解反应在温度小于900℃时进行碳酸钙先分解为CaO和CO2,电解质为熔融碳酸钠,根据图中信息阳极是熔融盐中的碳酸根离子得到电子生成氧气和二氧化碳,因此阳极的电极反应式为2CO32-4e-=2CO2↑+O2↑,阴极是二氧化碳得到电子变为碳和碳酸根,其阴极的电极反应式为3CO2+4e-=C+2CO32;故答案为:2CO32-4e-=2CO2↑+O2↑;3CO2+4e-=C+2CO32。


 全优点练单元计划系列答案
全优点练单元计划系列答案科目:高中化学 来源: 题型:
【题目】I-具有还原性,含碘食盐中的碘元素主要以KIO3的形式存在,I-、I2、IO3-在一定条件下可发生如图转化关系。下列说法不正确的是
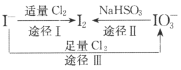
A.用淀粉-KI试纸和食醋可检验食盐是否加碘
B.由图可知氧化性的强弱顺序为C12>IO3->I2
C.生产等量的碘,途径I和途径Ⅱ转移电子数目之比为2:5
D.途径Ⅲ反应的离子方程式:3C12+I-+3H2O=6C1-+IO3-+6H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求填写下列空白
(1)写出Na2O2的电子式_____
(2)Al(OH)3在碱性溶液中的电离方程式为_____
(3)用离子方程式表示Na2S溶液呈碱性的原因_____
(4)在锌粒与稀硫酸的反应体系中,若滴加几滴CuSO4溶液,发现放出气体的速率明显加快,说明其原因:_____;若加入少量醋酸钠固体,发现放出气体的速率明显减慢,说明其原因_____。
(5)用惰性电极电解U形管中的饱和食盐水(已滴加酚酞),_____极附近溶液会变红。写出用惰性电极电解氯化铜溶液的化学反应方程式_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】新型纳米材料MFe2Ox(3<x<4)中M表示+2价的金属元素,在反应中化合价不发生变化。常温下,MFe2Ox能使工业废气中的SO2转化为S,流程如下:
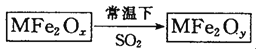
则下列判断正确的是( )
A.x>yB.MFe2Ox是还原剂C.SO2是该反应的催化剂D.SO2发生了置换反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学研究小组探究外界条件对化学反应mA(g)+n(B)(g) ![]() pC(g)的速率和平衡的影响图像如下,下列判断正确的是( )
pC(g)的速率和平衡的影响图像如下,下列判断正确的是( )
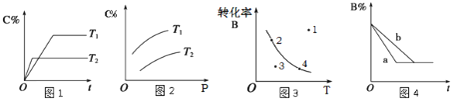
A.由图1可知,T1<T2,该反应正反应为吸热反应
B.由图2可知,该反应m+n<p
C.图3中,表示反应速率v(正)>v(逆)的是点3
D.图4中,若m+n=p,则a曲线一定使用了催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化氯(ClO2)是一种广谱、高效的杀菌消毒剂,有与氯气相似的强烈刺激性气味,易溶于水,沸点11℃,遇热不稳定易分解发生爆炸。一种工业制法用硫铁矿(主要成分为FeS2)还原氯酸钠制取二氧化氯,某研究小组在实验室设计如下装置制备ClO2的水溶液。
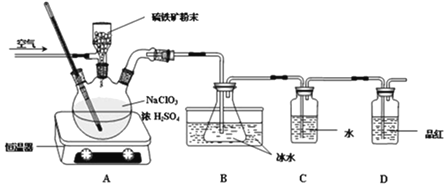
(1)三颈烧瓶中加入NaClO3溶液、浓H2SO4,通入空气,调节恒温器至60℃,通过固体加料器缓慢匀速加入硫铁矿粉末。反应开始时烧瓶内发生反应的离子方程式如下,请配平该方程式:__ClO3- +__FeS2+__H+=____ClO2+____Fe3++____SO42-+____H2O
(2)装置D的作用是__________。
(3)用上述反应完后的废液(除上述产物外,还有Al3+、Mg2+、H+、Cl-等)可制备摩尔盐,即(NH4)2Fe(SO4)2·6H2O。其操作流程如下:

回答下列问题:
①操作Ⅰ的名称为:___________。
②试剂X是___________,写出发生的主要反应的离子方程式__________。
③为测定(NH4)2Fe(SO4)2·6H2O晶体中铁的含量,某实验小组做了如下实验:用电子天平准确称量5.000g硫酸亚铁铵晶体,配制成250mL溶液。取所配溶液25.00mL于锥形瓶中,加稀H2SO4酸化,用0.01000mol/L KMnO4溶液滴定至Fe2+恰好全部氧化成Fe3+,同时,MnO4_被还原成Mn2+。测得消耗KMnO4溶液的平均体积为21.00mL。则该晶体中铁的质量分数为___________。(保留4位有效数字)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.《抱朴子》中“丹砂烧之成水银,积变又还成丹砂”两个反应互为可逆反应
B.电热水器用镁棒防止内胆腐蚀,原理是牺牲阴极的阳极保护法
C.门捷列夫根据元素的性质随着相对原子质量递增呈现周期性变化规律,制出了第一张元素周期表
D.石灰乳与海水混合,过滤得![]() ,将其溶于盐酸,再蒸发结晶得到
,将其溶于盐酸,再蒸发结晶得到![]() ,电解熔融
,电解熔融![]() 可得到金属镁
可得到金属镁
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢气是一种新型的绿色能源,又是一种重要的化工原料。
(1)氢气燃烧热值高。实验测得,在常温常压下1gH2完全燃烧生成液态水,放出142.9kJ热量。则表示H2燃烧热的热化学方程式为_____________________。又已知:![]() ,则氨气在空气中燃烧生成液态水和氮气时的热化学方程式为______________________。
,则氨气在空气中燃烧生成液态水和氮气时的热化学方程式为______________________。
(2)氢气是合成氨的重要原料。
①当合成氨反应达到平衡后,改变某一外界条件(不改变![]() 和
和![]() 的量),反应速率与时间的关系如图所示。
的量),反应速率与时间的关系如图所示。
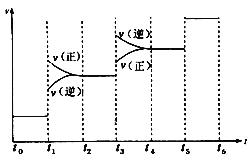
图中t1时引起平衡移动的条件可能是_______________,其中表示平衡混合物中NH3的含量最高的一段时间是______________。
②氨催化氧化可以制硝酸,此过程中涉及氮氧化物,如![]() 等。对于反应:
等。对于反应:![]() ,在温度为
,在温度为![]() 时,平衡体系中NO2的体积分数随压强变化曲线如图所示。
时,平衡体系中NO2的体积分数随压强变化曲线如图所示。
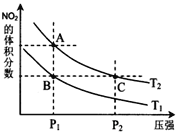
下列说法正确的是______。
a.![]() 两点的化学平衡常数:
两点的化学平衡常数:![]()
b.![]() 两点的气体颜色:
两点的气体颜色:![]() 浅,
浅,![]() 深
深
c.![]() 两点的气体平均相对分子质量:
两点的气体平均相对分子质量:![]()
d.![]() 两点的反应速率:
两点的反应速率:![]()
e.由状态B到状态A,可以用加热的方法
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向20mL含有1mol/L的氯化铝和一定量盐酸的溶液中逐滴加入浓度为1mol/L的氢氧化钠溶液,产生沉淀的质量与所加碱的体积如图所示:
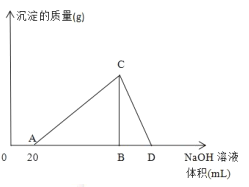
(1)写出AC段和CD段发生反应的离子方程式:
AC_______________________________________
CD_______________________________________
(2)盐酸溶液的浓度是____________________。
(3)若产生0.78g白色沉淀,则加入的氢氧化钠溶液的体积可能是__________________。
(4)D点表示的氢氧化钠溶液的体积是______________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com