
| �� | �� | �� | �� | ||
| ��ʼ���ʵ��� | n��SO2��/mol | 0.40 | 0 | 0.80 | 0.02 |
| n��O2��/mol | 0.24 | 0 | 0.48 | 0.04 | |
| n��SO3��/mol | 0 | 0.40 | 0 | 0.40 | |
| ����Ӧ���ƽ��ת����% | 80 | ��1 | ��2 | ��3 | |
| A������SO3��ƽ��ת����Ϊ��1=20% |
| B��ƽ��ʱ������c��SO3���Ǽ��е�2�� |
| C��ƽ��ʱ����3����1 |
| D�����¶��£�ƽ�ⳣ����ֵΪ400 |
| 0.162 |
| 0.042��0.04 |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
A��NaCl�ĵ���ʽ��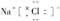 |
| B������ʱ����ʳ�β����ƻ�NaCl�еĻ�ѧ�� |
| C���ӵ�ʳ���мӵ���KIO3 |
| D��NaCl����ˮ�������룺NaCl=Na++Cl- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��Fe��S��ϼ�������FeS2 |
| B��������ͭ��Ũ���ᷴӦ��һ���������� |
| C��NaHCO3�����ȶ��Դ���Na2CO3 |
| D�������ڿ����м��ȵ�һ���¶���ת��Ϊ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��ͨ��״̬�£�O2��O3�Ļ����16��������ԭ����ΪNA |
| B����NO2��N2O4���ӹ�NA����������״���£������Ϊ22.4L |
| C������£�11.2LSO3�����ķ�����ĿΪ0.5 NA |
| D��15.6gNa2O2������CO2��Ӧʱ��ת�Ƶ�����Ϊ0.2NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A�����ķ�Ӧ����=0.5mol/��L?min�� |
| B������ķ�Ӧ����=0.5mol/��L?min�� |
| C�����������ķ�Ӧ����=0.5mol/��L?min�� |
| D�������ķ�Ӧ����=0.5mol/��L?min�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

| A��A������������һ���������ܷ���ˮ�ⷴӦ |
| B��A��һ�������¿���3mol H2�����ӳɷ�Ӧ |
| C����������A���ӽṹ�������л���ֻ��һ�� |
| D����A����ͬ������ͬ���칹��ֻ��2�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A�����顢������CH4 |
| B�������ᡢ���ᡢHCl |
| C���������ơ���NaOH |
| D�������ơ���ʯ�ҡ�CaCO3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��������ȼ�� |
| B�����ڸ߷��ӻ����� |
| C�����ܷ���������Ӧ |
| D�������ụΪͬ���칹�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
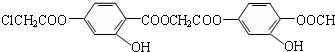 ��˵������ȷ���ǣ�������
��˵������ȷ���ǣ�������| A�����л�������к�����ԭ�ӡ��ǻ����Ȼ��ȹ����� |
| B�����л������Ũ��ˮ�����ӳɷ�Ӧ�������ܷ�ȡ��ȥ��Ӧ |
| C�����л���������������ˮ�⣬���ɵ��л���ֻ������ |
| D��1mol�û�����������10molNaOH��Ӧ |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com