
【题目】加热聚丙烯废塑料可以得到炭、氢气、甲烷、乙烯、丙烯、苯和甲苯。用如图所示装置探究废塑料的再利用。下列叙述中不正确的是( )

A.装置乙的试管中可收集到芳香烃B.装置丙中的试剂可吸收烯烃
C.最后收集的气体可作燃料D.该实验是聚丙烯发生加聚反应的实验
【答案】D
【解析】
由图可知,装置探究废旧塑料的再利用,加热聚丙烯废塑料可以得到碳、氢气、甲烷、乙烯、丙烯、苯和甲苯,冷却时乙试管中得到苯与甲苯,在丙中乙烯、丙烯发生加成反应,最后收集的气体为氢气、甲烷,以此来解答。
由图可知,装置探究废旧塑料的再利用,加热聚丙烯废塑料可以得到碳、氢气、甲烷、乙烯、丙烯、苯和甲苯,冷却时乙试管中得到苯与甲苯,在丙中乙烯、丙烯发生加成反应,最后收集的气体为氢气、甲烷,
A. 冷却时乙试管中得到苯与甲苯,均为芳香烃,A项正确;
B. 乙烯、丙烯与溴发生加成反应制取卤代烃,B项正确;
C. 最后收集的气体为氢气、甲烷,均具有可燃性,可作燃料,C项正确;
D. 该实验为聚丙烯分解再利用实验,不是加聚反应实验,D项错误
答案选D。


 习题精选系列答案
习题精选系列答案科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式书写正确的是
A.Cl2与水反应:Cl2+H2O=HCl+HClO
B.Fe与稀盐酸反应:2Fe+6H+=2Fe3++3H2↑
C.CaCl2溶液和Na2CO3溶液反应:Ca2++CO32-=CaCO3↓
D.CaCO3 和稀硝酸反应:CaCO3+H+=Ca2++CO2 ↑ + H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究与深度开发CO、CO2的应用对构建生态文明社会具有重要的意义。
(1)CO可用于炼铁。高炉炼铁过程中发生的主要反应为:![]() Fe2O3(s)+CO(g)
Fe2O3(s)+CO(g)![]()
![]() Fe(s)+CO2(g),已知该反应在不同温度下的平衡常数如下:
Fe(s)+CO2(g),已知该反应在不同温度下的平衡常数如下:
温度/°C | 1000 | 1150 | 1300 |
平衡常数 | 4.0 | 3.7 | 3.5 |
则该反应的平街常数表达式K=_________,H_________0(填“>”、“<”或“=”)。
(2)CO2可用于生产燃料甲醇。一定条件下发生反应:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g),为探究该反应原理,将1 mol CO2和3 mol H2充入一容积为1L的密闭容器中,分别在250°C、T°C下发生反应,测得甲醇的物质的量随时间的变化如下图所示。
CH3OH(g)+H2O(g),为探究该反应原理,将1 mol CO2和3 mol H2充入一容积为1L的密闭容器中,分别在250°C、T°C下发生反应,测得甲醇的物质的量随时间的变化如下图所示。
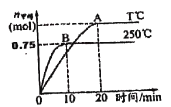
请分析并回答下列问题:
250°C时,反应在前10min的平均速率v(H2)_________molL-1min-1,从反应开始到平衡,CO2转化率为_________%。相同温度下,若某时刻该容器中含有1 mol H2、1.2mol CO2、0.8mol CH3OH、1.5 mol H2O,则此时反应所处的状态为____________________________________(填“向正反应方向进行中”、“向逆反应方向进行中心”或“平衡状态”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水中含有80多种元素,是重要的物质资源宝库,同时海水具有强大的自然调节能力,为解决环境污染问题提供了广阔的空间。
(1)①已知不同pH条件下,水溶液中碳元素的存在形态如下图所示。

下列说法不正确的是_____________ (填字母序号)。
a. pH=8时,溶液中含碳元素的微粒主要是HCO3-
b. A点,溶液中H2CO3和HCO3-浓度相同
c. 当c(HCO3-)=c(CO32-)时,c(H+)>c(OH-)
②向上述pH=8.4的水溶液中加入NaOH溶液时发生反应的离子方程式是_____________。
(2)海水pH稳定在7.9~8.4之间,可用于烟道气中CO2和SO2的吸收剂。
①海水中含有的OH-可以吸收烟道气中的CO2,同时为海水脱钙,生产CaCO3。写出此反应的离子方程式:_____________。
②已知:25℃时,H2CO3电离平衡常数K1=4.3×10-7 K2=5.6×10-11
H2SO3电离平衡常数K1=1.5×10-2 K2=6.0×10-8
海水中含有的HCO3-可用于吸收SO2,该过程产物中有CO2和_____________。
(3)洗涤烟气后的海水呈酸性,需处理后再行排放。与新鲜海水混合同时鼓入大量空气排出部分CO2,是一种处理的有效方式。
①通入O2可将酸性海水中的硫(IV)氧化,该反应的离子方程式是_____________。
②上述方式使处理后海水pH升高的原因是_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)已知CH3OH(l)的燃烧热ΔH=-238.6kJ/mol,CH3OH(l)+ ![]() O2(g) =CO2(g)+2H2O(g)ΔH=-a kJ/mol,则a___238.6(填“>”、“<”或“=”)。
O2(g) =CO2(g)+2H2O(g)ΔH=-a kJ/mol,则a___238.6(填“>”、“<”或“=”)。
(2)如图是通过热化学循环在较低温度下由水或硫化氢分解制备氢气的反应系统原理。

通过分析,可知系统(Ⅰ)和系统(Ⅱ)制氢的热化学方程式分别为_______、________。
(3)反应mA(g)+nB(g)![]() pC(g) +qD(g)过程中的能量变化如图所示,回答下列问题。
pC(g) +qD(g)过程中的能量变化如图所示,回答下列问题。
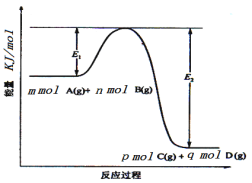
该反应ΔH=____kJ/mol(用含E1、E2式子表示);在反应体系中加入催化剂,E1___,E2___,(填增大、减小、不变)。
(4)已知:CO (g) +H2O (g)![]() H2 (g) +CO2 (g) K,C(s)+CO2(g)
H2 (g) +CO2 (g) K,C(s)+CO2(g)![]() 2CO(g) K1,C(s) +H2O(g)
2CO(g) K1,C(s) +H2O(g)![]() CO(g) +H2(g) K2 ,则K、K1、K2之间的关系是 ___________。
CO(g) +H2(g) K2 ,则K、K1、K2之间的关系是 ___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】![]() 在KI溶液中存在平衡
在KI溶液中存在平衡![]() 。某
。某![]() 、KI混合溶液中,
、KI混合溶液中,![]() 的物质的量浓度
的物质的量浓度![]() 与温度T的关系如图所示
与温度T的关系如图所示![]() 曲线上的任何一点都表示平衡状态
曲线上的任何一点都表示平衡状态![]() 。下列说法正确的是( )
。下列说法正确的是( )

①![]()
②若温度为![]() 、
、![]() 时反应的平衡常数分别为
时反应的平衡常数分别为![]() 、
、![]() ,则
,则![]()
③若反应进行到状态D时,一定有![]()
④状态A与状态B相比,状态A的![]() 大
大
⑤保持温度不变,向该混合溶液中加水,![]() 将变大
将变大
A.只有①②B.只有②③C.①③④D.①③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学设计如图装置进行乙醇氧化反应的探究实验,有关说法不正确的是()
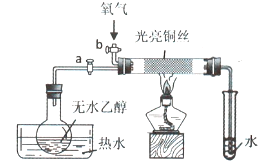
A.热水的作用是促使乙醇挥发,为硬质玻璃管内提供乙醇蒸汽
B.通入乙醇蒸汽反应的过程中,撤离酒精灯后反应仍能进行
C.在硬质玻璃管内发生的主反应为:![]()
D.实验结束时,先停止加热,再关闭活塞a、b,最后将导管移出水面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究表明,氮氧化物和二氧化硫在形成雾霾时与大气中的氨有关(如下图所示)。下列叙述错误的是

A. 雾和霾的分散剂相同
B. 雾霾中含有硝酸铵和硫酸铵
C. NH3是形成无机颗粒物的催化剂
D. 雾霾的形成与过度施用氮肥有关
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在一密闭容器中充入2mol HI气体,发生反应:2HI(g) ![]() H2(g)+I2(g) ΔH>0 ,达到化学平衡状态后,为使体系颜色加深,可采取的措施是( )
H2(g)+I2(g) ΔH>0 ,达到化学平衡状态后,为使体系颜色加深,可采取的措施是( )
①维持温度和容器体积不变,再充入少量I2(g) ②维持温度和压强不变,再充入2molHI ③降低温度 ④加压(缩小容器体积) ⑤升高温度
A.①④⑤B.②③C.②③④D.①②⑤
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com